2. 北京中医药大学管理学院 北京 100029
2. School of Management, Beijing University of Chinese Medicine, Beijing 100029, China
在卫生技术评估中,成本—效果分析(cost-effectiveness analysis, CEA)和成本—效用分析(cost-utility analysis, CUA)是两种最常用的评估方法。一些学者将成本—效用分析视为成本—效果分析的特殊情况,即不采用单一临床效果指标,而使用质量调整生命年(Quality-adjusted life years, QALY)这个综合指标时的成本—效果分析。[1]在世界范围内,越来越多的国家(如加拿大、澳大利亚、英国等)在《药物经济学评价指南》中要求同时提供平均成本—效果比数据(average cost-effectiveness ratio, CER)和增量成本—效果比(incremental cost-effectiveness ration,ICER)数据。其中,增量成本—效果比是成本—效果分析中评价结果最常用的方法[2],特别是基于QALYs这一综合指标构建的ICER在卫生政策制定过程中得到了非常广泛的应用。[3]
CEA是以特定的治疗目的或临床效果为指标,比较不同治疗方案获得单位健康产出所需成本的分析方法,常用的评价指标包括CER和ICER。其中,CER表示产生单位健康产出所需的平均成本,通常用于评估单个治疗方案的效率高低;ICER指增量成 本除以增量健康产出,表示增加一单位的健康产出所消耗的增量成本,可用于评价两个及以上替代治疗方案之间的相对经济性。
假设两种治疗方案A和B,其中A为新治疗方案,B为旧治疗方案或标准治疗方案,采用两种治疗方案产生的成本分别为CA 和CB,获得的健康产出分别为EA 和EB,则:A方案的成本—效果比即CERA=CA/EA,B方案的成本—效果比即CERB= CB/EB;A方案相对于B方案的增量成本—效果比即ICER=(CA-CB) /(EA-EB),其中△C= CA -CB为增量成本,△E=EA -EB为增量健康产出。
当采用CER作为评价准则时,通常以比值最小的方案作为最优选择,表示该方案给患者带来单位健康产出的成本最小,因而效率最高。然而,在现实卫生决策中,效率并不构成唯一的决策依据,还需考虑诸如公平、伦理、健康价值等其它因素。
一般而言,新治疗方案相对于旧治疗方案在改善健康结果的同时往往也增加了成本,即EA >EB, CA >CB。假如CERA >CERB即新方案的效率小于旧方案,若仅以效率高低作为评价指标B为最优方案。但是A方案获得的健康改善优于B方案,决策者必须考虑健康改善会导致社会整体福利水平的提高,此时A方案有可能成为最优方案。此时,决策者关注的焦点是为了获得特定的健康结果改善,采用A方案比B方案多支付的成本是否值得,因此需要引入ICER辅助决策制定。
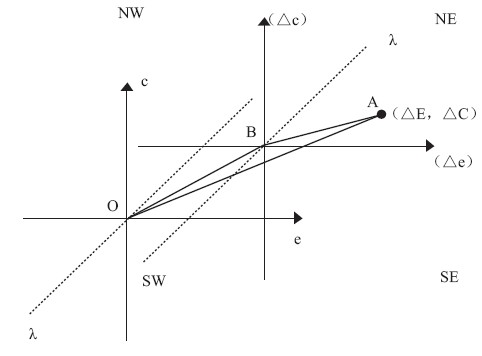
Black在1990年建立了成本—效果象限图(the cost-effectiveness plane, the CE plane)的雏形,用于解决成本效果含义不明确的问题,以及说明其与卫生决策制定的关系。[4]成本效果 象限图(见图1坐标系△eB△c)以基准方案为原点(本文指方案B),横坐标为健康产出差异值,即△e,纵坐标为成本差异值,即△c①。共有四个象限,这里简称为NE(Northeast)、NW(Northwest)、SW(Southwest)和SE(Southeast)。
① 由于基准方案不同,一些文献中将横纵坐标分别定为e和c,此时的基准方案可视没有任何干预 (视为方案O),经过坐标平移之后其本质含义与横纵坐标设为△e和△c时是一致的。
|
图1 CER与ICER在成本效果象限图中的实现 注:为了便于阐述,本文设计了两个坐标系:eOc和△eB△c,后者可以通过前者平移得到。坐标系eOc以O为原点,方案O可视为未采用任何干预措施,则O与A连线的斜率为方案A的平均成本—效果比率CERA,O与B连线的斜率即为方案B的平均成本—效果比率CERB。A与B连线的斜率即为ICER。为了便于ICER与成本—效果阈值λ比较,将坐标系eOc向右上平移得到坐标系△eB△c,即以B为原点。此时直线λ将坐标系△eB△c分成两个区域,右下区域为成本—效果区,左上区域为非成本—效果区。 |
根据△C和△E的取值情况,可以将ICER的结果分为如下四种情况:(Ⅰ)△C<0,△E>0,ICER为负值,即相对于B而言A为优势方案;(Ⅱ)△C>0,△E<0,ICER为负值,即相对于A而言B为优势方案;(Ⅲ)△C<0,△E<0,ICER为正值,即相对于B而言A消耗的成本及获得的健康产出均小于B;(Ⅳ)△C>0,△E>0,ICER为正值,即相对于A而言B消耗的成本及获得的健康产出均小于A。
在现实决策制定过程中,(Ⅰ)位于SE象限,表示新治疗方案与旧治疗方案相比,虽然成本减少了,但是健康产出增加了,因此我们必然会接受新方案;(Ⅱ)位于NW象限,表示新方案相对于旧方案,成本增加但是健康产出减少,所以我们不会采纳新方案;(Ⅲ)和(Ⅳ)分别位于SW和NE象限,说明新方案相对于老方案而言,成本和健康产出同时增加或减少,使得决策过程变得复杂。因此本文将重点讨论ICER为正值时如何进行决策选择。
如前所述,由于卫生技术评估是对两种或两种以上治疗方案的比较,通常一种治疗方案在增加健康产出的同时可能也增加了成本,但决定是否采用该种治疗方案还需要进行增量分析,即判断采用该种治疗方案后,增加一单位健康产出所支付的成本是否值得。此时需要引入一个外部参考值λ(也称为成本效果阈值),即增加一单位健康产出的最大支付意愿。[2]若增量分析的结果小于λ,则认为该治疗方案是可以接受的,否则拒绝该方案。
各国卫生决策制定者通常将增加一个QALY的最大支付意愿作为外部参考值λ,由于各国经济发展水平、对生命价值的预期等不同,因此λ的取值各异。[5]这也使得同一治疗方案在不同国家的卫生决策过程中的接受意愿是不同的。
因此若满足:(1)当△E>0时,ICER=△C /△E<λ, 或者(2)当△E<0时,ICER=△C /△E>λ,新方案A相对于方案B而言是具有成本效果优势的。
ICER为比率形式,比率间差异的统计学检验引入了一些额外的复杂因素,因此一些学者提出用净效益作为反映医疗项目货币价值的一项综合指标。[6, 7]净效益分析通常作为ICER分析的替代分析方案进行。[7, 8, 9] 净效益的方法是为了克服成本—效果比率所带来的统计学问题而采用的一种简单的决策规则。[2]如上文所述,将(1)当△E>0时, △C /△E<λ, 或者(2)当△E<0时, △C /△E>λ重新整理可得:λ△E-△C >0。
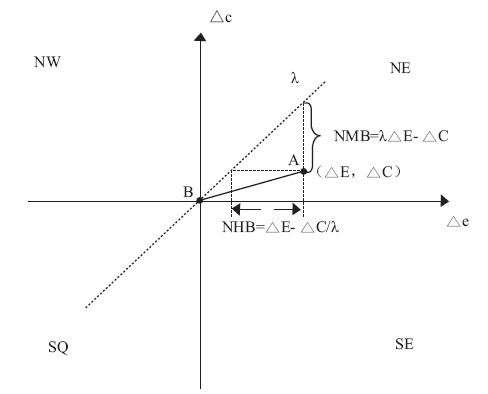
λ△E-△C称为干预方案的净货币效益(Net monetary benefit,NMB),在使用净货币效益进行决策时,无论△E取正值还是负值,只要NMB=λ△E-△C>0时就可以认为干预方案具有成本效果优势。另外,净健康效益(Net health benefit, NHB)也是经常使用的指标之一,NHB=△E-△C/λ>0时可认为干预方案具有成本效果优势。NMB与NHB在成本—效果象限图中的分布如图2。NMB与NHB均为正值,因此方案A在成本效果方面优于方案B。这与使用ICER进行决策选择所得的结论一致。
|
图2 NMB与NHB在成本—效果象限图中的实现 |
为了更好地说明这一方法的应用和展示如何使用ICER进行决策,本文引用2010年Punekar等一篇文章的数据和部分内容来举例说明。[10]
克罗恩病(crohndisease,CD),又称局限性回肠炎、局限性肠炎、节段性肠炎和肉芽肿性肠炎,是一种发病原因不明的肠道炎症性疾病。儿童克罗恩病的发病率低于成年人,然而近年来有上升趋势。克罗恩病严重影响儿童的生长发育及心理健康。另外,与健康儿童或患有某种慢性疾病(如1型糖尿病)的儿童相比,儿童克罗恩病患者易引发精神性疾患,如抑郁和焦虑等。在英国,有研究评估了成人克罗恩病对国家卫生服务系统(NHS)的影响,鲜有对儿童克罗恩病疾病经济负担方面的研究。
本研究从第三方支付者(英国国家卫生服务系统,NHS)的角度,评价英夫利昔单抗与标准方案(包括免疫调节剂或皮质类固醇之一作为对照)治疗重症儿童克罗恩病5年的长期成本效果。
采用成本—效果分析方法,使用马尔科夫模型模拟5年的疾病进展及长期成本,评价指标包括成本—效果比(CER)和增量成本—效果比(ICER)。成本及效果数据主要来自REACH临床试验①,成本单位为英镑,效果即健康产出的衡量单位为质量调整生命年QALY。成本和效果均采用3.5%的折现率进行折现。
① REACH是评估英夫利昔单抗用于治疗中度至重症儿童克罗恩病的安全性和有效性的随机对照临床研究。
模拟英夫利昔单抗与标准方案治疗1名重症儿童克罗恩病患者5年的长期成本效果分析结果见下表1。
| 表1 模拟5年的成本效果分析 |
由表可知,采用标准方案治疗的平均成本为25 987英镑,英夫利昔单抗的平均成本为34 012英镑,增量成本为8 025英镑;采用标准方案和英夫利昔单抗治疗获得健康产出分别为2.675QALY和3.224QALY,增量健康产出为0.549QALY。ICER=△C /△E=14 607②(英镑)
② 由于文中成本及健康结果数值取近似值,因此14 607与计算所得数值有误差。
根据英国国家卫生与临床优化研究所(NICE)推荐的每QALY的最大支付意愿(即λ)为20 000~30 000英镑,本研究所得ICER为14 607英镑,小于20 000英镑。因此英夫利昔单抗与标准方案相比治疗重症儿童克罗恩病具有成本效果优势。
敏感度分析结果显示英夫利昔单抗的疗效是ICER最重要的影响因素。当最大支付意愿为30 000英镑/QALY时,英夫利昔单抗有78.6%的可能性具有成本效果优势。
由表1可知,标准方案的成本—效果比CERS=9 715英镑/QALY,而英夫利昔单抗的成本—效果比CERT=10 550英镑/QALY,以上表明为获得等量的健康改善即一个质量调整生命年,采用两种治疗方案需要支付的单位成本分别为9 715英镑和10 550英镑,即标准方案的效率要高于英夫利昔单抗。
然而实际上,出于公平、伦理、健康价值等方面的考虑,NHS往往更加关注英夫利昔单抗在健康结果改善方面的积极作用,此时CER便不能作为唯一的评价指标。模拟1名重症儿童克罗恩症患者5年的成本效果分析表明,英夫利昔单抗比标准治疗方案多获得0.549QALY,但是需要多支付8 025英镑。此时NHS关心的是,为了多获得0.549QALY而多支付8 025英镑是否值得,即ICER为14 617英镑对于NHS而言是否可以接受?
本案例中,外部参考值λ的取值为20 000~30 000英镑/QALY,大于ICER数值。如图3所示,ICER落在成本—效果区,净货币效益NMB=λ△E-△C>0。综上所述,对于NHS而言,每多获得一个QALY而多支付14 607英镑是值得的,因此英夫利昔单抗与标准方案相比治疗重症儿童克罗恩病具有成本效果优势。

|
图3 英夫利昔单抗与标准方案比较的成本效果象限图 |
| [1] | Bambha K, Kim W. Cost-effectiveness analysis and incremental cost-effectiveness ratios: uses and pitfalls [J]. European Journal of Gastroenterology & Hepatology, 2004, 16(6):519-526. |
| [2] | Drummond M F, Sculpher M J, Torrance G W, et al. Methods for the Economic Evaluation of Health Care Programmes[M]. 3 ed. Oxford : Oxford University Press, 2005. |
| [3] | Firth B G, Cooper L M, Steve Fearn. The appropriate of cost-effectiveness in determining device coverage: a case study of drug-eluting stents[J]. Health Affairs, 2008, 27(6): 1577-1586. |
| [4] | Black W C. The C E plane: a graphic representation of cost-effectiveness [J]. Medical Decision Making, 1990, 10(3): 212-214. |
| [5] | Shiroiwa T, Sung Y K, Fukuda T, et al. International Survey on willing to pay (WTP) for One Additional QALY Gained: What is the Threshold of Cost Effectiveness? [J]. Health Economics, 2010, 19(4): 422-437. |
| [6] | Phelps C E, Mushlin A. On the (near) equivalence of cost-effectiveness and cost-benefit analyses [J]. Incremental Journal of Technology Assessment in Health Care, 1991, 7(1): 12-21. |
| [7] | Stinnett A, Mullahy J. Net health benefits: a new framework for the analysis of uncertainty in cost-effectiveness analysis [J]. Medical Decision Making, 1998, 18(2 Suppl.):S68-S80. |
| [8] | Comparative Benefits Modeling Project. A framework for cost-utility analysis of government health care programmes: a report to the Office of Disease Prevention and Health Promotion, Public Health Service, U.S. Department of Health and Human Services[R]. 1992. |
| [9] | Tambour M, Zethraeus N, Johannesson M. A note on confidence intervals in cost-effectiveness analysis [J]. International Journal of Technology Assessment in Health Care, 1998, 14(3): 467-471. |
| [10] | Punekar Y S, Sunderland T, Hawkins N. Cost-Effectiveness of Scheduled Maintenance Treatment with Infliximab for Pediatric Crohn’s Disease[J]. Value in Health, 2010, 2(13): 188-195. |
(编辑 刘 博)





