2. 国家食品药品监督管理总局药品评价中心 北京 100045;
3. 北京大学公共卫生学院 北京 100191;
4. 北京大学药学院 北京 100191;
5. 国家食品药品监督管理总局 北京 100053
2. Center for Drug Evaluation, China Food and Drug Administration, Beijing 100045, China;
3. Peking University School of Public Health, Beijing 100191, China;
4. Peking University School of Pharmaceutical Sciences, Beijing 100191, China;
5. China Food and Drug Administration, Beijing 100053, China
药品是预防、治疗、诊断疾病,有目的地调节生理机能并规定有适应症或者功能主治、用法和用量的物质[1, 2],应具有有效、安全、稳定的内在特性。然而由于药品上市前研究的局限,即病例数少、研究时间短、试验对象年龄范围窄、用药条件的严格控制、研究目的单纯,导致不能在上市之初就可以全面的认识和把握药品的属性,因此,药品安全并不意味着零风险[3, 4, 5],所谓安全的药品是人们认为它对人体损害的风险程度在可接受的水平,是权衡药品风险/收益的结果[6]。随着经济社会的发展和人民生活水平的提高,药品安全已经成为公共安全的重要组成部分,社会各界也对我国药品安全状况日益关注。药品安全问题不仅影响经济发展,而且已经成为重大的社会问题和公共安全问题。[7]虽然我国目前的监管体系建设已形成一定规模,但是迄今为止我国尚无具体的方法和综合评价指标评估药品安全形势。虽然以往评估药品安全往往通过质量抽验、不良事件发生例数和严重程度等统计数字进行说明描述,但这些统计结果相对于整个药品研究、生产、经营、使用环境而言都显得过于孤立,难以表明某一时期、某一范围内的药品监管工作整体形势。而且,无论这些绝对数量如何变化,都不能改变公众对药品安全形势的担心。[8]
本研究基于前期研究结果[8, 9],从影响药品安全的危险因素角度深入研究我国药品安全相关问题,探讨和建立我国药品安全综合评价指标,为进一步完善和推动我国药品安全综合评价工作提供参考。
药品安全综合评价涉及的内容十分繁杂,需要综合考虑与药品安全问题相关的诸多因素。文献综述方法可以系统总结影响我国药品安全的危险因素,确定药品安全综合评价的组成要素及其层次和结构,并对每个组成要素进行定义并说明各部分及各层级之间的相互关系,从而提出药品安全综合评价的备选指标。[10, 11]
文献检索资源涵盖中文数据库、英文数据库、中文网站和英文网站。其中英文数据库包括PubMed、American Society of Health-System Pharmacists (ASHP)、The Royal Society of Medicine (RSM);中文数据库包括中国期刊网全文专题数据库、维普数据库;中文网站包括国家食品药品监督管理局(SFDA)、SFDA药品评价中心、中国药品生物制品检定所、SFDA南方所、SFDA药品认证管理中心;英文网站包括World Health Organization(WHO)、U.S. Food and Drug Administration(FDA)、Agency for Healthcare Research and Quality (AHRQ)、Institute of Medicine(IOM)、European Medicine Agency(EMEA)。
综合评价备选指标提出以后,通过专家会议的方法讨论和确定综合评价指标。根据研究目的和专家会议法的要求[12, 13],选取了卫生政策、药事管理和临床合理用药等方面的12名具有高级职称,从事药品安全相关领域工作10年以上的专家和学者,从指标的重要性、敏感性、可靠性、可操作性和可比性等方面对备选指标进行评价,并按照专家的意见和建议筛选、修订、补充和完善药品安全综合评价指标。
对于文献综述和专家会议法仍无法确定的指标则进一步通过问卷法和访谈法进一步补充、筛选和确定。
采取文献综述方法,系统收集中文数据库、英文数据库、中文网站和英文网站的相关信息,经研究者系统整理和归纳后将药品风险分为药品研发风险、药品生产风险、药品经营风险、药品使用风险、药品监管风险和药品保障风险。(1)药品研发风险是由于上市前的动物实验与临床试验设计不严谨、试验结论失实和上市技术审批不严格等因素造成的。(2)药品生产风险包括生产过程偏离规范、人员道德素养缺失、擅自变更工艺或物料、企业管理混乱等导致的产品质量缺陷。[14](3)药品经营风险是指药品从生产领域到经营领域(医院药房和药店)的传递过程中,因进货途径、储存环境和出库管理环节混乱而导致药品质量改变。[15](4)药品使用风险是医师、药师或患者在用药过程中产生的风险,包括意外风险和人为的用药风险。[3](5)药品监管的风险包括监管体制、法制不健全,监管能力薄弱等。(6)药品保障的风险包括药品短缺、药品储备不足、可及性差和药品价格偏高等。
基于影响我国药品安全风险因素的研究结果,将我国药品安全评价分为药品研发安全评价、药品生产安全评价、药品经营安全评价、药品使用安全评价和药品保障安全评价五个方面。为了提高研究的针对性和可行性,结合我国目前药品工作的实际情况和专家意见,暂不将药品保障安全评价内容列入药品安全评价的范畴。
结合文献综述的结果,研究者整理和归纳后得到药品安全综合评价的备选指标池供专家会议筛选和补充。综合评价指标体系备选指标共包括药品研发安全、药品生产安全、药品经营安全、药品使用安全4个一级指标,可分解为26个二级指标,153个三级指标。
经过专家会议法的筛选、修订和补充,确定了药品安全综合评价的一级、二级指标和部分三级指标。其中,一级指标包括药品研发安全、药品生产安全、药品经营安全和药品使用安全。二级指标包括药品研发风险评价等13个指标(表1)。
|
|
表1 药品安全综合评价的一级和二级指标 |
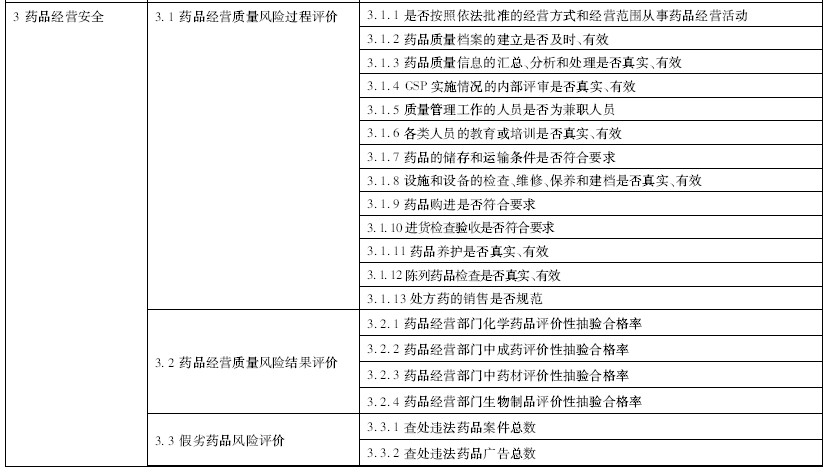
其中,药品生产和经营风险评价所涉及的三级指标最终没有取得统一的结果。与会专家认为这部分三级指标涉及药品生产质量管理规范(以下简称GMP)和药品经营质量管理规范(以下简称GSP)检查的内容,难以通过文献综述和专家会议的方式从GMP和GSP十分繁杂的检查内容中检查筛选和确定有针对性、可操作性强的核心指标。建议进一步征求药品生产和经营领域与GMP和GSP相关人员的意见,以探索目前实际工作中能够反映GMP和GSP检查结果的核心内容,并据此建立敏感性和可操作性强的指标。通过深入访谈征求药品生产和经营领域相关人员的意见,初步建立了药品生产和经营风险评价相关的三级指标。其中,药品生产风险评价分为质量风险过程评价、药品风险管理水平和质量风险结果评价三个方面,分别包括13个、5个和4个三级指标;药品经营风险评价分为质量风险过程评价、质量风险结果评价和假劣药品风险评价三个方面,分别包括13个、4个和2个三级指标(表2)。
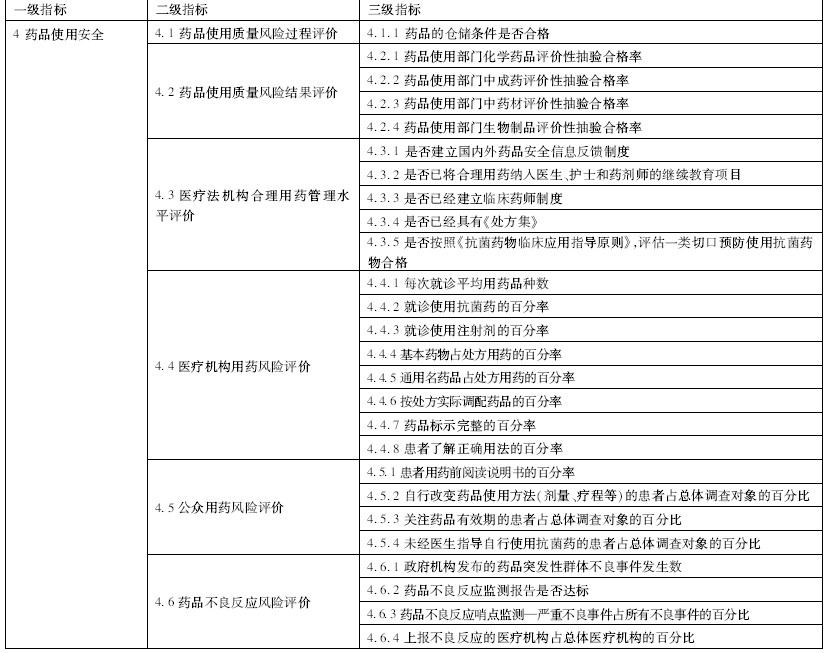
本研究参考国内外综合评价以及影响我国药品安全风险因素的研究结果,总结分析了我国药品安全评价的主要内容,经专家论证后提出了我国药品安全评价的框架,包括药品研发安全评价、药品生产安全评价、药品经营安全评价和药品使用安全评价四个方面。基于综合评价框架的内容,利用文献综述、专家会议、定性访谈和问卷调查等多种方法收集、整理、筛选和补充药品安全评价指标,提出了药品安全综合评价指标体系,共包括4个一级指标,13个二级指标,69个三级指标,具体指标如表2所示。
为保证药品研发的安全、有效和质量可控,规范药品注册行为,原国家药品监督管理局组织制定了《药品注册现场核查管理规定》(《管理规定》)。该规定将药品注册现场核查分为研制现场核查和生产现场检查两个部分。其中,药品注册研制现场核查,是指药品监督管理部门对所受理药品注册申请的研制情况进行实地确证,对原始记录进行审查,确认申报资料真实性、准确性和完整性的过程。涵盖了药物临床前研究现场核查、药物临床试验现场核查和申报生产研制现场核查三个方面;药品注册生产现场检查,是指药品监督管理部门对所受理药品注册申请批准上市前的样品批 量生产过程等进行实地检查,确认其是否与核定的或申报的生产工艺相符合的过程。包括新药、生物制品、已上市药品改变剂型、改变给药途径、仿制药、补充申请生产现场检 查和药品注册检验等方面内容。综上可知,药品注册研制现场核查和药品注册生产现场检查已经基本涵盖了药品研发风险评价的内容,可以作为药品研发风险评价的主要内容。
|
|
表2 我国药品安全综合评价指标 |
为了从不同角度反映药品生产质量风险评价水平,本研究将药品生产质量风险评价分为过程评价和结果评价。其中,GMP检查的相关内容作为药品生产质量风险过程评价的三级指标,而药品生产部门药品质量评价性抽验的结果作为药品生产质量风险结果评价的三级指标。
本研究参照国家药品生产质量管理规范检查(GMP检查)评定标准的相关内容,并广泛征求SFDA药品认证部门和药品生产企业质管部门的意见,选择GMP检查中客观、重要和灵敏的项目作为评价指标。在此基础上修订评价指标的提法和要求,以达到强调检查和评价过程真实、有效的目的。共提出13个三级指标。同时着重从两个方面考察生产企业GMP的执行情况。一是真实性,即生产企业是否如实按照GMP认证的要求对企业进行管理。二是有效性,即考量生产企业执行GMP认证的效果如何。可以采取现场抽查检验的方式,考评各个检查项目的真实性和有效性。药品安全并不意味着零风险,限于人类的认知水平和科技发展水平的限制,目前尚无法完全避免药品生产过程中的风险。因此早期发现、评估和干预药品风险,实现用药收益最大化、风险最小化的目标就显得尤为重要,为了体现药品风险管理的重要意义,本研究引入药品生产部门药品风险管理水平的评价指标。根据专家定性访谈的结果和新版GMP的要求,列举了影响药品生产部门药品风险管理水平的5个评价指标。
药品生产部门药品质量评价性抽验是药品监督管理部门为掌握、了解辖区内药品质量总体水平与状态而进行的抽查检验工作 。[16]因此本研究采用评价性抽验的结果反映药品安全—药品质量和状态的总体水平。药品质量评价性抽验涉及药品生产、经营和使用环节,抽验药品按照类别主要可分为化学药品、中成药、中药材和生物制品几种类型。为了充分反映不同环节中不同类型药品的抽验结果,本研究按照生产、经营和使用部门分类别设计评价性抽验的指标。药品生产部门药品质量评价性抽验共包括四个三级指标。
与药品生产质量风险评价指标相同,本研究将药品经营质量风险评价分为过程评价和结果评价。其中,GSP检查的相关内容作为药品经营质量风险过程评价的三级指标,而药品经营部门药品质量评价性抽验的结果作为药品经营质量风险结果评价的三级指标。GSP检查将药品经营企业分为药品批发企业和药品零售企业两种类型。本研究在深入访谈的过程中发现药品批发企业和零售企业在执行药品经营质量管理规范时工作的重点和难点基本是一致的,为了减少评价指标设置的个数,本研究在广泛征求SFDA药品认证部门和药品经营企业质管部门意见的基础上,将其相同部分合并统一设置评价指标。本研究共提出13个三级指标,与生产安全评价一样,着重从真实性和有效性两个方面考察经营企业GSP的执行情况。
与药品生产质量风险评价指标相同,本研究将药品使用质量风险评价分为过程评价和结果评价。其中,药品使用质量管理规范的相关内容作为过程评价的三级指标,而药品使用部门药品质量评价性抽验的结果作为结果评价的三级指标。目前,SFDA没有对药品使用质量管理规范做出统一规定,部分省局为了规范药品使用部门的药品质量,制定了《药品使用质量管理规范》。本研究在参照各省局制定的药品使用质量管理规范条款和征求专家意见过程中,发现药品仓储条件是否合格是各方专家普遍关注的焦点,因此选取“药品仓储条件是否合格”作为评价药品使用质量管理规范的指标。
“医疗机构合理用药管理”的指标是在参考WHO促进合理用药管理策略的基础上,经过专家研讨会结合中国的实际情况确定下来的;医疗机构合理用药是反映药品使用安全的重要方面,而医疗机构处方评价是衡量医疗机构合理用药的重要参考,也是衡量医疗机构用药风险评价的重要参考。本研究参照处方评价和“WHO监测和评价国家药物状况的操作包”中的合理用药相关内容作为医疗机构用药风险评价指标。
为了全面评价公众用药风险,本研究主要针对公众用药的安全认知、安全意识、安全行为和依从性的方面进行评价。公众用药风险评价的结果对于评价我国药品安全状况而言非常重要,但是我国目前这方面的调查研究工作并不多,建议在各个地区有计划的实施公众用药风险情况的调查,调查结果可为了解公众用药实际情况,有针对性的对公众开展合理用药干预,提高总体合理用药水平提供帮助。药品不良反应情况可以通过药品不良反应报告的情况而进行考量,目前药品不良反应报告属于被动报告模式,漏报的情况十分常见,报告率过低并不反应药品安全形势良好,而是监测工作不到位的表现。 因此我们需要鼓励责任单位报告不良反应,提高报告的质量,通过有效的监测工作,将药品不良反应的发生限制在较少或者可接受的范围内。因此,为反映药品不良反应风险评价的结果,本研究主要选择了能够反应药品安全形势的群体性指标和主动监测的指标。
本研究选用文献综述的方法收集和整理综合评价备选指标,然后采用专家会议法进一步筛选、修订和补充药品安全综合评价指标。共包括4个一级指标,13个二级指标和69个三级指标。这些指标是经过与会专家的筛选、修订、补充、完善以后,严格遵守专家意见确定的。随着我国药品安全监管形势的变化和药品监管手段的更新,尤其是新版GMP的施行,本研究所提出的指标需要进一步修改完善。
另外,本研究虽然初步构建了药品安全的综合评价指标体系,然而在研究过程中发现一些很重要的评价指标由于目前条件所限,不能搜集到原始数据。为了进一步完善药品安全综合评价指标体系,特提出以下政策建议:一是进一步加强收集和整理药品质量管理规范检查资料;二是分部门分类别统计药品抽验结果;三是逐步开展医疗机构合理用药 管理的检查和信息整理; 四是提高对医疗机构处方评价资料的整理和利用;五是逐步开展公众合理用药调查工作;六是稳步推动药品不良反应哨点监测工作。
| [1] | 关于药品的定义[EB/OL].(2006-12-12). http://www. instrument.com.cn/search/BBSArchive_664835_1.htm. |
| [2] | 中华人民共和国药品管理法.[EB/OL].(2009-06/17). http://baike.baidu.com/view/414733.htm?fr=ala0. |
| [3] | Bates D W, Cullen D J, Laird N, et al. Incidence of adverse drug events and potential adverse drug events-Implications for prevention. ADE Prevention Study Group[J]. Journal of the American Medical Association, 1995, 274(1): 29-34. |
| [4] | Miller G C, Britth H C, Valenti L. Adverse drug events in general practice patients in Australia.[J]. Medical Journal of Australia, 2006,184: 321-324. |
| [5] | Baker G R, Norton P G, Flintoft, et al. The Canadian Adverse Events Study: the incidence of adverse events among hospital patients in Canada[J]. Canadian Medical Association Journal, 2004, 170: 1678-1686. |
| [6] | 龚时薇, 张亮, 黄杰敏, 等. 药品安全与风险管理[J]. 中国药房,2007, 22(18): 1687-1690. |
| [7] | 尚鹏辉, 刘继同, 刘佳, 等. 从社会风险的角度反思药品安全问题[J]. 中国药物警戒, 2010, 4(7): 226-228. |
| [8] | 刘佳. 中国药品安全的定义和范畴研究[D]. 北京: 北京大学, 2009. |
| [9] | 北京大学医学部. 中国药品安全评价指标体系政策研究终报告[R]. 北京: 国家食品药品监督管理局, 2009. |
| [10] | 韩仲琪. 医学文献综述的特点及方法[J]. 中华医学写作, 1995, 3(2): 3-5. |
| [11] | 段玉斌, 毕辉, 韩雪峰. 文献综述的写作方法[J]. 西北医学教育, 2008, 1(16): 163-165. |
| [12] | 专家会议法[EB/OL]. [2009-10/09]http://www.hudong.com/wiki/专家会议法 |
| [13] | 孙振球, 王乐三. 医学综合评价方法及其应用[M]. 北京: 化学工业出版社, 2006. |
| [14] | 孙彩虹. 药品安全与政府监管责任-以齐齐哈尔第二制药有限公司假药案为例[J]. 中国浦东干部学院学报, 2008, 1 (2): 109-115. |
| [15] | 美“泰诺”胶囊杀人启示录[EB/OL].[2003-06/16]. http://www.huaxia.com/200373/00035834.html. |
| [16] | 关于印发药品质量抽查检验管理规定的通知[EB/OL].[2006-07/21]. http://www.law-lib.com/law/law_view.asp?id=169108. |
(编辑 刘 博)