罕用药是指用来治疗罕见疾病(rare disease)的药物。对罕用药激励机制的研究源自对罕见疾病的认识。所谓罕见疾病,泛指危及生命或慢性的、发病率低、非常见性的疾病。1983年的美国《罕用药法案》(the Orphan Drug Act,ODA)将每年患病人数少于20万人(约占总人口的0.75%)或高于20 万人但药物研发和生产没有商业回报的疾病界定为罕见疾病。[1]这些病症由于患病者少,患者分布各地,在医学界就如散落在角落的“孤儿”一般,故又称“孤儿病”。
罕见疾病虽然罕见,但受此类疾病折磨的患者和承受巨大压力的家庭却不在少数。2008年美国国家卫生研究院(National Institute of Health,NIH)下设的罕见疾病办公室(Office of Rare Diseases,ORD)共认定6 819种罕见疾病,这些疾病困扰着大约2 000万~2 500万美国人的日常生活,占全美人口的6%~8%,同时每年大约有250种新的罕见疾病或临床新情况被发现。[2]相关数据显示,2014年全球罕见疾病数量多达7 000余种,绝大多数是遗传性疾病。[3]
由于罕见疾病单病种患病人数少,难以治愈,导致每一种罕用药的市场规模极小,而研发成本却因为疾病的疑难少见而大大增加。在研发风险大、利润难以保障的情况下,很少有制药公司和科研机构愿意投入大量资源用于研发罕用药。罕用药市场面临困境。
美国是世界上市场经济最发达的国家,同时也是罕用药上市最多的国家,这与美国卓有成效的罕用药市场激励机制有很大关系。在严重失灵的罕用药市场中,“看得见的手”如何诱导“看不见的手”,值得我们研究和借鉴。
当“看不见的手”无法保证社会目标的实现时,其他机制就会出现用以改进甚至替代市场机制。美国政府在面对罕用药市场的严重失灵时,采取了以“政府撬动市场”的激励机制。市场激励机制的本质是激励相容,即政策的制定者通过机制设计给每个市场参与者以激励,从而使参与者在最大化个人利益的同时实现预定的公共目标。[4]
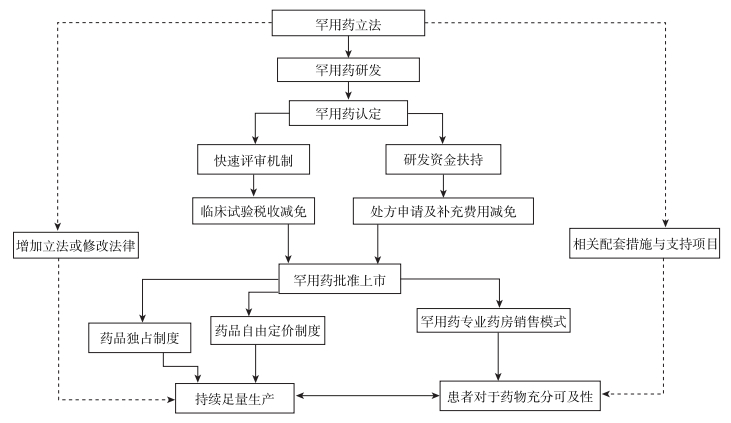
美国政府在设计罕用药市场激励机制时,综合运用了多种激励工具,以期达到激励相容的结果,其总体建构和运作框架如图 1所示。
|
注:立法修改往往不定时出现,而配套措施则有可能关联了更多的社会组织与人群。两者都无法完全放入实线路径中,但又确实起到激励作用,故以虚线表示 资料来源:FDA. Financial Assistance and Incentives for Research and Development of New Drug/Biologic Products[EB/OL]. http://www.fda.gov/downloads/aboutfda/centersoffices/officeofmedicalproductsandtobacco/cder/ucm118328.pdf. FDA. Overview of the Office of Orphan Products Development: Incentives for Rare Diseases[EB/OL]. http://www.fda.gov/downloads/drugs/developmentapprovalprocess/smallbusinessassistance/ucm276029.pdf. 图 1 美国罕用药市场激励机制的总体路径 |
罕用药立法是罕用药市场激励机制建立的起点。立法使政府这只“看得见的手”干预罕用药市场合法化、制度化和常态化。20世纪70年代,美国就开始了相关立法的准备工作。1983年《罕用药法案》的通过标志着美国罕用药市场激励机制的形成。该法案明确界定了罕用药的内涵,同时规定了一系列旨在促进罕用药研发销售的激励措施。[5]后来美国对ODA进行了多次修订,并通过了《罕用药监管条例》等多个法律文件,进一步完善罕用药的认定标准和激励机制(表 1)。ODA出台以来,美国罕用药上市数量从10种迅速增至近500种[6],立法工作为美国罕用药市场的发展提供了一个良好的制度环境。
| 表 1 美国罕用药市场激励机制相关法律文件的制定和修订 |
在一个供需极度失衡的市场中,调整供需格局的激励机制主要针对市场短缺的一方。美国罕用药市场激励机制的设计遵循了这一原理。美国政府针对罕用药的研发到上市多个阶段实施包括补贴、税惠、授权等在内的多种方式鼓励罕用药的研发和生产,提高罕用药的供给量,以满足罕见病患者的需求。
在研发阶段,美国政府通过专项拨款令FDA和NIH实施各种资金扶持计划,资助生物制药厂商及科研机构研发罕用药。近年来,美国政府每年提供的专项资金均不少于2000万美元。[7]图 2显示的是ODA实施以来FDA下属的罕用药开发办公室(Office of Orphan Products Development,OOPD)扶持的罕用药研发项目的数量变化情况。
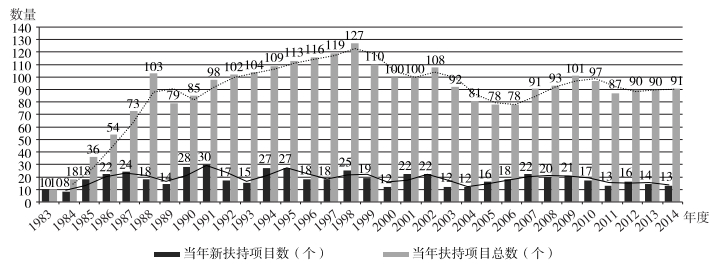
| 资料来源:Orphan Products GrantProgram[EB/OL]. http://www.accessdata.fda.gov/scripts/opdlisting/oopdgrants/ 图 2 OOPD1983—2014年扶持和累计扶持的罕用药研发项目的数量 |
当一种罕用药完成研发,即进入评审阶段。尽管负责药物审查的美国药物评价和研究中心(The Center for Drug Evaluation and Research,CDER)和美国生物制品评价和研究中心(the Center for Biologics Evaluation and Research,CBER)所建立的优先评审(priority review)、加速审批(accelerated approval)和快速通道(fast track programs)三种快速审批机制并不是完全专门为罕用药而设置,但是使用这三种机制的申请者绝大多数都是罕用药项目,这无疑为其尽快上市销售提供了便捷渠道。图 3 显示了2009年12月—2014年6月间CDER和CBER在70或75天目标评审时长下,每个月的评审完成比例。虽然每月因罕用药申请数量不同而完成评审的数量不一,但是,平均完成比例高达88.34%,充分表明FDA为罕用药评审提供了一条畅通的“快速通道”。
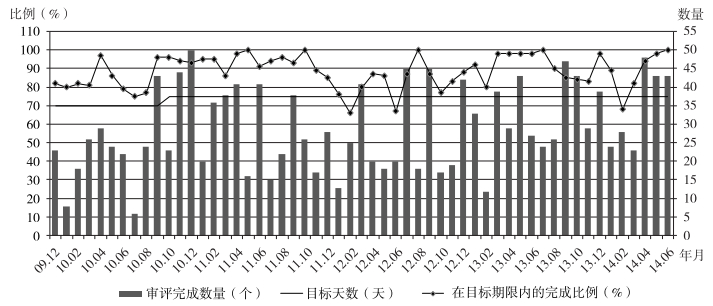
| 资料来源:Percentage of orphan drug designation reviews completed in 90 days or less [EB/OL].http://www.accessdata.fda.gov/FDATrack/track?program=osmp&id=OSMP-OOPD-Percentage-orphan-drug-designation-reviewed-completed-in-90-days-or-less&fy=all. 图 3 2009—2014年美国罕用药评审于目标时长内的完成数量及完成比例 |
此后,罕用药进入临床试验阶段。在这一阶段,研发者可申请临床试验50%的税收减免,并且有效期能够向前延伸3年,向后延伸15年,剩下的50%税收同样可以有一定程度的减免,最高免税比例可达70%左右。
另外,根据美国《处方药使用者费用法案》(Prescription Drug User Fee Act,PDUFA),被认定的罕用药物的处方申请费用将自动予以减免;获批上市的罕用药,其生产及确认费用也将予以一定程度的减免。从美国政府公布的财务报告来看,这三项费用的减免力度逐年增加。2004—2013年,处方申请费用累计减免约3.5亿美元。药物生产及确认费用的减免自2008财政年度开始实行,至2013年已分别减免1 400多万和3 300多万美元(表 2)。
| 表 2 2004—2013年罕用药的费用减免情况 |
完成评审认定且通过临床安全性试验以后,罕用药就可正式上市。这一阶段的激励措施除继续刺激生产者持续供应罕用药以外,还通过专业药房(Specialty Pharmacy)形式提高患者对药品的可及性。
为进一步刺激供应,ODA出台时就明确为已上市的罕用药提供7年市场独占权和永久价格自由量定权。尽管7年市场独占权并不是当今实施了罕用药市场激励的国家中最长的(欧盟、日本及中国台湾地区皆为10年),而且有一定的限制条件[8],但美国健康和人类服务部的报告指出,市场独占权仍然是ODA中激励作用最大的一项措施。
在药品可及性方面,美国采取专业药房的销售模式,方便患者及时购买所需的罕用药物。专业药房定位于销售各类专业药品,虽然美国尚未对专业药品有相关定义,但罕用药因其药物的针对性、特殊性往往成为专业药房的主要销售产品。[9]专业药房起源于20世纪70年代的美国药物冷链配送途径,随后在Walgreens、CVS等大型连锁药店建立,目前美国已发展出CVSCaremarkcvs、Medco、Express Scripts等多个专业药房公司。从专业药房销售模式衍生出的还有专业药房计划(Specialty Pharmacy Programs),它们是保险公司为解决药品和生物制剂的费用高、管理难和补偿问题而推出的保险计划。美国专业药房的针对性销售取得了巨大成就,根据IMS Health统计,2008年9月—2009年9月,全球最畅销的15种专业药房药品年销售额均达20亿美元以上。[10]这些专业药房一方面由于专业性而具有规模效益,另一方面简化了包括罕用药在内的专业药物的销售程序,满足对专业药物有刚性需求的患者。
通过以上介绍,可以美国罕用药市场的激励机制有以下几个特点:
一是对于罕见疾病和罕用药界定清晰,激励目标和激励对象十分明确,从而易于“对症研药”。美国是世界上第一个对于罕见疾病进行精确定义的国家,按ODA关于罕见疾病的认定标准,美国认定的罕见疾病有近7000种,为全球最多。也只有用于治疗这些被认定疾病的药物方能被认定为罕用药,然后才能享有一系列优惠政策。当然,随着美国人口数量的增加,罕见疾病也面临着是否需要重新定义的争论。
二是激励措施涉及罕用药的研发、认定、临床试验直至上市等各个环节,自成体系,联动共进,是目前全球同类机制中涉及领域最为全面,布局最为精细,联动效应最为突出的机制设计。
三是通过一系列的立法工作,不断规范和完善罕用药市场激励机制,使其具有权威性、公平性、时效性和可操作性,为激励机制的实施提供了法律保障。
四是设立专门的管理机构负责激励机制的实施,分工协作。如上文提到的ORD负责一些项目资金的资助工作,同时负责确认罕见疾病;OOPD则是对符合规定的罕用药研发和上市项目进行资助,同时承担罕用药优惠政策的各类咨询及政策效果的评估工作。FDA下设的CDER和CBER则负责药物审查工作。整个激励机制的政府实施部门分工明确,运转高效。
罕用药市场是一个严重失灵的市场,由于激励缺失,完全靠市场“看不见的手”来配置资源,只会导致厂商退出,供给不足。激励机制的设计和实施,有助于打破这一困境。我们从供需两个方面来评估美国罕用药市场激励机制的运行效果。
根据FDA的相关统计S数据,本文估算了《罕用药法案》颁布实施以来,美国每年参与罕用药研发及资格认定活动的企业数量(图 4)。从1983年仅有1家厂商参与资格申请活动,到2014年的389家,30多年间,罕用药的资格申请企业数量不断增加,罕用药资格认定申请的成功率大约为72%。
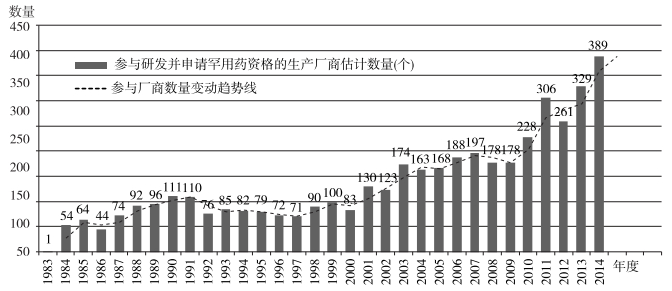
| 资料来源:FDA[EB/OL]. http://www.accessdata.fda.gov/scripts/opdlisting/oopd/index.cfm. U.S.Department of Health and Human Service Fiscal Year2015[EB/OL]. http://www.fda.gov/downloads/AboutFDA/ReportsManualsForms/Reports/BudgetReports/UCM388309.pdf 图 4 1983—2014年间每年参与罕用药研发及资格认定活动的企业数量 |
包括《罕用药法案》在内的一系列罕用药市场激励机制是美国整个生物制药产业发展的巨大动力之一[11],甚至在某种意义上而言,美国生物技术产业是1983年《罕用药法案》出台后的产物[12]。1994—2013年,美国生物制药产业的私人研发支出由70亿美元上升至233亿美元,增长了两倍多。
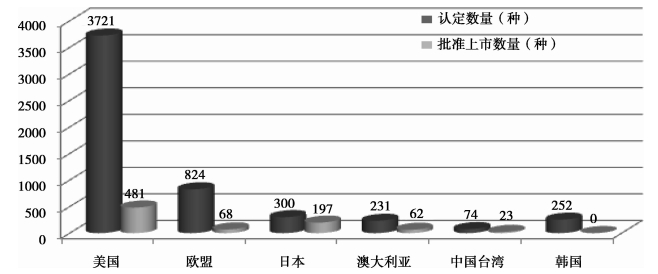
图 5反映了1983—2014年CDER和CBER评审认定的罕用药及批准上市的罕用药数量变化情况。截至2014年12月底,美国一共认定了3 721种罕用药,目前已经上市的有481种,大大超过了其他国家或者地区的数量(图 6)。

| 资料来源:Search Orphan Drug Designations and Approvals[EB/OL]. http://www.accessdata.fda.gov/scripts/opdlisting/oopd/index.cfm 图 5 1983—2014年美国罕用药认定及批准上市数量 |
|
注:美国统计数据截止2014年12月,日本为2012年3月,欧盟为2012年6月,澳大利亚为2011年,中国台湾地区为2012年1月,韩国为2011年底,其中韩国批准上市数量缺失。 资料来源:美国统计数据来自:U.S.Department of Health and Human Service Fiscal Year2015[EB/OL]. http://www.accessdata.fda.gov/scripts/opdlisting/oopd/index.cfm;欧盟、日本、澳大利亚及中国台湾数据来自:信枭雄, 管晓东, 陈敬, 等.国内外孤儿药注册制度比较研究[J].中国药学杂志,2013(48): 1323-1328. 韩国数据来自:褚淑贞, 李伟霞. 亚洲部分国家和地区针对罕用药开发的激励措施以及对我国的启示[J]. 中国医科大学学报,2014(45): 125-128. 图 6 部分国家(地区)罕用药认定及批准上市数量比较 |
截至2014年底,美国六大领先生物制药公司获得认定和上市的罕用药数量如表 3所示。尽管相对于3 000多种已认定的罕用药和480余种已经上市的罕用药而言,这六家企业的占比并不算很多,但是,美国同一家生物制药企业能拥有两个及以上的上市罕用药的情况并不多见。[13]在这六家公司中,有五家公司罕用药的销售收入占其当年总营收的50%以上,罕用药的生产成为这些公司主要的收入来源。[14]
| 表 3 美国六大领先生物制药公司获得认定及批准上市的罕用药数量 |
HHS发布的调查公报显示,绝大多数的罕见疾病患者团体都认为获得罕用药并不存在障碍[15],美国罕用药的可及性状况良好。当然,以目前的科研和医疗水平,使得全部罕见疾病都有药可医是不可能的,即使是激励机制尚且健全的美国,目前也只上市近500种罕用药物,而美国认定为罕见疾病的种类却超过了6 000种。显然,要满足所有罕见病的治疗需求还有很长的路要走。
尽管我国对罕见疾病至今都无任何官方定义①,但是我国罕见病患者总体数量大,分布广,病种多却是不争的事实。根据中华医学会的标准,我国罕见病患者的数量在1000万~2000万之间。[16, 17]但这一估计值仅覆盖了四大类共43种罕见疾病,而欧美等国的标准均在千种以上。如若按欧美标准估算,我国的罕见疾病人口规模将大大增加。
① 中华医学会遗传学分会曾于2010年将患病率小于五十万分之一或新生儿发病率小于万分之一的疾病定义为罕见病,但迄今并无任何官方标准问世。
面对庞大的罕见疾病患者群体,我国罕用药生产和进口情况却不容乐观。据统计,我国绝大多数罕用药物依赖进口,且数量仅为130种左右,不到美国的1/3。[18]同时国内医药企业往往因为罕用药规模利润低而不愿意进行研发;即使有少量研发成功,也会因药品统一定价,罕用药单位利润低而不愿意进行生产。[19]
因此,建立我国罕用药市场激励机制,促进罕用药的研发和上市,有效保障罕见病患者的健康权是当前亟待解决的问题。美国较为完备的罕用药市场激励机制对我国有以下几点启示:
相比美国完备的罕用药法律,我国的罕用药立法十分滞缓,目前未见关于罕见病和罕见药的官方界定以及相关立法的出台。因此,必须首先定义罕见疾病,建立相关病录,为罕用药立法和激励机制的建立奠定基础②。
② 2016年1月4日,国家卫生计生委办公厅发布《关于成立国家卫生计生委罕见病诊疗与保障专家委员会的通知》,指出应研究提出符合我国国情的罕见病定义和病种范围。但要达此目标尚需时日。
在审批方面,我国目前针对罕用药的特殊审批制度十分模糊③,因此制定更具操作性的罕用药政策法规有助于进一步激发相关企业和机构的自主研发和生产动力。在税费优惠方面,目前我国仅对药品中的避孕类药物实行增值税免征,对中药实行13%的增值税低税率征收,但是对罕用药临床试验及销售未实行任何优惠政策。为此,可对认定为罕用药的临床试验及销售费用进一步免征或减征增值税。另外,如前文所述,市场独占权的实施对于罕用药研发生产的激励作用最大,我国可制定相关政策,引导企业和机构参与罕用药的研发,亦可通过政策倾斜鼓励国内研究机构和企业抢仿、首仿国外专利权和独占权过期的罕用药物,实现自主供应。在当前我国罕用药研发生产水平下,加大进口国外成熟罕用药品亦是一个相对有效的手段。
③ 2009年国家食品药品监督管理局印发《新药注册特殊审批管理规定》,指出,“治疗艾滋病、恶性肿瘤、罕见病等疾病且具有明显临床治疗优势的新药,可适用特殊审批程序。”但何为“特殊审批程序”并无具体规定。
罕用药的研发生产成本往往比普通药物更高,因而需要更多的资金支持。美国在资金供给方面,形成了以政府政策为支点,以公共部门、民间组织、生物制药产业为三大基点的多种筹资渠道。筹资能力薄弱,资金短缺是制约我国罕用药研发与供给的重要原因。我国可以借鉴美国的筹资经验,多渠道筹措资金,一方面加大政府投入,以直接拨款或基金资助等方式支持罕用药的研发,另一方面鼓励企业和非营利组织通过资本市场和慈善捐赠募集资金,促进罕用药的研发与供给。
增强罕见病患者的支付能力,提高罕用药的有效需求也是对罕用药市场的一种激励。美国大部分的罕见病患者通过公共医疗保险计划和商业保险来负担治疗费用,其中以商业保险为主。[20]患者可以根据自身情况自主选择不同的保险计划,十分灵活。近年来我国也有少量省市(上海、青岛、福州、铜陵等)出台了地方性罕用药医保政策[21, 22],但我国目前尚未有专门针对罕见疾病及罕用药的整体医疗保障政策,患者的选择余地非常有限。有学者统计了国内广泛使用的35种罕用药在国家基本医疗保险目录以及8个省份新型农村合作医疗药品目录中的覆盖率,分别为54.3%和33.6%。[23]因此,我国针对罕见疾病的医疗保障水平较低,应当进一步提高罕用药保险报销目录覆盖率,建立罕见病及罕用药的专项报销计划,完善罕见病救助机制。同时,应积极促进商业保险机构开发针对罕见疾病的险种,进一步降低患者自付比例,减轻其经济负担。
罕用药市场的信息披露和意见反馈有助于激励机制作用的发挥和不断完善。美国在这方面的工作主要通过FDA这个平台来完成。当前,我国尚未有针对罕见疾病和罕用药的法规出台,市场参与力量薄弱,非营利组织虽然发展较快,但个体规模十分有限,运作亦不规范。因此,在建立罕用药市场激励机制的过程中,更应充分考虑政府、市场和社会之间的沟通与反馈。由政府部门牵头,搭建信息沟通的平台,在制定相关法律法规的同时,建立罕用药研发、申请、审批信息披露制度和罕用药政策效果追踪机制,联合市场和社会的力量,促进激励机制的进一步完善。
| [1] | The Orphan Drug Act[EB/OL].http://www.ecfr.gov/. |
| [2] | Seoane-Vazquez E, Rodriguez-Monguio R, Szeinbach S L, et al. Incentives for orphan drug research and development in the UnitedStates[J]. Orphanet Journal of RareDiseases, 2008, 3(3):33. |
| [3] | Jyoti T. Navigating through orphan medicinal product regulationsin EU and US-Similarities and differences[J]. Regulatory Toxicology and Pharmacology, 2015, 71(1):63-67. |
| [4] | Hurwicz L.The design of mechanisms for resource allocation[J]. American Economic Review, 1973, 63(63):1-30. |
| [5] | Haffner M E. Orphan Products:Origins,Progress, and Prospects[J]. Annual Review of Pharmacology, 1991, 31(31):603-620. |
| [6] | Drummond M F, Wilson D A, Panos K, et al. Assessing the economicchallenges posed by orphan drugs[J]. International Journal of Technology Assessment in Health Care, 2007, 23(1):36-42. |
| [7] | 龚时薇. 促进我国罕见病患者药品可及性的管理策略研究[D]. 武汉:华中科技大学, 2008. |
| [8] | 甘珏, 徐珊萍, 陈永法, 等. 多国(地区)罕用药制度比较分析[J]. 上海医药, 2013(34):27-31. |
| [9] | Blaser D A, Lewtas A J, Ousterhout M M. How To Define Specialty Pharmaceuticals:A Systematic Review[J]. The American Journal of Pharmacy Benefits, 2010, 2(6):371-380. |
| [10] | 许焱. 我国罕见病药品可及性评价指标体系的构建与影响因素分析[D]. 武汉:华中科技大学, 2012. |
| [11] | Wesley Yin. Market incentives and pharmaceutical innovation[J]. Journal of Health Economics, 2008, 27(4):1060-1077. |
| [12] | 李伟. 各国罕用药管理制度比较研究[J]. 上海食品药品监管情报研究, 2008(4):1-6. |
| [13] | Wellman-Labadie O, Zhou Y. The US Orphan Drug Act:Rare disease research stimulator or commercial opportunity?[J]. Health Policy, 2010, 95(2-3):216-228. |
| [14] | Lazonick W,?nerTulum. US biopharmaceutical finance and the sustainability of the biotech businessmodel[J]. Research Policy, 2011, 40(40):1170-1187. |
| [15] | The Orphan Drug Act Implementation and Impact[EB/OL]. http://oig.hhs.gov/oei/reports/oei-09-00-00380.pdf. |
| [16] | 马端, 李定国, 张学, 等. 中国罕见病防治的机遇与挑战[J]. 中国循证儿科杂志, 2011, 6(2):81-82. |
| [17] | 李定国. 关于罕见病的定义和发病率[J]. 临床检验杂志, 2013(3):186. |
| [18] | 丁锦希, 刘维婧, 李伟, 等. 我国罕用药可及性现状及其市场准入制度分析[J]. 中国药科大学学报, 2014, 45(1):111-117. |
| [19] | 张建国. 我国罕用药供应的管理[J]. 药物流行病学杂志, 2008, 17(5):342-343. |
| [20] | 刘伟静, 李丽华, 王世家,等. 国外罕见病医疗保险制度现状[J]. 现代商贸工业, 2015, 36(11):166-167. |
| [21] | 梁土坤, 尚珂. 青岛模式:罕见病医疗保障制度的实践与展望[J]. 社会保障研究, 2014(3):64-73. |
| [22] | 许燚, 王英晓, 龚时薇. 美国罕见病用药的专业药房销售模式研究[J]. 中国药事, 2011(12):1238-1242. |
| [23] | 胡娟娟, 龚时薇, 许焱, 等. 我国罕见病及罕用药基本医疗保险覆盖现况分析[J]. 中华医院管理杂志, 2013, 29(8):573-577. |
(编辑 赵晓娟)




