2. 华润赛科药业有限责任公司 北京 100124
2. China Resources Saike Pharmaceutical Co., Ltd, Beijing 100124, China
药品质量作为我国医药卫生体制改革的重要内容,一直以来是国家药品监管的重点。2001年,国务院印发的《医疗机构药品集中采购工作规范(试行)》(以下简称 308号文)里首次对招标药品提出“质量分层”概念,药品采购中的质量层次划分工作由此展开。在其后的集中采购改革文件(如《国务院办公厅关于建立和规范政府办基层医疗卫生机构基本药物采购机制指导意见的通知》(国办发〔2010〕56号)和《关于印发医疗机构药品集中采购工作规范的通知》(卫规财发〔2010〕64号))中均强调采用质量层次划分方法确保药品质量。[1]伴随药品集中采购制度的不断改革,质量层次评审标准在实践探索的基础上不断丰富,各省市已形成较为固定的模式。但层次划分标准不一、“地方保护主义”掺杂、评价指标难以真实体现质量等问题依旧突出,质量分层并未发挥预期效果。[2]
针对上述问题,国务院《关于完善公立医院药品集中采购工作的指导意见》(国办发〔2015〕7号)(以下简称7号文)提出“竞价分组”概念,突出强调药品质量应“分组”而非“分层”,表明传统意义上的“质量层次划分”已逐步演变为“竞价分组”。[3]随后,国家卫生计生委《关于落实完善公立医院药品集中采购工作指导意见的通知》(卫药政发〔2015〕70号)(以下简称70号文)明确指出,“集中采购要根据仿制药质量一致性评价技术要求,科学设定竞价分组”,对其具体操作提出要求。各省市以7号文和70号文为基础,陆续出台药品集中采购改革文件,其中大部分对竞价分组的设计方案做出明确规定;同时,部分省市已经开始进入竞价分组实践运作层面。
本文通过统计各省市最新出台的集中采购改革文件及竞价分组评价指标,从能够直接反应竞价分组制度建立与落实情况的层级设计(反映竞价分组竞争程度)、指标构建(反映药品质量凸显情况)、评审内容(反映层级与指标设计是否合理、科学)等方面分析2015年5月—2016年5月内各省市具体实践情况,发现现阶段我国竞价分组方案仍需改进的问题,探索我国“竞价分组”完善和优化的策略。
1 实施竞价分组的原因 1.1 我国药品质量评价体系现状我国的药品(尤其是仿制药)注册审评以《中华人民共和国药典》、部颁标准等作为标准,主要考察生产企业上报的综述资料、药学研究资料、药理毒理研究资料、临床试验资料等是否符合相关规定,对于真正涉及药品质量的核心要素(主要指生物等效性、体外溶出度、药品杂质检验等)缺乏实践层面的有效监管,上述因素叠加在一起造成了医药行业普遍存在的“仿标准、不仿产品”的堪忧现实。同时,同通用名药品多家企业生产的情况在我国较为普遍。截至2014年,国家食品药品监督管理总局(CFDA)共颁发约17.2万个药品批准文号,市场流通药品品种仅1.5万种[4],这种情况往往很难保证药品质量。如果不区分仿制药间质量差异,质量高的药品无价格优势,必然会降低企业质量提升动力,导致企业倾向生产低质量药品,即所谓的“劣币驱逐良币”,从而产生“柠檬市场”(The Market of Lemons)效应,不利于我国药品市场的良性发展。 因此,参考域外国家与地区(如英国、德国等)药品质量监控的政策实践,有关部门已尝试建立符合我国实际的药品质量监测体系(如“仿制药一致性评价”政策)。目前,各项政策措施正处于探索阶段,并不能发挥应有的政策效果。因此,我国提出“竞价分组”作为上述问题在此过渡时期的解决方法。
1.2 竞价分组的提出本文将竞价分组定义为根据质量属性、注册状态、生产企业资质等相关指标将药品划分为不同竞价组,同组药品展开价格竞争,实现“优质优价”目标的一种药品质量评价方法。竞价分组作为新双信封制下最主要的质量评价方法,通过区分药品质量层次,确保有力竞争,旨在解决我国一致性评价系统缺失、药品质量层次不齐等问题。
1.3 竞价分组的具体作用设立“竞价分组”的初衷就是区分质量层次,确保医疗机构使用药品的“优质优价”,这也是药品集中采购制度改革中需要重点突破的问题。其主要作用可归纳为三点:
(1) 区分质量层级。从各省(市)或地区的竞价分组层级设置来看,主要将专利药品、原研药品、获奖药品等置于较高组别,而将其他药品按照GMP、企业资质等指标置于较低组别。这样的做法,可以在一定程度上将质量层次区分开来,有利于体现集中采购“质量优先”的原则。
(2) 经济技术标评审的主要依据。以浙江省采购方案为例,浙江省经济技术标评审项目中,与产品质量相关的两项主要指标(产品质量评价和临床疗效评价)分值为59分,占评价体系的59%;而江苏省相关指标占比为40%,虽略低于浙江省,但对经济技术标评审的影响依旧很大。
(3) 鼓励药品生产研发创新。各省市竞价分组评价体系中,专利药品、原研药品、实力或资质较强企业的药品等均能处于较高的组别,对于企业进入商务标议价,并最终中标都有较大帮助。
1.4 我国实施竞价分组的必然性目前,我国仿制药一致性评价工作方案虽已确定,但参比制剂选择,实验方案设计等方面仍需进一步完善,“仿标准、不仿质量”的现象依旧存在[5],故原研药与仿制药之间、仿制药与仿制药之间,在药品质量、尤其是临床疗效方面存在较大差异,导致现阶段我国药品质量参差不齐,故在药品采购制度设计中区别质量层次就显得十分必要。竞价分组可以很好的区分质量层次,且有利于双信封制度更好的发挥药品筛选和价格控制作用。结合我国药品集中采购现状,现阶段应当仍以竞价分组作为划分质量层次的主要方法。
2 我国现阶段竞价分组的实施情况 2.1 数据来源及研究方法本文参考2015年5月—2016年5月全国各省(市)最新出台的药品集中采购文件,对各省(市)竞价分组的情况进行统计。以此为据,选择医疗卫生体制改革成效较为显著的江苏、广州、北京、浙江4个重要试点省(市)作为重点调研对象,同时组织参与一系列集中采购政策相关会议,通过专家访谈、研讨会、座谈会等形式完善全国竞价分组情况(如层级设置、指标体系构建等)的统计和研究(表 1)。
| 表 1 数据资料调研采集信息情况 |
竞价分组层级就是根据药品质量情况所归纳的类别,是竞价分组的主体框架。在具体层级设置完成后,将相应的指标纳入相应层次,才能发挥竞价分组区分质量层次的作用。因此,层级设置就显得格外重要。各省市参照国家要求,均出台相应的文件设置层级,本文统计了目前各省市采购文件中对竞价分组层级设置的相关规定(表 2)。
| 表 2 27省招标采购药品竞价组划分情况(截至2016年5月) |
根据统计结果,可以看出:(1)我国现阶段质量层次划分多为2、3、4层,表明在[2, 4]这个区间内,层级划分的可操作性较强;(2)划分三个层次的省份最多,占全国近2/3,这说明较其他两种类型,划分三个层次优势更加明显。 需要特别说明的是:(1)江西和河南虽在文件中提及划分的质量层次数,但并没有对各层内容或具体内容进行描述;(2)对质量层次划分做出具体规定的24个省市中,17个省市是在经济技术标评审前划分质量层次的,7省(四川、青海、湖北、内蒙古、天津、福建、陕西)是在经济技术标评审后进入商务标评审时划分质量层次的;(3)福建和陕西划分质量层次以具体药品经济技术标得分为依据,与其他省份不同,其他22省主要依据药品专利情况、药品注册分类情况、企业资质、获奖情况等进行质量层次划分。
2.3 竞价分组指标构建情况指标体系是竞价分组发挥区分质量层次作用最重要的依据,也是经济技术标分值设定的基础。因此,本文根据各省市最新的药品采购文件,将明确规定竞价分组项目的16个省市的质量层次划分指标进行统计,通过统计各项指标在各省市竞价分组出现频次、所处组别等(如①表示处于第一质量层次),反映现阶段我国药品竞价分组指标构建情况。具体如表 3—表 5。
| 表 3 省竞价分组指标层次划分统计表(1) |
| 表 4 省竞价分组指标层次划分统计表(2) |
| 表 5 省竞价分组指标层次划分统计表(3) |
根据表 3、表 4及表 5的统计情况,现阶段我国竞价分组指标体系构建主要有三个特点:(1)在18个纳入统计的评价指标中,指标性质主要可概括为药品注册审评情况(该类指标占比66.67%)①、药品认证情况(该类指标占比11.11%)②、企业情况(该类指标占比22.22%)③三个方面;(2)现阶段,药品注册审评情况被认为与药品质量关系最密切,故各省市将与其相关的指标置于较高组别,如“不在保护期内的专利药品”、“药品注册分类第一类新药”等指标,85%以上的省份均将其置于第一竞价组,体现出该类指标在竞价分组中的重要性;(3)企业情况指标统计的结果显示,该类指标在各省市竞价分组体系中占比不高,相反,与药品直接相关的指标被普遍应用于评价体系中;(4)近期关注度较高的药品质量政策在各省市竞价分组中占比变化较大,其中,已有13个省份将仿制药一致性评价指标纳入竞价分组,而纳入首仿药的省份也从最初的4个增长至10个。
① 药品注册审评情况指标主要包括:保护期内的专利药品、不在保护期内的专利药品、国家中药保密处方、药品注册分类第一类新药、中药保护品种、进口药品非专利药、药品注册分类第二类新药、通过质量一致性评价的仿制药品、首次仿制药品、达到国际水平的仿制药
② 药品获奖情况指标主要包括:中成药所用中药材通过GAP认证的药品、普通GMP药品
③ 企业情况指标主要包括:创新企业药品、质量标杆企业、《医药工业企业主营业务收入(排序)》排名前N为企业生产的药品、省网上集中采购(或销售)金额排名前N为企业生产的药品
3 竞价分组存在的问题 3.1 竞价分组层次划分不统一层级设置不统一系我国竞价分组现存最主要的问题[7]。在70号文发布之前,我国药品竞价分组情况非常复杂,大多数省份对采购药品直接进行竞价组划分,竞价组数量2组至8组不等[8],比较特殊的,则不对其进行直接划分,转而将药品划分为不同评审组进行审评;70号文发布后,各省市重新制定竞价分组方案,现已形成以2~4组为主的竞价组划分模式(见表 2),情况虽有所好转,但竞价分组层次划分仍不统一。不同的层级设置将引起一系列问题:一方面会导致药品质量评价结果差异较大,难以同时发挥“增强竞争、区分质量”的作用,如较少竞价组的情况可加强标后市场环节的竞争力度,但质量区分作用有限,而较设置多层次恰恰相反;另一方面,各省市划分情况不一,加大了集中采购的工作量和操作难度,以“新药注册分类第一类”指标为例,大部分省市将其设置为第一竞价组,而海南和江西却设置为第二竞价组,不同的竞价分组情况必然对企业的评标、竞标以及采购部门监管产生较大影响。
3.2 涵盖类别不全面现阶段竞价分组主要包含专利药、原研药、中成药、仿制药四大类,但大多数省份忽略了近年来广受国内外热捧的首仿药品。我国竞价分组中首仿药品受关注度不高,严重挫伤了我国药品生产企业的研发,也不利于竞价分组激励创新的作用。
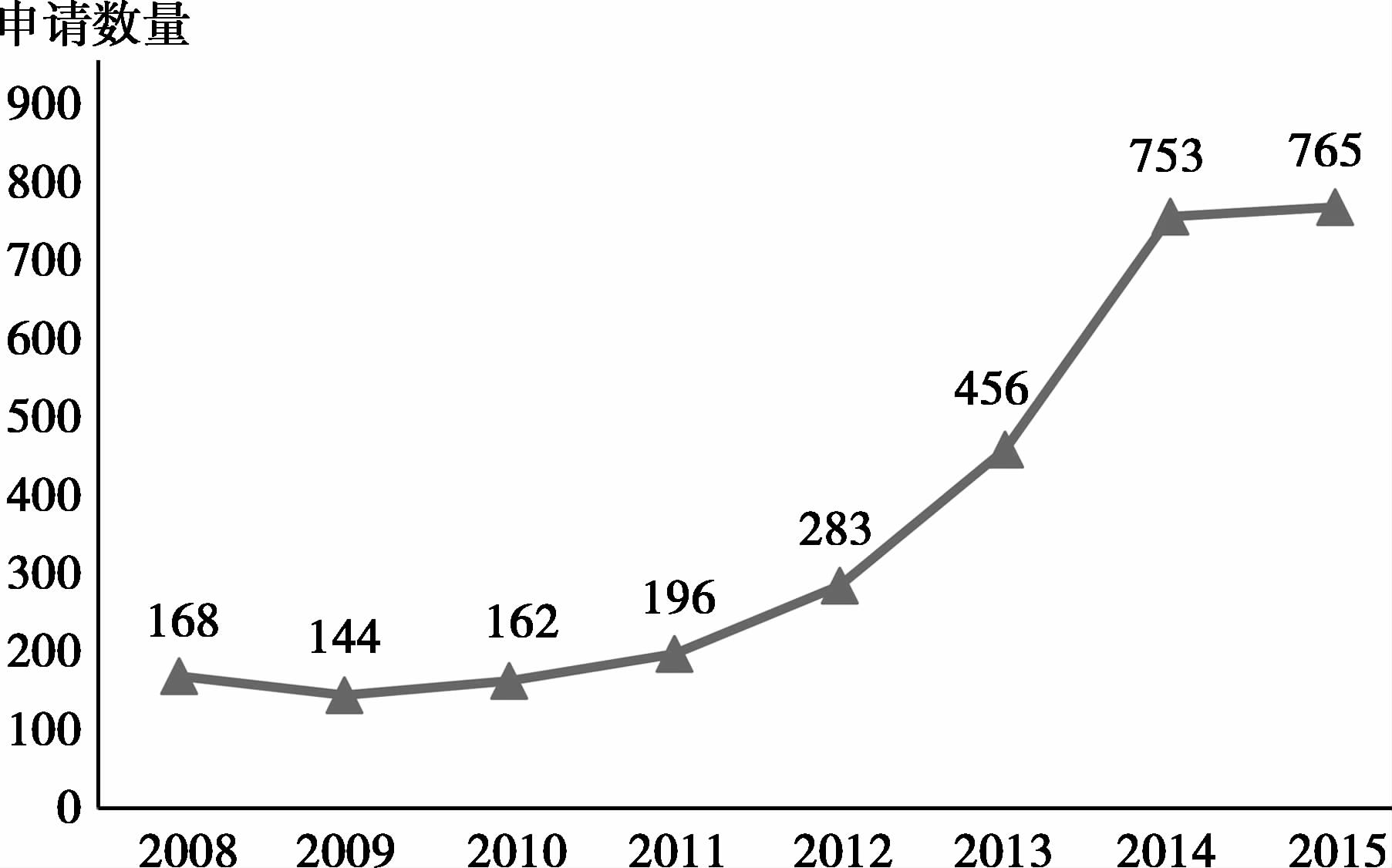
在我国,三类仿制药①在业内一般被称之为“首仿药”②,由于其在中国市场处于空白,能够优先抢占市场份额③,因此广受中国企业的追捧,其申请数量也在逐年大幅度增长,从2008年的168增长到2015年的765(图 1)。
|
数据来源:insight数据库 图 1 2008—2015年第三类仿制药临床申请品种数量趋势 |
① 根据国家新的化学药品注册分类,原注册分类中的3.1类新药现统称为三类仿制药
② 目前我国尚无官方文件对首仿药进行界定,各省市对于首仿药的认定也存在差异,导致首仿药并未纳入所有省市竞价分组体系当中
③ 2016年7月21日国家药品审评中心出台《“首仿”品种实行优先审评评定的基本原则》,对22个“首仿”品种提供优先审评审批的政策优惠
从2009年开始,部分省市药品招标采购方案中首仿药的定义和质量层次划分的依据被明确写入标书,表明各省市已经开始接纳并逐步将首仿药纳入集中招标采购体系。根据各省市最新的药品招标采购方案,目前已有12个省市将首仿药品明确纳入竞价分组体系,较2015年情况大为好转(仅有江苏、内蒙古、辽宁三个省市),充分说明首仿药品在竞价分组设置中的重要性。但同时仍有超过50%的省市没有将首仿药纳入竞价分组方案中,说明其在我国受重视程度不高,证明现阶段竞价分组涵盖范围并不全面(表 6)。
| 表 6 竞价分组明确体现首仿药的省市情况 |
评价体系主要通过构建指标对药品进行各方面的考察,最终在投标企业中选择药品质量好、临床疗效高、价格能够负担的药品作为中标药品参加省级药品集中采购,是药品集中采购制度的核心内容。
目前,我国竞价分组指标体系主要包括药品注册审评情况、药品获奖情况和企业资质三大类(表 3—表 5)。其中,与药品关系最为密切的药品注册审评情况难以客观体现药品质量①;而获奖情况和企业资质与药品质量关联性更小。表明我国现阶段竞价分组外围指标过多,难以准确体现同通用名项下药品间的质量差异,与“优质优价”的原则相背离。[8]
① 竞价分组中涉及药品注册评审的内容主要包括药品专利情况、是否通过一致性评价、是否符合国际标准三方面。其中,专利情况难以充分证明药品质量;我国一致性评价工作尚未开展,该条内容尚不能发挥其应有作用;将符合国际标准纳入竞价分组的省份目前不到50%。因此,现阶段药品审评无法客观体现药品质量
② 《国务院关于机构设置的通知》(国发[2013]14号)主要职责第6、7、16条;其他事项第3条
3.3.2 评价主体职能与药品质量关联度不高现阶段,我国竞价分组指标体系构建工作主要由由卫生计生委药政管理部门承担。但其主要职能范围为公立医院改革、基本药物制度运行及管理、药品价格控制,不良反应监测等②,并未涉及药品质量评价相关内容;与此同时,主管药品的药物政策与基本药物制度司和各省药政处主要负责竞价分组指标体系构建,而这些部门并不具有药品质量评价的相关职能。由此,评价主体与药品质量评价关联度较低,成为外围评价指标过多,药品质量难以体现的主要原因。
4 结论与建议 4.1 设置合理的质量层级设置合理的质量层次的意义在于体现竞价分组“质量优先”的本质,而统一我国质量层次水平就成为亟待解决的问题。建议在保证质量层次区分的前提下,设置较少的层级,这样既能够保证质量,又能够促使各层级之间形成一定的竞争,有利于降低药品价格,就各省具体情况而言,将层级设置为三层较为合理,且各省(市)层级统一较为容易。
4.2 引入国际质量评价指标现阶段,我国药品注册审评中“仿标准,不仿质量”的情况较为普遍,药品质量差异难以在审批环节得到准确体现;同时,另一个用来体现药品质量情况的方法——竞价分组,由于其多选用与质量关联性不大的指标(如企业规模、药品注册情况等),导致药品质量在集中采购环节也难以凸显。 由于国际认证体系在“产品注册”、“GMP认证”两个方面都提出了更高的要求,其成品药在“质量稳定性”(批间差异)、“安全性”(有关物质)、“有效性”(生物利用度)等方面优势明显;且国际认证体系与国内的“仿制药一致性评价”都是通过使用科学规范的手段方法,对药品质量进行评估,对药品安全性和有效性的监管更加有效。建议应当在竞价分组体系中引入能够反映药品质量情况的指标改善上述情况(表 7)。
| 表 7 国际认证体系与中国药品审批标准主要指标对比情况[9] |
目前,浙江、天津、湖南等10个省(市)最近一轮的药品集中招标采购当中已经率先将“是否通过国际药品质量认证体系”作为竞价分组指标,并置于较高组别当中,这将为该指标在竞价分组中的推广提供实践基础。
4.3 构建科学的评价体系 4.3.1 设置合理的评价指标参照70号文要求及国外药品采购发展趋势,本文建议构建直接指标与间接指标相结合的质量评价体系。其中,直接指标主要负责考察药品质量问题,尽可能消除同品种质量分层的现象,主要包括:企业资质认证(如GMP、COS认证)、一致性评价(主要是指体外溶出度检测,工艺、设备验证,药品杂质检测等)、生物等效性评价等;而间接指标在确保质量的前提下,综合考虑企业的生产供给能力、信用情况,为采购方选择药品提供参考,如企业规模、药品获奖情况、是否为首仿药品等(表 7)。
但是,竞价分组仅是针对我国目前现状的权宜之计,从未来药品采购发展的趋势来看,竞价分组的形式将逐渐被一致性评价为主的评价体系代替。在该体系下,一致性评价确保药品质量,即原研药与仿制药不存在质量差异,药品采购制度将回归其服务职能,通过发挥带量优势,来换取价格上的优惠,这将是我国药品集中采购未来发展的主要方向。
4.3.2 评价主体应与药品质量评价密切相关伴随着评价体系的变化,评价主体也要进行相应调整,在遵循“各尽其能”的原则下评价主体应当由卫生计生委调整为负责药品质量的相关部门。具体做法是,在保持现阶段卫生计生委和各省市药政主管部门为评价主体的基础上,逐步过渡到卫生计生委与CFDA联合进行药品质量评价,待我国一致性评价方案基本完善,药品质量以直接指标评价为主后,评价主体将调整为与药品质量关系最为密切的部门,如负责仿制药上市前评价的药品审评中心(CDE)及负责仿制药上市后评价的一致性评价办公室等。同时,评价主体需协同多部门参与,确保药品质量评价的价值在药品集中采购中真正得以体现。
| [1] | 汤少梁, 张玉蓉. 药品招标采购中质量分层机制的评价研究[J]. 中国执业药师 , 2014 (8) : 36–40. |
| [2] | 尹明芳, 徐爱军, 梁红云, 等. 医疗机构药品集中采购质量层次划分研究[J]. 药学与临床研究 , 2014 (1) : 5–14. |
| [3] | 陈昊. 质量层次划分的历史演进[N]. 医药经济报, 2015-10-12(F02). |
| [4] | 国家食品药品监督管理中心. 企业查询[DB/OL].[2016-09-06]. http://app1.sfda.gov.cn/datasearch/face3/dir.html |
| [5] | 冯毅, 朱波. 关于我国仿制药质量一致性评价的研究及建议[J]. 中国新药杂志 , 2016 (1) : 19–26. |
| [6] | 2015-2016年我国各省市药品集中采购方案[S]. |
| [7] | 朱琳, 孙利华, 刘国恩, 等. 关于药品招标中质量分层的思考[J]. 中国药房 , 2010 (40) : 3774–3777. |
| [8] | 周明月, 宋民宪, 俞铖航. 我国药品招标管理中的药品质量分层问题研究[J]. 药品评价 , 2015 (6) : 20–23. |
| [9] | 毕军, 陈佩毅, 沈传勇, 等. 通过国际药品GMP认证的药品生产企业调研情况分析[J]. 中国药事 , 2014 (9) : 954–958. |
(编辑 薛 云)




