2015年5月,国家发展改革委在《关于印发推进药品价格改革的意见》(发改价格〔2015〕904号) 中提出:取消绝大部分药品政府定价,药品实际交易价格主要由市场竞争形成。药价放开后,药品价格监测成为建立以市场为主导的药品价格形成机制的关键问题。目前, 我国主要通过各省依据《药品价格监测办法》(计价格〔2000〕2185号) 建立的药品价格监测报告制度来监测药品价格。各地的监测方法多停滞于定点采集数据、分析价格走势方面[1, 2], 各省判定价格异常波动的标准也不一致,难以实现国内药品价格监测效果的横向对比,也不便与国际药品价格水平进行比较。例如《广东省药品及药品原材料价格监测专项报告制度》(粤价〔2013〕300号) 指出半年内价格上下浮动30%以上的药品须作专项分析并上报,《江西省价格鉴定监测管理局关于加强对非处方药品市场价格监测的通知》》(赣价鉴监字〔2014〕20号) 则重点监测价格上下浮动超过10%的品种。
1 资料与方法本研究以“(medicine price or pharmaceutical price or drug price [Title/Abstract]) and (monitor or supervise [Title/Abstract])”为检索式,在pubmed数据库中共检索到文献25篇,以“药品价格、监测”或“药品价格、预警”或“药品价格、预测”为主题词,在中国知网数据库中共检索到相关文献108篇。本研究未设置文献发表年限限制,最后的更新日期是2016年10月24日。研读文献发现境外已经有较为成熟的药品价格监测模式,主要包括基于药品价格指数、基于价差法、基于医保支付价、基于市场份额、基于国际参考价格五种监测模式。相比于其他监测模式,以国际参考价格为参比指标,可为国内外药品价格比较搭建桥梁,有利于我国的药品价格与国际水平接轨。此外,《关于印发推进药品价格改革的意见》(发改价格〔2015〕904号) 中指出:“对于与国际价格存在较大差异的药品,要及时研究分析,必要时开展成本价格专项调查[3]”。可见,将国际参考价格引入药品价格监测既符合我国国情,又符合医改新政。因此,本文主要研究基于国际参考价格的监测模式。
研读文献发现加拿大是采用国际参考价格进行药价监测的代表性国家,本文以“加拿大、药品价格”为主题词,且未设置发表年限限制,在中国知网数据库中共检索相关文献35篇。除《境外药品价格监测模式及对我国的启示》中梳理境外较成熟的药品价格监测模式并简单介绍加拿大药品价格监测方法外,其余34篇文献主要介绍加拿大药品价格管理体制,并未详细分析其药价监测模式。基于此,本文对加拿大基于国际价格的监测模式进行深入剖析,以期为我国应用国际参考价格进行药价监测提供参考。
2 基于国际参考价格的药品价格监测模式药品国际参考价格是指根据药品在一个或者多个国家的价格建立一个基准或者参照, 以期帮助应用药品国际参考价格的国家进行定价或价格调控。[5]在价格管理的过程中,各国通常将本国的药品价格与国际价格水平进行比较,据此来衡量本国的药品价格水平,从而为价格调整提供依据。
加拿大对引入期的新药价格和已上市药品的价格采用不同的方法进行监测。对于引入期的新药,加拿大按照创新程度将其分为四类,并且主要采用四种价格测试方法监测其药品价格,即国际中位价格比较测试、最高国际价格比较测试、国内治疗类别比较测试、国际治疗类别比较测试;对于已上市药品,加拿大主要通过计算国际价格比率,进而与参照国的相应药品价格进行双边比较和多边比较。
2.1 引入期新药的价格监测 2.1.1 价格信息的获取加拿大的药品价格信息由专利药价格评审委员会 (PMPRB) 提供。PMPRB主要通过两种渠道收集药品价格信息:国内药品价格信息主要通过各省的医疗保险系统收集,专利药生产企业每年两次报告药品单价与销量;国际药品价格信息主要来源于PMPRB与法国、德国、意大利、瑞典、瑞士、英国、美国的卫生部门和国际药品市场调查机构建立了合作关系,定期获得上述七国的药品价格信息。[6]
2.1.2 新专利药引入价格的确定加拿大联邦政府通过计算各地区三个不同消费群体 (医院、药房、批发商) 的全国平均交易价格和特定市场的平均交易价格来确定新专利药的引入价格。其中,全国平均交易价格由全部市场的总净收入除以所有市场中单元 (医院、药房、批发商) 数目得出。特定市场的平均交易价格由该市场的总净收入除以该市场中的单元数目得出。制定出专利药的引入价格之后,PMPRB依据《过高价格指南》采用比较测试的方法监测引入期 (从首次销售到6个月监测期结束) 的价格是否过高。[6, 7]
《过高价格指南》由PMPRB依据《专利法》而制定。其中规定了4条专利药的评审指导原则:①大多数新专利药的价格不得超过治疗同一疾病的已有药品的最高价格;②取得突破性创新或者疗效有大幅度提高的专利药,其价格不得超过七国同种专利药的中位价;③已有专利药每年的价格增幅不得超过CPI的增幅;④加拿大的专利药价格永远不得超过7个参照国同种专利药的最高价格。[5, 10]
2.1.3 价格比较测试方法(1) 国际中位价格比较测试 (Median International Price Comparison Test, MIPC),用于确定引入期新药的最大平均潜在价格和非过高平均价格。首先,最大平均潜在价格是7个参考国家 (法国、德国、意大利、瑞典、瑞士、英国、美国) 同专利同剂型剂量药品出厂价格的中位值。当参考国家少于5个时,需确定一个临时中位值,3年之后或者参照国超过5个时,则需重新确定国际中位价格。其次,非过高平均价格为重新确定的国际中位价和由居民消费指数 (CPI) 调整方法学计算出的非过高平均价格之中的较低者。[8]当确定了非过高平均价格以后,专利人将会降低全国和市场平均交易价格,使其在监测期内不得高于非过高平均价格。[7, 9]
(2) 最高国际价格比较测试 (Highest International Price Comparison Test, HIPC)。无论在引入期还是未来几年,专利药在全国、各省药房、医院的平均交易价格均不得超过参照国同专利同剂型剂量药品的最高价格。否则,则认为该药品价格过高。[7, 9]
(3) 国内治疗类别比较测试 (Therapeutic Class Comparison Text, TCC)。该方法将新专利药在全国或特定市场的平均交易价格与参比药品的价格进行比较。PMPRB依据世界卫生组织的ATC分类系统初步筛选参比药品,并通过考虑可比剂量方案 (可比剂量不得高于包含相关临床参数的产品专论中推荐的最高剂量) 确定最终的参比药品。PMPRB将通过多个公共资源获取参比药品的价格,并从中选取最低的公共价格用于价格比较。如果价格不可得,PMPRB将探索更多的来源,直到获得可用的公共价格。PMPRB根据每疗程的价格或者每天的价格进行价格比较,通常每疗程的价格适用于急性适应症,而每天的价格 (基于维持剂量) 适用于慢性适应症。此外,PMPRB在TCC测试中也会依据《过高价格指南》剔除以过高价格出售的药品。[7]
(4) 国际治疗类别比较测试 (International Therapeutic Class Comparison Test, ITCC) 用于比较加拿大待评审专利药品的全国平均交易价格和参考国家可比药品的价格。该方法不是主要的价格测试方式,但可在调查明显过高的药品价格时提供一些参考信息。该测试有直接法和比值法两种方法。直接法是计算参照国所有可比药品价格的中位值,并将其与全国平均交易价格比较。比值法是计算所审查的药品价格与各参照国可比药品的价格比值,比值中位数将被用于确定关键比较价格 (该价格被用来确定国内最大平均潜在价格),并且比值中位数需与全国平均交易价格进行比较。[7, 9]
2.1.4 新药的分类及相应的价格监测方法加拿大价格评审办法的标准取决于新药的创新程度。新药根据治疗水平的提高程度可分为四类:突破性提高、大幅度提高、中等程度提高、小幅度甚至没有提高,这四种新药的全国或者特定市场的平均交易价格均不得超过被测试药品的最大平均潜在价格。最大平均潜在价格的具体确定方法如表 1。
| 表 1 四种新药价格监测中最大平均潜在价格的确定方法 |
已上市药品价格信息的获取同引进期新药,包括所有的专利药和非专利药。其中专利药的参考国家同引进期新药,非专利药的参考国家涉及11个,其中7个是用于专利药价格评估的参考国家,另外4个国家 (荷兰、西班牙、澳大利亚、新西兰) 在仿制药市场规模方面与加拿大具有可比性。已上市药品价格监测的方法是计算国际价格比值,从而进行多边比较和双边比较。
2.2.1 国际价格比值国际价格比值是指加拿大与参照国同通用名药品的价格之比。将加拿大的药品价格水平设为1,国际价格与加拿大的价格比值>1,意味着较高的国外价格,反之,则国外价格较低。例如,价格比值为0.81,表示人们在x国购买相同的药品,其支出是在加拿大购买时的81%。[10]
无论是多边比较还是双边比较,在计算每一专利药或者非专利药的国际价格比率后,都要综合所有的专利药或非专利药计算均值。PMPRB报导的均值主要有几何平均值 (Geometric Mean, RG) 和算数平均值 (Arithmetic Mean, RA),且RG永远不会超过RA,两者之间的差值将随着单个药品价格比值的变化而变化,只有当所有药品价格具有相同价值时,RG和RA才可能相等。几何平均值和算数平均值的计算公式分别如下[11, 12]:
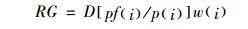
|
其中,D意味着加拿大所有专利药或非专利药的乘积,p (i)代表加拿大药品i的价格,pf (i)代表该药的国外药品的价格 (转化为加元),w (i)该药在加拿大药品总销售额中所占的比例。
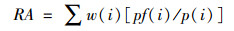
|
其中, ∑意味着加拿大所有专利药或非专利药的总和,其他符号意义同上。
2.2.2 多边比较首先需要获得参考国家的某种专利药或者非专利药价格的中位值,然后计算该中位值与加拿大相应药品的价格之比,最后综合所有的专利药或非专利药国际价格比值计算均值。另外比较指标还有国外价格的平均值、最大值、最小值。PMPRB一般采用36个月的市场汇率的移动平均值来转换货币单位。
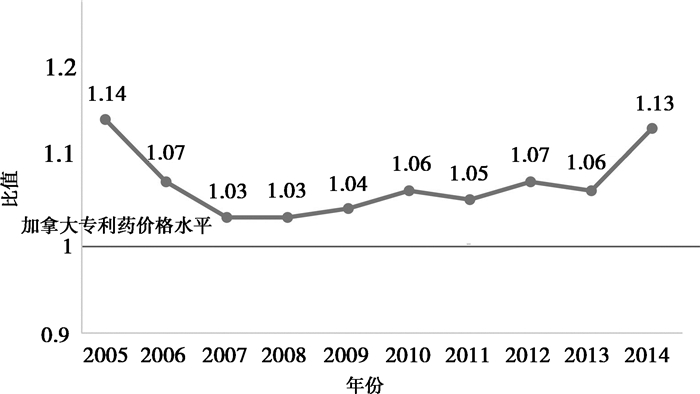
国际中位价 (MIP) 与加拿大专利药品价格的比较结果如图 1。2005-2014年,国际中位价格与加拿大专利药价格之比经历了逐渐下降然后又缓慢上升的过程。2005比值为1.14, 2008年下降为1.03,2014年又上升至1.13。十年间专利药的国际价格比率虽出现较大程度的波动,但仍位于基准线 (加拿大药品价格=1) 之上,可见加拿大专利药品价格已低于国际价格水平。
|
数据来源:2005年-2014年PMPRB的年度报告 图 1 专利药品国际中位价与加拿大药品价格的比值 (RA)-多边比较 (2005-2014) |
双边比较是指逐一计算参照国药品价格与加拿大同一药品的价格之比 (加拿大=1),据此监测加拿大的药品价格。若比值变化异常,则分析其影响因素,如加拿大药品价格变化、国外药品价格变化、市场汇率等,从而进行政府干预或者市场调节。
2010年和2014年第四季度的加拿大仿制药价格与国际水平的双边比较结果如图 2:2014年瑞士、澳大利亚的仿制药价格高于加拿大,虽然加拿大的仿制药价格高于其余九国,但2014年仿制药的国际价格比值均高于2010年。在加拿大,政府的介入使得仿制药的价格在药品价格利润列表中受到限制,所以生产者竞相为零售客户提供服务和利益而非较低的价格;而且,国家政策将仿制药生产者和药房零售者从市场规律中隔离出来,虽可为仿制药价格产生一种向下的压力,却也影响了专利药和非专利药、仿制药零售商之间的价格竞争,致使仿制药价格仍高于部分参照国。但自从2010年,多数省份实施仿制药价格政策,降低了仿制药价格并节约了重要成本,可见加拿大仿制药价格水平与国际水平的价格差异已逐步缩小。

|
图 2 国家药品价格与加拿大药品价格的价格比值--双边比较[9] |
目前,除《价格监测规定》、《价格异常波动监测预警制度》等适用于全部商品外,仅《药品价格监测办法》(计价格 (2000)2185号) 是针对药品价格监测而言的,而且该办法主要着眼于国内各省区的药品价格监测工作。因此,笔者建议增加对药品价格监测的立法,加强对国内外经济形势和市场药品价格变动及相关因素的跟踪分析,做好预测预警工作,并且依据法律积极采用现代化信息技术加强价格监测工作,组织力量大力开发新的药品价格信息资源,建立国际药品价格信息系统和完善国内药品价格数据库,全面收集、整理价格、成本、供求等相关资料。
3.2 分类确定监测品种目前,我国国家层面较完善的药品价格监测制度仅有《药品价格监测办法》(计价格〔2000〕2185号),其监测内容为药品经营单位实际购进、销售价格及招标采购药品的实际中标价格,并未区分药品类别。加拿大依据《过高价格指南》采用不同的方法监测引入期的新药价格和已上市药品的价格,又根据创新程度将新药分为四类,且采用四种不同的价格测试方法监测其药品价格。鉴于我国药品分类、药品价格政策与加拿大不同,可酌情考虑借鉴其分类监测的思想,根据《药品价格重点监测品种遴选情况说明》遴选出重点监测的药品种类,并将药品按照长期、定期、应急监测品种分类。长期监测品种以群众日常用药为主,应重点关注低价药、紧缺药、品牌药以及市场占比较大药品;定期监测品种可根据各省药品集中采购周期需要就采购品种开展专项监测;应急监测品种需根据突发公共卫生事件处置需要,即时开展。
3.3 探索建立以国际参考价格为警兆指标的药品价格监测预警机制加拿大通过计算药品的国际价格比值,从而有效监测已上市药品的价格变化。我国可以构建类似的价格比值,建立药品价格监测预警机制。第一,选取合适的参考国家,参考国家的遴选可考虑以下几点:(1) 与我国经济发展水平相当;(2) 药品价格市场化程度较高;(3) 药品价格数据可及性较高。由于中国GDP总量和人均GDP与国际比较结果差异较大,选取与我国经济水平相似的国家比较困难。建议组建发达国家和发展中国家两个参考组。在评判药品价格是否过高时,参考发达国家组;反之,则参考发展中国家组。第二,分别采用两个参考组药品价格的中位值作为警戒线。第三,计算国际价格比值,可采用某种药品的最高零售价与国际中位价 (警戒线) 进行比较。第四,根据计算的国际价格比值,划分预警阈值和预警级别。通过构建该监测预警机制,以准确反映药品价格的变动情况,为有关部门进行药品价格监测、宏观调控与管理提供依据,从而保证药品价格在一个合理区间内以符合市场规律上下浮动。
| [1] | 阚玉玲, 常峰. 我国低价药价格监测预警机制研究[J]. 现代商贸工业, 2015 (25): 1. |
| [2] | 中华人民共和国国家计划委员会.药品价格监测办法[Z]. 2000. |
| [3] | 中华人民共和国国家发展和改革委员会.推进药品价格改革的意见[Z]. 2015. |
| [4] | 常峰. 药品国际参考价格在我国的应用[J]. 价格理论与实践, 2015 (7): 14–16. |
| [5] | 张方, 朱越. 加拿大专利药品政府管制定价政策介绍[J]. 中国药物经济学, 2012 (1): 15–19. |
| [6] | Patented Medicine Prices Review Board.Compendium ofPolicies, Guidelines and Procedures[EB/OL].(2015-05-11)[2016-05-27].http://www.pmprb-cepmb.gc.ca/view.asp?ccid=492. |
| [7] | Anis A H, Wen Q. Price regulation of pharmaceuticals in Canada[J]. Journal of Health Economics, 1998, 17 (1): 21–38. DOI:10.1016/S0167-6296(97)00016-7 |
| [8] | 常峰, 阚玉玲. 境外药品价格监测模式及对我国的启示[J]. 中国卫生经济, 2015, 34 (12): 91–93. |
| [9] | Patented Medicine Prices Review Board.Generics360-Generic Drugs in Canada[R]. 2014. |
| [10] | 刘宝. 加拿大药品费用及药品价格管理介绍[J]. 中国药房, 2009 (4): 244–247. |
| [11] | Patented Medicine Prices Review Board[R]. 2009. |
| [12] | 田鹤, 刘洋, 管晓东, 等.药品价格国际比较参比国家遴选方法探讨[C]//中国药学会药事管理专业委员会.2013年中国药学会药事管理专业委员会年会暨"医药安全与科学发展"学术论坛论文集, 2013. |
(编辑 薛 云)





