2. 深圳职业技术学院 广东深圳 518055
2. Shenzhen Polytechnic, Shenzhen Guangdong 518055, China
人口老龄化进程的加快、疾病谱的变迁、新药的高成本,均是造成医药费用上涨的重要因素。同时伴随着药品市场的激烈竞争,制药企业在战略布局中更加重视药品上市速度,但这往往会造成药品临床试验研究的不完全性,新药在真实世界中的安全性、有效性和经济性数据,仍有待上市后再审查和循证医学研究加以确定。在政府财政预算压力和新药存在不确定性的双重背景下,研究如何满足国民医疗卫生需求,降低新药纳入医保目录对医保基金产生的冲击,体现药品物有所值,是各国政府和保险机构面临的挑战。
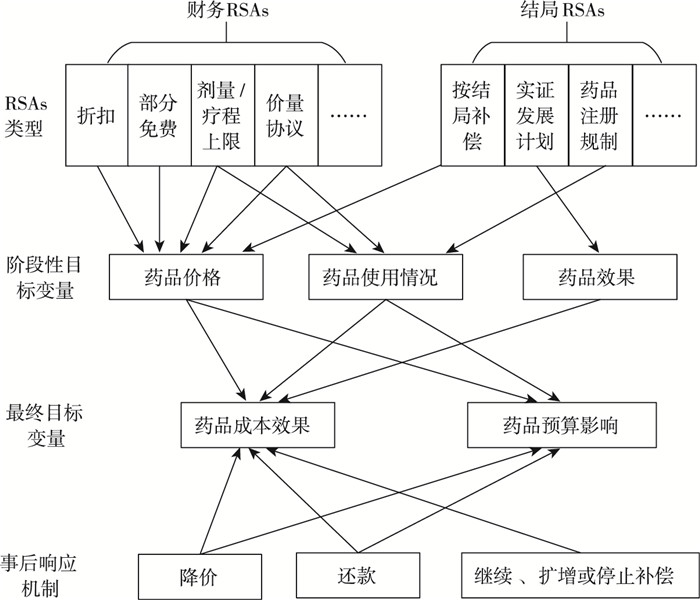
国外有研究者定义风险分担协议 (risk-sharing agreements,RSAs) 为:交易双方基于某产品最终价值存在不确定性而达成的协议,其中厂商对其产品的疗效和效果有足够的信心,并准备根据观察到的绩效接受奖励或处罚。[1]药品风险分担协议政策在欧洲、澳大利亚、美国、新西兰、韩国等国家和中国台湾地区均得到较为广泛应用 (表 1)。RSAs总体可划分为“财务”与“结局”两大类。[2]财务RSAs旨在通过管控药品价格和使用情况,起到控制药品预算,分担政府财务风险的作用,具体表现为药品折扣、使用量上限/药费上限、免费使用、价量协议等形式。结局RSAs则通过管控药品效果、价格、限定适应症范围,来提高药品成本效果,减少超说明书用药行为的发生,具体表现为绩效结局补偿、实证发展补偿和药品注册规制等形式。[3]同时RSAs事后响应机制通常包括降价,还款,继续、扩增或停止补偿3种情况,其运作模型如图 1所示。
| 表 1 全球视野下风险分担协议政策 |
|
图 1 药品风险分担协议模型 |
由于各国卫生服务体系的不同,衍生了多种RSAs称谓,如澳大利亚称为协议契约 (deeds of agreement)、中国台湾称为价量协议、英国称为患者用药可及性方案 (patient access schemes) 等,其实所有的协议均包含了某种形式风险分担,下文将统一使用RSAs这一术语。鉴于澳大利亚和新西兰RSAs实施时间较早且运作管理机制较为完善,同时新西兰是研究范围内唯一将RSAs应用于仿制药的国家;台湾地区作为实施价量协议的新兴市场,其探索和经验可为大陆早期实施RSAs提供借鉴,因此本文将重点对澳大利亚、新西兰和台湾地区的RSAs进行比较研究,以期完善中国大陆RSAs政策。
2 澳大利亚、新西兰和台湾地区药品风险分担协议政策 2.1 主管机构澳大利亚RSAs是由卫生部 (Department of Health) 官员代表澳大利亚政府与药品厂商 (或赞助商) 签订的商业协议,具有法定效力。其中澳大利亚药品福利咨询委员会 (Pharmaceutical Benefits Advisory Committee,PBAC) 和药品福利定价委员会 (Pharmaceutical Benefits Pricing Authority,PBPA) 均可提出RSAs,厂商也可以直接向PBAC提出RSAs。[4]新西兰药品管理局 (Pharmaceutical Management Agency,PHARMAC) 则通过采用多种成本控制方式管控药品费用,早在1993年PHARMAC成立后就开始运作RSAs,现今也是负责审核、执行RSAs的机构。台湾地区RSAs则由“卫生福利部中央健康保险署”(简称健保署) 负责管理,其中健保署可自行启动RSAs,同时全民健康保险药物给付项目及支付标准共同拟定会议 (简称药物拟定会议) 也可要求健保署与厂商开展RSAs。[5]
2.2 适用范围一般而言,由于新药预估对医保基金产生的冲击、成本效果、预期使用情况等因素存在不确定性,因此RSAs往往适用于新药。如澳大利亚会针对成本、临床效果存在不确定性的药品签订RSAs,其中抗肿瘤和免疫调节剂是最常应用的领域。[4]台湾地区RSAs则适用于新药和扩增补偿范围的药品。根据厂商事先提供的财务预估数据或者实际药费支出,如果药品获得补偿后五年间,有任何一年预估药费支出或实际药费支出高于新台币二亿元 (新药) 或新台币一亿元 (扩增补偿范围的药品) 的,适用于RSAs。[6]新西兰RSAs同时适用于新药和仿制药,例如在2007年便与Apotex公司针对其生产的高价仿制药签订了还款协议。[7]
2.3 类型划分澳大利亚、新西兰和台湾地区RSAs存在以下共性,如表 2所示。不同于澳大利亚和新西兰,台湾地区价量协议中包括降价、还款两种机制,可择一或并行处理。
| 表 2 澳大利亚、新西兰和台湾地区RSAs类型比较 |
同时新西兰仿制药RSAs包括以下两种形式:(1) 提案要求书 (Requests for Proposals,RFPs):当特定药品由于生产厂商数量较少,不适用于招标时,PHARMAC会邀请厂商提交RFPs,目的在于增强厂商间为获得医保报销的竞争。(2) 备选商业提案 (Alternative Commercial Proposals,ACPs):当PHARMAC根据暂定的招标目录与药品厂商进行协商时,如果厂商不愿让药品进入招标目录,他们可提供ACPs,然后由PHARMAC权衡ACPs与招标方案的收益与风险,并做出最佳选择。[7]
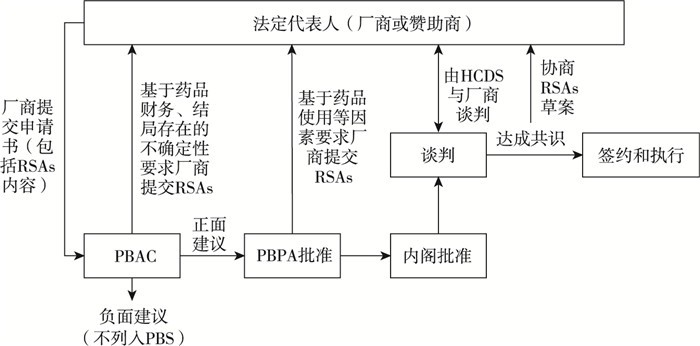
2.4 应用流程在澳大利亚,如果PBAC认定某个申请纳入药品福利计划 (Pharmaceutical Benefits Scheme,PBS) 的药品存在财务、结局风险,便会建议厂商与政府签订RSAs。初期,厂商可以联系高价药品部门 (High Cost Drugs Section,HCDS) 了解协议的程序及标准。对于PBAC正面推荐的药品,PBPA将评估药品使用相关的不确定性及风险并讨论药品的价格,也有可能要求厂商与政府签订RSAs。然后交由内阁批准,虽然RSAs必须在内阁批准后才能执行,但厂商可以在向内阁申请期间与HCDS进行谈判。其中对于涉及财务数据的RSAs,相关预测值需征求有关部门同意,当预测值及连带的降价、还款方案获得同意后,澳洲政府事务律师 (Australian Government Solicitor) 便会草拟一份RSAs送给厂商,并欢迎厂商针对RSAs内容提出修改意见。最后谈判达成共识并签约,由双方履行各自的权利义务 (图 2)。一般而言,RSAs的期限为4~5年。[4]
|
图 2 澳大利亚RSAs应用流程 |
新西兰RSAs类型多样,本文将重点分析RFPs。(1) 提交提案。厂商需通过政府电子招标平台向PHARMAC提交提案。对逾期提交的提案,由PHARMAC在充分考虑对其他厂商的公平性和RFPs程序完整性的基础上,依据行政裁量权决定是否纳入评估范围。(2) 评估。评估委员会 (由PHARMAC职员组成) 评估提案,并做出最佳选择。评估中需参考下列资料:①提案内容;②药理治疗咨询委员会 (The Pharmacology and Therapeutics Advisory Committee,PTAC) 或其他相关附属委员会的临床建议;③其他相关组织或专家的建议;④PHARMAC收到的关于该药品临床使用情况的建议或反馈等。(3) PHARMAC要求厂商提供更多信息。为进一步澄清或评估提案,PHARMAC可以要求厂商提供以下信息,包括 (但不限于):①额外的样品;②医务人员使用该药品时,事先可获得的培训、教育等方面的信息;③公司结构、信用状况和其他相关信息。(4) 谈判。由PHARMAC与厂商进行谈判,对于存在多个提案的情况,将选择其一。谈判将达成暂定协议,如果在合理时间内,PHARMAC没有和厂商达成暂定协议,PHARMAC可以选择终止谈判并与其他厂商进行谈判。(5) 研讨和批准。任何暂定协议都将与厂商或其他利益相关者进行研讨。然后由PHARMAC董事会 (或者官方授权的董事会代表) 考虑暂定协议和研讨结果,做出最终决定。
台湾地区则没有繁琐的协议流程,新药获得补偿后五年间,如果满足RSAs适用范围要求,将自动适应于降价、还款协议。RSAs期限原则上为五年,必要时,可缩短或延长。[6]
2.5 实施效果自2003年以来,澳大利亚RSAs数量逐年增加,从2007的55项上升至2010年的90项,同时所有纳入救生药物计划 (Life Saving Drugs Program,LSDP) 的药品,均会签订RSAs。根据卫生部2012-2013年度财务报告显示,当年RSAs为澳大利亚卫生部节约了3亿元[8],由此可知RSAs在澳大利亚市场的重要性。新西兰RSAs是PHARMAC控制药费支出的重要抓手,2014年6月-2015年6月年度报告显示该年度药品联合预算 (Combined Pharmaceutical Budget,CPB) 为$7.95亿元,其中$7.933亿元用于药品支出,而当年药品费用实际支出为$9.8955亿元,因此至少有$1.9625亿元通过还款的形式由厂商还款给保险机构。[9]另外,2011年6月-2015年6月药品费用支出数据显示,还款方案的成功实施降低了新西兰药品支出的15%~17%。台湾地区RSAs对于控制药品价格,降低医药费用支出也起到了积极作用,有学者分析了2009-2015年间台湾地区与厂商签订RSAs的33种药品,其中26种药品由于RSAs的实施启动了降价机制,平均降幅为11.44%。[10]以拜耳公司利伐沙班片10mg为例,原支付价格为98元,2014年由于RSAs的实施,支付价格调整为82元,降幅达17.4%。同时台湾规定如果厂商在保险机构通知日起,两个月内未响应RSAs的,则自该年10月1日起,支付价格降低5%,若于明年7月底前仍未响应RSAs的,再降价5%,并以此原则逐年降价5%,直至厂商响应RSAs或协议期满。[6]
3 启示通过分析部分国家和地区RSAs实施经验,发现RSAs在降低药品价格、控制药品费用支出、提高药品可及性等方面具有重要作用。同时我国山东青岛于2012年7月1日起,开始正式实施城镇大病医疗救助制度,并首次运用价量协议、病患援助项目两种RSAs将医保目录外的8种特药、1种特材纳入保障范围。到2015年,特药特材项目扩大到26种,并取得了阶段性成效,如截至2015年6月30日,特药特材项目共救助6 760人次;赫赛汀等肿瘤靶向药物的临床有效率达到80%等。[11]随之江苏、江西、浙江、湖南等省市也陆续开展了特药谈判工作,但在我国,RSAs仍属新事物且未经广泛验证,相较于其他国家或地区较为成熟的RSAs,存在协议形式单一、试点范围较窄、缺乏科学论断等问题,因此仍需从以下5个方面加强制度建设。
3.1 完善风险分担协议理论基础在我国实施RSAs前,为避免签订长期产出不明确或者不具备可持续性的协议,首先应完善RSAs理论基础,包括协议的起源、概念、适用范围、分类、应用流程、条款、优劣性等内容。同时为使厂商和保险机构达成双赢协议,需要采取科学的方法对药品安全性、有效性和经济性数据进行评估,但当前我国卫生技术评估 (HTA) 的推广使用情况仍乏善可陈,因此研究HTA在RSAs中的应用,对于提高RSAs的科学性、可操作性和针对性具有重要的理论和现实意义。
3.2 界定风险分担协议适用范围RSAs具有两面性,签订协议本身对利益相关方也有风险,因此需合理界定协议适用范围。近期,鉴于当前我国市场中存在多种治疗重大 (罕见) 疾病临床必需、疗效确切、价格昂贵且难以用其他治疗方案替代的非医保药品,因此保险机构可依据患者需求与基金存量,事先针对该类药品签订财务RSAs。中长期,随着我国卫生技术评估的发展,可探索对疗效和效果存在不确定性、预期会产生净健康效益、无替代性,但为延长患者生命必需使用的药品,探索实施财务和结局RSAs。同时在协议期间内或结束前,需重新审查协议内容,若协议期间并未发生财务、结局风险,则应建议结束协议;如果有必要继续达成协议,则由厂商与保险机构重新谈判,对药品风险进行持续管理。对于招标采购的药品而言,由于其激烈的市场竞争,产品不确定性程度较低,实施RSAs会造成较高的机会成本,不利于卫生资源配置,因此对于我国招标采购的药品往往不适用于RSAs。
3.3 多样化风险分担协议类型RSAs类型具有多样性,仅以价量协议为例,便可细化出多种形式。首先价量协议的限额可用金额、数量、市场份额等指标表示,并包括降价、还款两种响应机制,其中降价、还款比例并非常态化,可视风险程度高低而定。同时价量协议也可设计成多层次的,即可以有一个以上的限额附带不同比例的降价、还款,限额越高,降价、还款比例越高。同时也可以设计为连续几年内有不同的限额。在药品分类管理框架下,RSAs的多样性对实现药品与RSAs的精准匹配具有积极作用。同时实际操作过程中,并不限定于某种单一的RSAs类型,多种RSAs类型的衔接使用将更有利于提高卫生资源配置效率,最大化体现药品物有所值。
3.4 标准化风险分担协议流程RSAs流程包括简单型和复杂型两种。如台湾地区规定当药品符合特定情况时,即可纳入价量协议管理,与我国药品集中采购中量价挂钩不同的是,价量协议着重强调事后控制,即当药品实际药费支出超过约定数量时,则启动降价、还款机制。而澳大利亚和新西兰则往往需要事先与厂商进行沟通、评估委员会评估、谈判、签署、执行等流程,强调事前、事中、事后兼并管理。在我国实施RSAs时,一刀切的管理方式难以适应我国复杂的医药市场,因此建议采用复杂型RSAs流程,具体包括利益相关者提出RSAs、事前讨论、厂商提交材料、评估、反馈 (如有必要,可要求厂商提供更多信息)、谈判、签署、执行、监测 (监测RSAs运行情况)、响应 (降价;还款;继续、扩充或停止补偿等)、复审 (决定是否继续或停止实施RSAs) 等环节,鉴于RSAs理论的复杂性和类型的多样性,实施RSAs前,利益相关者应明确RSAs相较于其它备选方案的收益与风险。
3.5 完备的风险分担协议条款约束科学、完整、合理的协议条款对保障RSAs的实施具有重要作用。制定RSAs时,应重点关注以下5点:(1) 应采取正式的书面协议,最终协议应由各方签字并备案。(2) 应基于机密性和透明性两者平衡的原则,设定协议条款。(3) 应依据充分的证据制定协议内容,包括转化医学和循证医学证据以及新药在真实世界中的临床产出。(4) 协议需包含清晰简便的测量指标,便于测量新药有真实世界中的临床产出。(5) 协议不应单纯包括降价、还款等负向响应机制,如果厂商收集的额外证据足以证据药品成本效果时,应允许提高药品价格,体现药品价值等。
| [1] | de Pouvourville G. Risk-sharing agreements for innovative drugs[J]. The European Journal of Health Economics, 2006, 7 (3): 155–157. DOI:10.1007/s10198-006-0386-6 |
| [2] | Carlson J J, Sullivan S D, Garrison L P, et al. Linking payment to health outcomes:a taxonomy and examination of performance-based reimbursement schemes between healthcare payers and manufacturers[J]. Health policy, 2010, 96 (3): 179–190. DOI:10.1016/j.healthpol.2010.02.005 |
| [3] | Ferrario A, Kanavos P. Dealing with uncertainty and high prices of new medicines:A comparative analysis of the use of managed entry agreements in Belgium, England, the Netherlands and Sweden[J]. Social Science & Medicine, 2015, 124 (12): 39–47. |
| [4] | PBS. Guidelines for Deeds of Agreement[EB/OL].(2011-02-14)[2016-08-20].http://www.pbs.gov.au/info/industry/listing/elements/deeds-agreement. |
| [5] | 何建志. 全民健康保险价量协议法律问题分析[J]. 台大法学论丛, 2014, 43 (2): 381–417. |
| [6] | 卫生福利部中央健康保险署.全民健康保险药物给付项目及支付标准[EB/OL]. (2016-10-11)[2016-12-01]. http://www.nhi.gov.tw/webdata/webdata.aspx?menu=21&menu_id=713&WD_ID=849&webdata_id=4295 |
| [7] | PHARMAC. Medicines and medical devices contract negotiation[EB/OL]. (2016-10-11)[2016-12-02]. https://www.pharmac.govt.nz/about/your-guide-to-pharmac/factsheet-05-contract-negotiation/ |
| [8] | Vitry A, Roughead E. Managed entry agreements for pharmaceuticals in Australia[J]. Health Policy, 2014, 117 (3): 345–352. DOI:10.1016/j.healthpol.2014.05.005 |
| [9] | PHARMAC. Annual Report-year ended 30 June 2015[EB/OL].[2016-12-02].https://www.pharmac.govt.nz/search?search_q=Annual+Report |
| [10] | 常峰, 夏强, 崔鹏磊, 等. 药品价量协议制度的国际经验及启示[J]. 中国新药杂志, 2016, 25 (2): 134–138. |
| [11] | 于子淇. 青岛大病医疗救助制度探索[J]. 中国医疗保险, 2015, 8 (8): 39–40. |
(编辑 薛 云)





