创新药物研发是支撑医药产业发展和满足人民健康需求的关键,世界各国对此都给予高度重视。自上世纪90年代以来,创新药物市场规模快速扩大、具有突破性治疗意义的新药品种不断涌现,2015年全球新药市场已逾6 000亿美元,占药品市场总规模的63%,医药创新的重要性日益显现。从国际创新格局来看,我国仍落后于美日欧等发达医药强国、处于以“精益仿制”为主的第三梯队,上市药品原创性不足、部分产品临床价值有限,尚无法充分参与国际市场竞争。近年由我国自主研发的新药对于全球创新药物市场的贡献率约为4%,仅为美国市场贡献度的1/12,日本市场贡献度的1/3。[1]创新能力不足已然成为我国医药产业发展壮大的瓶颈,在全球知识技术创新浪潮推动以及国家“十三五”创新驱动发展战略的要求下,我国必定要在提高创新药物研发能力方面有所突破。
良好的制度环境是创新能力巩固和提升的土壤,当今创新药物的研发竞争,实质上也已逐渐发展为各国医药政策环境和制度的竞争。[2]作为一项难度较大、风险极高、周期冗长,涉及医学、化学、生物学等诸多领域的高新技术活动,创新药物研发尤其需要政策助力。本文系统比较了中、美、日、欧创新药物的研发现状,以此为基础发掘我国与医药强国创新能力差异产生的政策根源,以期对突破“十三五”我国医药产业创新发展瓶颈、促进医药产业转型升级有所助益。
1 基于国际比较的我国创新药物研发能力分析创新是依靠自主研发力量实现技术突破,并取得原创性的科技成果。[3]创新能力的本质则是将技术知识嵌入于行为过程,可用行为的效率和效果进行测度。[4]本文在综述国内外相关研究并结合医药产业特点的基础上,从资金、人员和产出三个行为方面,选取创新研发(Research and development, R & D)资金投入总量、强度,R & D人员投入总数、强度以及创新药物上市数量、获利能力6个指标,对我国创新药物研发能力进行比较分析。
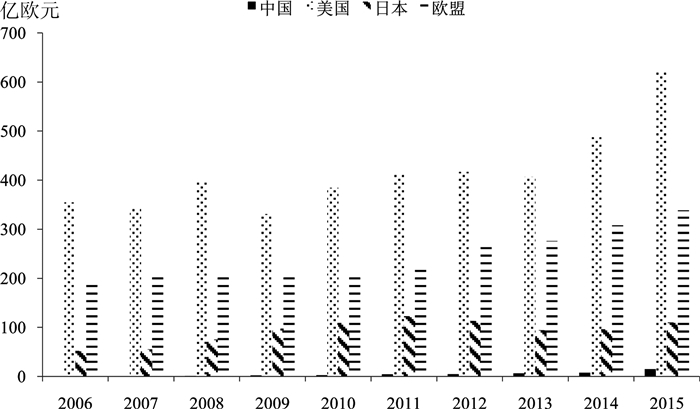
1.1 创新研发资金投入 1.1.1 R & D投入总量较低但增长显著,基础研究阶段的投入比例过低资金是创新药物研发的血液,是创新能力提升的重要保障。有研究发现R & D投入能极大推进医药产业创新发展[5],有研究指出创新药物R & D投入是医药企业科技活动的重要内容,也是其保持优势竞争地位的关键所在。[6]如图 1可知,我国创新药物R & D经费投入近年已有显著增长,相比2006年前的不足4亿元,2015年增长近26倍;但总量上与发达国家相比仍有显著差距,历史投入最高的110亿元仅为美国同期2%、欧盟同期4%左右。
|
数据来源:EU Survey on R & D Investment Business Trends 2007—2016 图 1 2006—2015年部分国家医药R & D投入总量 |
此外,为实现具有突破性意义的原始创新,高水平的基础研究及对其高强度的资金支持是必不可少的。目前,我国在创新药物基础研究阶段的经费投入比例过低、仅占医药R & D经费总投入的15%左右,绝大部分都耗散于应用研究和试验发展,这不仅遏制了原始创新的初始动力、制药企业也难以在R & D活动中真正获得创新能力的提升。[7]美国、日本和欧盟在创新药物基础研究阶段的R & D经费投入比例,则基本都保持在60%左右。
1.1.2 R & D投入强度始终处于低位,目前尚未突破2%R & D投入强度可用以衡量企业技术创新的积极性,也是产业研发信心和创新能力的集中体现。[8]根据OECD定义,R & D强度是指R & D经费投入占工业总产值、工业增加值或企业销售收入的比重。本文选取R & D投入占医药工业总产值的比重作为测量指标进行计算,结果如图 2所示。我国创新药物R & D投入强度始终保持在1.4%~1.8%的较低水平,与发达国家相差7~28倍不等;美国近年投入强度虽有小幅下滑,但始终保持在20%以上,日本、欧盟在2010年后则有小幅增长,创新药物R & D投入强度现稳定在15%。

|
数据来源:《中国高技术产业统计年鉴》;PhRMA Member Company R & D Investment 图 2 2006—2015年部分国家生物医药R & D投入强度 |
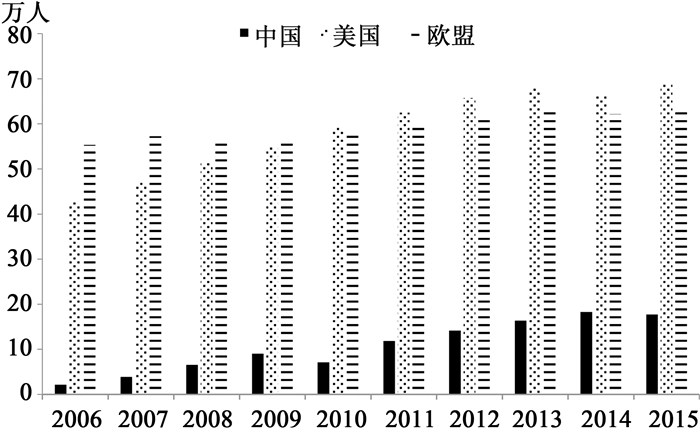
创新药物研发是一项知识密集型的人力资本活动,需要多学科、高层次科研人员的通力合作[9],R & D人员投入水平很大程度上决定了医药产业的创新能力。经过多年发展,我国医药R & D人员在数量上已形成较大规模,2011年首次突破10万人,年增长幅度高达68%;但与科技创新人员基数庞大的发达国家相比仍有较大差距,2011年美国医药领域R & D全时人员已达624 790人,欧盟更是在2006年即已突破50万人(图 3)。
|
数据来源:The Pharmaceutical Industry in Figures;《中国高技术产业统计年鉴》 图 3 2006—2015年中美欧医药R & D人员投入总数 |
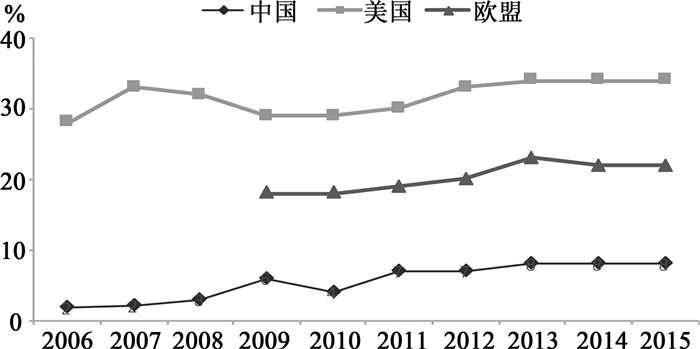
R & D人员投入强度是指从事研究开发的科技人员占行业从业人员的比例,反映了创新研发活动的人力资源储备状况,该比例过低则表示创新人才储备不充分。[10]在前文数据的基础上,本文统计了中、美、欧医药行业从业人员总数并加以计算后得图 4结果,我国医药R & D人员投入强度始终居于低位且增长缓慢,2007年前尚不足2%;美国医药领域的科研人员数量基本保持在其从业人员总数的30%~35%之间,欧盟略低于美国、亦有年均20%的投入强度。
|
数据来源:《中国高技术产业统计年鉴》;Bureau of Labor Statistics, Occupational Employment Statistics 图 4 2006—2015年部分国家医药R & D人员投入强度 |
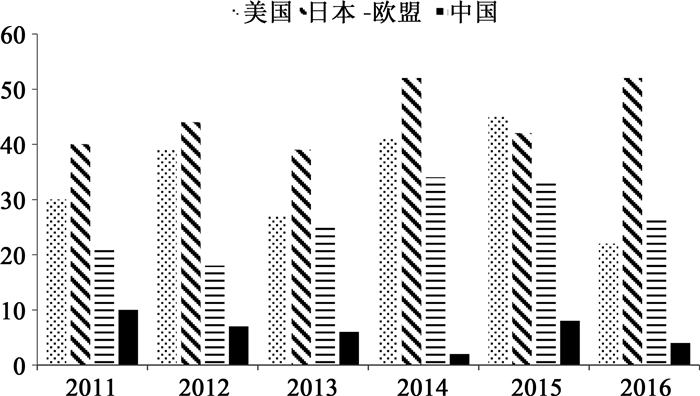
创新能力的提升肇始于高强度的资金和人员投入,[11]同时必须以产出进行衡量,创新研发的根本目标也在于形成真正具有社会经济效益的技术产品。有研究认为新分子实体是衡量医药创新研发能力最鲜明的指标[12],而有研究则指出新生物制品的上市是一国医药产业发展水平获得国际认可的关键[13]。据此,本文统计了2011—2016年间各国批准上市的新分子实体和新生物制品数量,如图 5可知,我国创新药物的研发产出情况不容乐观,近六年上市新药总数尚不及日本一年内上市的数目,同时也远远落后于欧美等老牌创新先驱。
|
数据来源:FDA、EMA、PMDA、CFDA官方网站统计 图 5 2011—2016年中美日欧创新药物获批上市数量 |
良好的市场回报有助于制药企业回收高昂的创新药物研发成本,是创新能力可持续的源泉和保障。[14]当市场竞争趋于成熟后,企业也只有不断研发上市新产品才可能继续获利。[15]从全球范围来看,单个创新药物的研发成本正逐年攀升,现已高达13~18亿元,通过分析特罗凯和赫赛汀2在中、美、日上市五年内的销售数据则可发现,创新药物在我国缺乏可观的市场回报。如表 1所示,特罗凯上市后五年的总销售额仅14亿元、赫赛汀仅3.5亿元,尚不及该药在美国年均销售额的1/8,也远低于日本特罗凯年均4.1亿元、赫赛汀年均3.2亿元的销售增长速度。
| 表 1 特罗凯和赫赛汀在中、美、日上市后五年的销售额对比(亿元) |
从实证评价结果来看,我国创新药物R & D经费投入总量正持续增加,R & D人员数量已渐成规模,但在R & D经费及人员投入强度方面与发达国家的差距仍较为显著,R & D经费投入结构也缺乏合理性。研发投入不足使得自主创新缺乏初始动力,由此导致的创新产出少、质量差或低水平重复又使得二次创新的良性循环无法形成,制约了我国创新药物研发能力的有效提升。这诚然有我国医药工业创新起步晚、底子差的历史原因,也与当前亟待优化的医药政策环境密不可分。
2.1 创新药物研发投入的财税优惠政策缺位相比其他财政工具,税收优惠对于市场的扭曲度最小、操作性最强、成本最低,是激励科研活动开展最为有效的政策手段。有研究指出,医药领域所得税每降低1%,企业R & D投资总额将提高2.13%。[16]发达国家历来重视创新药物研发的财政扶持,所得税优惠的重心也更多放在研究与开发阶段。如美国通过减免、退税、费用扣除、加速折旧等多种方式对R & D实施税收优惠;日本政府为鼓励药物创新也实行了实验研究费税额扣除、向海外出售技术等海外收入给予特别税额扣除的鼓励政策;法国更是将科研人员的薪资开支、购买机器设备的折旧等也划归为R & D费用优惠范围。无论从目标、形式及覆盖面来看,发达国家的财税激励政策都显示出了较强的科学性与合理性,医药企业几乎将近四成的销售收入都用于药物创新及新增长点的发掘。
我国制药企业长期面临研发资金短缺、技术力量薄弱、抗风险能力差等问题,创新药物研发投入总量及强度处处受限。目前虽也有以驱动产业创新为目标的“重大新药创制”专项,政府财政拨款也不断以国家科技计划等为载体投入医药产业创新建设;但专门性的医药R & D财税优惠政策依然缺位,已有的“企业研究开发费用税前加计扣除政策”在执行过程中也存在挑战。首先是可抵扣的研发费用范围较窄且缺少认定细则,如基建土地等固定资产不允许计入、可抵扣的费用限定于上市前研发部分等,对于越来越多的上市后研发(如Ⅳ期临床、新增适应症、联合用药等)都不得计入扣除范围。其次,因委托临床试验所发生的研发费用在加计扣除申报时要提供受托试验机构的详细财务报表,出于生产经营信息保密的考虑,受托机构大多会拒绝向委托企业提交该材料。种种条件制约下,许多大型医药企业只有不足一半的R & D费用能享受到加计扣除优惠,财务制度尚不健全的中小企业甚至与税收优惠政策无缘。
2.2 高端科研人才的培养和布局缺乏合理性人才是创新药物研发的知识源泉,争取和培养科研人才无疑成为各国医药企业发展技术、壮大实力的必由之路。德国通过建立科研人才跨界循环制度,降低紧缺人才移民门槛,资助青年科研人才留学和提供国际交流等方式,有效改善了科研人员职业的稳定性与优越性。日本则以打造生物技术密集型研究群的方式加强基础资源和信息的交流共享,促进知识、技能、人力等创新资源的扩散和外溢,有效提升了科研人才的利用效率。作为全球医药创新的中坚力量,美国汇集了高密度的科研人才和最尖端的研发机构,现已实现了生物医药产业的集群创新。
我国的人力资本总量有一定优势,在教育部重点工程建设及国家重大科研项目扶持下,每年由本土培养的科学和工程领域的博士已超三万人,加速吸引海外人才归国也使科研人员的综合素质有了明显提升。然而,在高层次创新研发人才培养和布局方面现仍缺乏权威明确的政策指引,科研人员的流动、家属随任和生活保障等方面未见明文出台,各地的人才引进标准也过于零散。目前,我国高端科研人才就业集中于高校和科研机构,研究多为跟踪国际热点、原创性不足,难以推动有深远社会影响的自主创新;产业界则缺乏创新药物研发的领军人物,为数不国的海归人才通常只是某一研发环节的专家,缺乏系统完整的创新成功经验。加上我国医药企业大多规模较小,无法提供宽广的研究平台、充足的研发资金以及配套的科研条件,科研人才向大型跨国制药企业汇聚的趋势明显,不利于我国生物医药R & D人员投入强度及产业自主创新实力的提升。
2.3 未能营造起产学研协同创新的宏观环境产学研协同创新是指企业、高校及科研机构等发挥各自的创新优势,将经济发展、知识生产与科学研究有机结合,进而实现协力共赢。[17]虽具有资源共享和知识集成的先天优势,然因各协同主体的利益诉求存在差异,有效的产学研协同创新也离不开清晰的政策引导。美国政府早在二战时即开始关注产学研合作,通过宏观政策调控、行政和经济支持的方式成功打造了企业孵化器、科技工业园和工程研究中心等合作载体,出台了明确权威的用以指导成果归属、利益分配和技术转让的政策法规,在促进科技成果转化和经济发展方面已取得显著成效。
反观我国,科研与产业协同创新的局面尚未形成,创新资源和生产要素长期割裂,每年取得的医药创新成果转化率不足8%,与发达国家50%~70%的转化率相比严重偏低,极大影响了我国医药产业在新科技革命机遇期的创新能力提升。究其原因,主要是我国产学研协同创新机制尚不健全,缺乏系统、可操作的政策文件指引,导致协同的组织形式较为松散,各主体可能会以争取国家项目为目标短期合作,但缺乏长期、战略性的合作意图;其次是我国产学研联盟建设尚处起步探索阶段,协同创新成果与临床防治实践长期存在“两张皮”问题,因缺乏真正具有技术成熟性、预算经济性和市场相容性的成果问世,各主体也失去了共担风险的信心和持续协同的动力。
2.4 医疗保险政策对于创新药物的覆盖不足创新药物上市定价较高、市场容量较小。进入医保目录则意味着创新药物将获得稳定可观的市场,是其销售额提升的重要保障。目前,美国、日本、德国等主要发达国家的医保支付体系均覆盖了创新药物,且报销资质的获得与上市批准基本同步,有效满足了企业回收成本及合理获益的需求,快速累积的销售利润也增强了企业二次创新的实力,形成了医药产业创新的良性循环。
我国医疗保险政策在收录可报销药品时秉持的是“广覆盖”和“保基本”的原则,对于高价创新药物的重视程度不足,2005年至今我国上市的384种新分子创新药仅20%进入了国家基本医疗保险药品目录,且报销收录等待时间至少在5年以上。[1]未能进入目录的创新药上市后销售增长则极为困难,如治疗ALK基因突变型非小细胞肺癌的创新药物克唑替尼(Crizotinib),以目标适应症患者2.4万人和每位患者21万元/年的处方费用估算,该药在我国的年销售潜力应当在52亿元以上;然而,因未被纳入国家及各省医保目录,克唑替尼在我国的实际使用患者数仅为潜在患者总数的0.16%、上市后首年销售额仅850万元。制药企业快速回收研发成本及合理获益的诉求无法得到有效满足,继续加大创新药物研发投入也就无从谈起。
3 小结创新药物研发对于资金和高质素人员的投入要求与我国医药企业的资本实力间正存在较大张力,产出效率低下及市场回报不理想也不利于企业创新能力和技术水平的提升。在全球医药产业竞争日益激烈的当下,加快完善我国创新药物研发政策环境、激发自主创新活力已属刻不容缓。我国应继续增加政府投入并完善创新药物研发的税收优惠政策,制定研发经费税收减免与抵扣的操作办法,增强税收优惠政策的可操作性;改进创新人才的合作培养模式,提高科研人才的使用效率;鼓励科研与生产、创新成果与产业需求的紧密衔接,不断改善产学研协同创新的政策环境;充分认识医保政策对于产业创新发展的重要意义,支持具有较高临床价值的创新药物进入医保目录,并加快医保目录更新。也只有不断推出促进药物创新研发的优势政策,方能缩小我国与发达国家的创新能力差距,甚至实现在重点领域的超越。
| [1] | 中国医药企业管理协会. 构建可持续发展的中国医药创新生态系统[R]. 北京: 中国医药企业管理协会, 2016. |
| [2] | 桑国卫院士: 药物创新本质是政策环境竞争[EB/OL](2016-07-05). [2017-05-19]. http://news.sciencenet.cn/htmlnews/2016/7/350379.shtm |
| [3] | 陈劲. 从技术引进到自主创新的学习模式[J]. 科研管理, 1994(2): 32–34. |
| [4] | Paroutis S. Strategizing Capabilities:Conceptual and Empirical Insights from a Multi-Method Study[C]. Strategic Management Society conference, 2007. |
| [5] | 殷林森, 胡文伟, 李湛. 我国科技投入与产业经济增长的关联性研究[J]. 中国软科学, 2007(11): 57–63. DOI:10.3969/j.issn.1002-9753.2007.11.009 |
| [6] | 杨晓荣, 邱家学. 战略网络视角下的医药企业竞争优势何在[J]. 中国医药技术经济与管理, 2011(3): 52–55. |
| [7] | 丁锦希, 季娜, 李晓婷, 等. 我国生物医药创新投入及其政策成因分析——基于中美欧创新投入现状的实证评价[J]. 科学管理研究, 2012, 30(4): 10–14. |
| [8] | 张玲, 赵立雨, 师萍. 基于国际经验的我国R & D投入强度偏低因素解析[J]. 科技进步与对策, 2010, 27(12): 10–13. |
| [9] | 杨易成. 中国医药产业研发生产力研究[D]. 天津: 天津大学, 2009. http://d.wanfangdata.com.cn/Thesis/Y1677575 |
| [10] | 顾海. 我国医药企业R & D能力与企业可持续发展关系研究[J]. 现代管理科学, 2008(5): 15–16. |
| [11] | Lichtenberg F R. Pharmaceutical Innovation and U.S. Cancer Survival, 1992-2003:Evidence from Linked SEER-MEDSTAT Data:Forum for Health Economics & Policy[J]. Forum for Health Economics & Policy, 2008, 10(1): 1090–1090. |
| [12] | McLean Lan W, David K. Research and Product Innovation in Australian Manufacturing Industries[J]. Journal of Industrial Economics, 1978, 27(1): 1–12. DOI:10.2307/2098114 |
| [13] | Jato J L V. New biopharmaceutical aspects in pharmaceutical nanotechnology[J]. Anales De La Real Academia Nacional De Farmacia, 2007, 73(4): 813–832. |
| [14] | 陈永法, 伍琳, 邵蓉. 药品上市许可与生产许可分离的新制度经济理论研究[J]. 中国医药工业杂志, 2015, 46(9): 1034–1039. |
| [15] | Raymond Vernon. International Investment and International Trade in the Product Cycle[J]. Quarterly Journal of Economics, 1966, 180(2): 190–207. |
| [16] | Zee H H, Stotsky J C, Ley E. Tax Incentives for Business Investment:A Primer for Policy Makers in Developing Countries[J]. World Development, 2002, 30(9): 1497–1516. DOI:10.1016/S0305-750X(02)00050-5 |
| [17] | 刘瑞, 吴静, 张冬平, 等. 中国产学研协同创新政策的主题及其演进[J]. 技术经济, 2016, 35(8): 45–52. |
(编辑 赵晓娟)





