创新药物的市场化进程,决定创新研发回报率,影响研发主体的积极性及创新能力。目前我国重视创新药物研发投入,截至2015年,创新药物经费投入427.95亿元,较2010年的131.40亿元,年均增长率高达37.61%。[1]然而创新药物的经济转化效率并不理想,2015年我国医药制造业的药品投入产出比为1.67%[1],而美国投入产出比高达13.37%[2]。创新药物市场化不仅需要实现对药物设计本身的创新,更需要满足创新药物从研发到市场化链条中各利益相关者的需求。在创新药物经过国家医保目录审核、卫生部门或医联体统一招标、医院采购到真正惠及患者的漫长进程中,涉及多个利益相关主体,利益权衡错杂交汇。本研究通过分析研究创新药物市场准入过程中相关主体及其相互作用机理,构建有效激励创新药物市场准入的政策环境,平衡各利益相关主体需求。
1 文献回顾与理论基础 1.1 利益相关者理论狭义的利益相关者理论为股东中心理论,认为股东是企业的所有者,企业的财产是由他们所投入的实物资本形成并承担企业的剩余风险,理应成为企业剩余索取权与剩余控制权的享有者。[3-4]而广义的利益相关者理论认为所有对企业的生存和发展注入了一定的专用性投资,同时也分担了企业一定经营风险的主体均为利益相关者。[5-6]此后,Freeman与Clarkson的表述则更具代表性,其认为“利益相关者是能够影响一个组织目标的实现,或者受到一个组织实现其目标过程影响的人”,强调利益相关者与企业间的关系,对企业活动有直接或间接影响的均可以作为利益相关者。[5]有国内学者结合上述观点,认为“利益相关者是指那些在企业中进行一定的专用性投资,并承担一定风险的个体和群体,其活动能够影响该企业目标的实现,或受到企业实现其目标过程的影响”,强调专用性投资和利益相关者与企业的关联性,被众多学者所认同和引用[7]。结合专用型投资以及行为主体关联性,本研究将创新药物市场准入过程中的利益相关者定为政府机构、医药企业、医疗机构及患者。
1.2 我国创新药物市场准入阶段划分在创新药物市场准入研究方面,国外学者们从利益相关者视角做出了相关探索性研究。Balotsky从三个利益相关者群体视角重点探讨价格战略与药物研发之间的关系,并提出创新药物价格最大化在降低产品开发风险的同时保障了医药企业的利润率,有助于激励创新。[8]我国创新药物从研发到到达患者手中,需要经历新药申请注册审批、各省物价局备案、备案采购和集中招标采购以及医院进药等流程,因此我国创新药物政策及国内外相关研究主要集中于知识产权、药品定价、医疗保障及招标采购等四个环节。[9-12]
综上,本文将从政府、新药企业、医疗机构和患者视角,从创新药物知识产权保护、药品定价、医保目录准入、药品招标采购四个方面对我国创新药物市场准入政策环境进行深入剖析,最终构建基于利益相关者的创新药物市场准入激励模型。
2 我国创新药物市场准入利益相关主体分析在上述文献综述的基础上,本文将创新药物市场准入各环节中的关键利益相关主体划分为三大类,即创新药物市场准入环境的制定者即核心群落政府机构、创新药物的实际供给群落即医药企业、创新药物的需求群落即医疗机构和患者。
2.1 政府机构政府作为创新药物政策环境创建的核心群落,其决策行为目的从根本上说是为了综合调控医疗卫生资源,满足人民群众的健康需求。政府一方面作为创新药物市场准入政策体系的制定者,其出发点在于通过充分发挥政策的导向作用,激励医药企业进行创新药物上市以及医疗机构和患者使用,提高群众健康效益的同时带动医药卫生产业的平稳发展。而另一方面,作为公共卫生资源的提供者,其所建立的创新药物准入政策体系在保障公民基本健康权益的同时,也要考虑创新药物的经济性。由于公共卫生资源的有限性,政府在创新药物市场准入政策体系建立过程中通过药品定价、医保和招采等方式在合理范围内减少卫生经费支出。
2.2 医药企业作为创新药物供给方的医药企业,需要通过创新药物市场准入而获得经济利益。作为创新药物准入政策影响的直接受体,医药企业的诉求包括强化新药知识产权保护力度、提高研发人员权益,增强企业新药定价自主权利,放宽新药进入医保目录条件以及在药品招标采购中给予一定优惠等。由于医药企业是医疗机构和患者的直接供应主体,医疗机构和患者对于创新药物的实用性、安全性以及经济性的认可和接受程度越高,越能直接提高企业的经济效益,激励企业创新药物研发并积极调整新药市场准入方向以更好地适应市场。
2.3 医疗机构医疗机构的行为需求是通过创新药物的使用提高患者健康效益,同时对患者使用创新药物进行治疗而获得合理报酬以维持医疗机构正常运营。由于目前对于我国公立医院的财政补贴不足以支撑其正常的经营管理,因此我国公立医院仍需通过日常诊疗进行盈利。虽然我国目前实行药品的“零差率”政策,从表面来看医疗机构已无法从药品销售中获取利润,但当政府补贴或医疗服务无法维持医院正常运转,或医药代表行为得不到有效约束时,药品销售与医疗机构之间的利益链条仍难以彻底断开。因此,相较于普通药品,医疗机构及医生更倾向于多开创新药等高价值处方药获取利润。
创新药物由于其研发投入成本较高,虽然能够一定程度上提高患者健康效益,但一般经济成本较高,从公共卫生角度而言是具有负外部性的产品(图 1)。创新药物经过统一招标采购进入医疗机构,且医生的处方行为将直接关系到患者健康和经济利益,通过医保报销制度间接影响政府公共卫生资源的使用。而医疗机构作为理性经济人,通过其处方行为达到经济利益和处方效用最大化,因此,创新药物使用过程中,当社会边际成本和个人边际成本相同时,将追求个人效益的最大化。当创新药物使用量为Q1时,边际社会成本与边际社会收益持平,而当创新药物使用量增加到Q2时,边际个人成本与边际个人收益才能持平,因此医生决定的使用量会高于社会对创新药物的最佳需求,以增加自身利益。

|
图 1 创新药物使用的负外部性 |
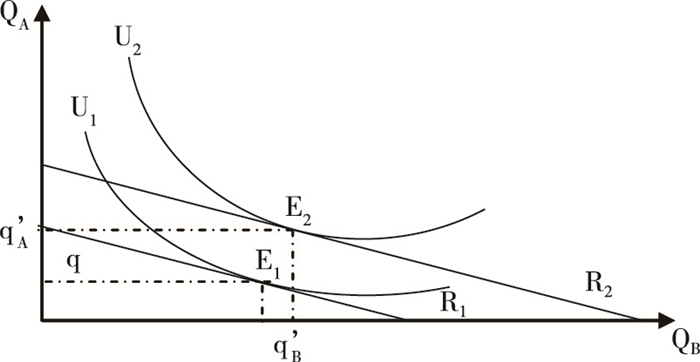
患者对创新药物的诉求不但包括创新药物的有效性和安全性,更包括其经济性。因此,经济基础不同的患者会产生不同层次的健康需求和经济需求,在医生确定治疗方案时会综合考虑其药物效用最大化。R1、R2代表不同经济水平下患者的药品费用预算线,且R1 < R2;U1、U2表示药品效用的无差异曲线,且U1 < U2。在图 2中,假设A和B分别为治疗同种疾病的创新药物和普通药品,A药品价格高于B药品。假设医生面临同样病情的两个患者,给患者开设处方使其均达到较低的U1效用无差异曲线时,有qA和qB数量的两种药品组合,此时患者效用为E1;而随着患者预算的提高,当达到更高效用曲线U2时,获得高效用E2时的药品组合为(q’A, q’B)。从图中可以看出,△qA(qA-q’A)明显大于△qB(qA-q’A),说明当达到较高健康效用E2时,创新药物A增加的量显著高于普通药品B。因此可以得到,从患者需求来看,当患者经济水平达到一定程度,并愿意支付更多的药品费用时,患者更倾向于选择更多的创新药物,给自身带来更高的健康效益。
|
图 2 不同药品费用预算对药品效用的选择 |
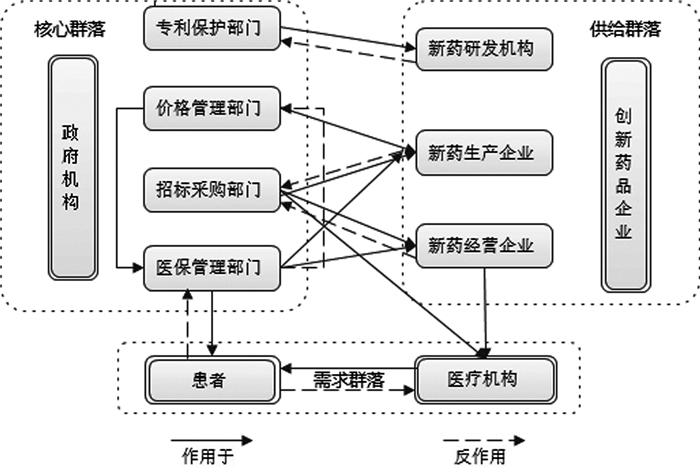
政府作为创新药物市场准入政策环境建立的核心群落,在整个创新药物市场准入和流通体系中占有主导地位。在核心群落内部,不同政府机构部门间也相互作用。由于目前我国实施以药物经济学评价为基础、多方参与的创新药物价格谈判机制,创新药物价格由政府机构与新药企业和专家等谈判制定。由于当下创新药物大多进入医保,为合理降低创新药物价格,减轻医疗保障及患者经济负担,目前创新药物医保价格主要由医疗保障部门代表政府机构进行谈判,因此谈判确定的价格不仅与价格部门相关,更与医疗保障部门密不可分。
政府医药相关部门及其营造的创新药物政策环境,对于医药企业等供给群落进行创新药物上市行为有重要影响:知识产权保护部门影响医药企业在创新药物研发过程中的各类批件申请、批准进程,新药能否获得临床及生产批件、申请周期长短,不但影响到创新药物的专利保护期,更关系到新药后期进入市场后的医药企业的销售盈利;价格管理部门及政策直接关系到创新药物的价格制定以及新药企业的盈利空间;医疗保障和招标采购部门及相关政策直接影响新药企业的创新药物能否进入医保目录以及决定新药能否在竞争激烈的药品市场获得一席之地。政府对于患者和医疗机构组成的需求群落而言,影响较为突出的主要有以下三个方面:一是创新药物谈判价格的确定,直接关系到患者的经济和健康利益,极大影响患者是否使用药品;二是招标采购部门配合医疗机构进行创新药物统一招标采购,在确保药品质量及疗效的同时,以合理价格进入医院;三是医保管理部门则通过医保报销制度影响患者对创新药物的选择和使用,创新药物是否参与报销及报销比例能够从经济的角度影响患者的购药行为。
3.1.2 供给群落作用机制创新药物企业作为创新药物的供给群落,其研发情况反过来影响药品专利保护部门审批流程,对于部分特需创新药,具有审评报批的“绿色通道”。其中创新药物生产经营企业作为创新药物主要供给和销售群落,其生产和经营的创新药物种类、质量、药物经济学评价结果直接影响招采部门在进行药品招标采购过程中政策的制定。创新药物经营企业直接销售对象为医疗机构,虽然创新药物需要经过统一招标采购进入医疗机构进行销售,但医疗机构作为药品销售终端,经过招标采购仅仅是药品进入市场的第一道门槛,创新药物真正由患者购买,需要经过医生的指导,因此新药经营企业会雇佣医药代表与医生进行学术交流,为医生用药提供信息支持的同时促进创新药物销售。
3.1.3 需求群落作用机制患者和医疗机构共同作为创新药物的需求群落,二者相互作用。医疗机构通过向患者提供医疗服务而开具药物处方,患者进而选择是否购买创新药物;而患者的健康利益和经济诉求反过来同样影响医生是否采用创新药物进行治疗。随着我国医疗保障的全覆盖,除了内部的相互作用,创新药物的报销比例会影响患者对创新药物的使用,同时患者使用创新药物的数量和费用影响医保管理部门对创新药物的报销预算和下阶段的财政支持。
|
图 3 创新药物市场准入各利益相关体相互作用机制 |
在确定创新药物在市场准入过程中各利益相关主体的相互作用之后,创建创新药物市场准入环境的作用在于为创新药物提供良好的市场需求环境,实现满足市场用药需求和激励创新主体持续研发的双重作用。在这一阶段,创新药物市场准入环境的构建核心在于通过系统中“无机环境”即“政策环境”的构建,使各利益相关主体积极进行创新药物市场准入。一方面使得生态系统中的创新药物需求方(医疗机构、患者等)对创新药物的临床需求得以满足;另一方面使生态系统中的创新药物供给方(研发主体等)能够获得应有的收益并促进创新药物的持续研发。最终通过“无机政策环境”的构建满足创新药物的消费需求,并在政策导向的基础上,利用市场机制实现创新药物研发资源的合理配置和价值回报(图 4)。

|
图 4 利益相关者视角下下创新药物市场准入政策环境 |
具体来说,构建有效的创新药物市场准入政策环境需要通过建立创新药物市场需求导向机制,使政府机构将医疗机构及患者的健康需求反馈到市场准入政策中。在此基础上建立的市场准入政策环境,通过知识产权的保护和专利期的适当调整、谈判机制合理制定新药价格、招标和采购政策的优惠以及医保政策的支持等激励新药生产企业及研发机构进行创新药物研发和上市,同时有效保证医疗机构及患者的经济和健康利益。通过有机群落和无机环境之间信息的循环反馈,不断完善我国创新药物市场准入环境,进而满足各利益相关主体的需求促进整个创新药物市场优化升级。
4 建议 4.1 缩短创新药物审评审批周期,提高我国创新药物知识产权的保护力度我国创新药物临床及生产批件的大量积压,直接导致我国上市的创新药物专利实际有效期比欧美等国短4~6年,影响供求主体即新药研发及生产企业的积极性。因此应针对创新药物的注册审批流程及审批各环节时间作出明确规定,并严格按照规定实施,力求提高创新药物注册审批审评效率。此外,针对我国创新药物数据保护制度不完善及可操作性较差的问题,应加大创新药物支持产权保护力度,着力满足新药研发及生产企业的创新药物市场独占需求。
4.2 明确界定我国创新药物的创新级别,建立健全药品价格谈判机制我国由于未能明确药物自主创新级别,部分创新药物未能享有专利药和独家药品的定价权利,在进行价格谈判机制时处于弱势地位,或只能通过市场调节自主定价。因此应明确划分我国创新药物的创新级别,同时建立健全药品价格谈判机制,鼓励各利益相关主体积极参与谈判。通过药物经济学评价,提高创新药物的经济性,在弥补供给群落研发投入的基础上,合理压缩创新药物价格水分,在满足患者健康诉求的同时降低其经济负担。
4.3 建立创新药物进入医保目录的定期增补机制,满足各利益相关主体的经济及健康需求激励创新药物研发主体积极性,为创新药物进入医保目录设置“绿色通道”。我国基本医疗目录更新频率低且遴选标准对创新药物尤其高价值创新药物不利,延缓创新药物供给群落的研发上市进程和积极性。通过规范创新药物进入医保目录的标准谈判流程,努力完善并建立创新药物进入医保目录的谈判增补机制,不但能使新药研发主体得到合理的经济回报,而且有利于提高整个社会的健康水平。
4.4 招标采购过程中重视药品的创新科技含量,鼓励招标采购创新药物我国各省招标采购流程不一,且采购周期较长,使得我国创新药物在注册上市后往往经过3年才能正式进入临床应用,不但消耗了创新药物的专利保护期,使得新药研发及生产机构利益受损,也延缓了患者对创新药物需求的满足。今后政府应着力改善药品招标采购环节中唯低价是取的现象,根据药物经济学评价结果对创新药物的质量效果进行合理认证,扩大创新药物招标采购范围,缩短其进入医疗机构的周期。
| [1] | 国家统计局. 中国高技术产业统计年鉴[M]. 北京: 中国统计出版社, 2016. |
| [2] | The National Science Foundation (NSF). Business Research and Development and Innovation:2014[EB/OL]. (2016-01-01)[2016-08-02]. https://www.nsf.gov/statistics/2016/nsf16315/nsf16315 |
| [3] | Grossman S J, Hart O D. The costs and benefits of ownership:A theory of vertical and lateral integration[J]. Journal of Political Economy, 1986, 94(4): 691–719. DOI:10.1086/261404 |
| [4] | Hart O, Moore J. Property rights and the nature of the firm[J]. Journal of Political Economy, 1990, 98(6): 1119–1158. DOI:10.1086/261729 |
| [5] | Freeman R E. Strategic management:A stakeholder approach[J]. Cambridge University Press, 1984. |
| [6] | Blair M M. For whom should corporations be run?:An economic rationale for stakeholder management[J]. Long Range Planning, 1998, 31(2): 195–200. DOI:10.1016/S0024-6301(98)00003-X |
| [7] | 贾生华, 陈宏辉. 利益相关者的界定方法述评[J]. 外国经济与管理, 2002(24): 13–18. |
| [8] | Balotsky E R. Where strategy and ethics converge:Pharmaceutical industry pricing policy for medicare part D beneficiaries[J]. Journal of Business Ethics, 2009, 84(1): 75–88. |
| [9] | 刘昌孝. 我国医药产业创新药物研发面临的问题及对策探讨[J]. 中国药房, 2012(22): 2017–2020. DOI:10.6039/j.issn.1001-0408.2012.22.01 |
| [10] | 常峰, 罗修英, 崔鹏磊. 典型国家基于价值的新药定价机制及对我国的启示[J]. 中国新药杂志, 2015(18): 2047–2051. |
| [11] | 崔孟珣, 彭奕, 赵瑾, 等. 国内外新药进医保目录的比较研究及对我国相关政策建议[J]. 药学实践杂志, 2011, 29(3): 226–228. |
| [12] | 马爱霞, 赵力利. 浅析我国创新药物的市场化障碍及其对策[J]. 中国医药指南, 2011, 9(22): 356–358. DOI:10.3969/j.issn.1671-8194.2011.22.272 |
(编辑 赵晓娟)




