2. 国家卫生健康委员会卫生经济与政策研究重点实验室(山东大学) 山东济南 250012
2. NHC Key Laboratory of Health Economics and Policy Research(Shandong University), Jinan Shandong 250012, China
自1928年青霉素被发现以来,抗生素的发现和使用对人类的健康和社会的进步发挥了巨大的促进作用。然而自20世纪70年代末,新型抗生素的研发速度渐慢,1984年以来再无全新结构的抗生素上市。[1]相对应的是,抗生素耐药问题的迅速加剧,并在世界范围内逐渐蔓延。[2]其中,抗生素滥用是造成耐药性的重要原因之一,过去10年间,全球抗生素处方量相比之前增加了36%;相关数据显示,多达50%的抗生素使用不当。[3]这促使世界各国对抗生素耐药问题越来越重视并相继采取了治理行动,然而通过梳理国际文献发现,目前尚无文章系统梳理世界各国和各个组织的治理情况,因此本文从研究角度将抗生素耐药性全球治理的发展历程进行归纳梳理,总结并探讨其趋势和特点,以期为抗生素耐药性持续治理提供借鉴。
1 研究方法本研究采用范围综述的方式,由两名研究员独立的开展文献检索和筛查工作。
1.1 数据收集在常用期刊数据库ISI Web of Science、Pubmed、Medline中,以“Antibiotic resistant”、“AMR”、“antimicrobial resistant”、“globalization”、“global”、“worldwide”、“international”、“stewardship”、“governance”、“administration”、“intervention”、“strategy”、“control”、“policy”、“progress”和“development”为关键词对文献进行检索。同时在世界卫生组织(World Health Organization, WHO)、联合国(United Nations,UN)、联合国粮农组织(Food and Agriculture Organization of the United Nations,FAO)、世界动物卫生组织(World Organization for Animal Health,OIE)等与抗生素耐药治理有关的关键行为体的网站收集相关报告、会议记录、政策简报等资料。
1.2 分析方法依据范围综述的分析方法,制定信息提取表。以发表时间、文献或者文件题目、作者或发布机构、主要事件、文件类资料的文号等作为提取指标,依次对每份纳入的资料进行信息的提取。通过对提取表中的内容进行归纳总结和具体分析,梳理抗生素耐药性全球治理的发展阶段、特点和趋势。
2 研究结果 2.1 期刊文献检索结果与分析将检索出的文献合并后去除重复,共计检索出文献8 102篇,后由两名研究人员分别对所有文献的题目和摘要逐一进行阅读,对筛查出的相关文献进行合并去重后,共筛查出305篇相关文献。经阅读全文后,根据纳入标准排除不相关文献74篇,排除后合计231篇文献纳入分析。
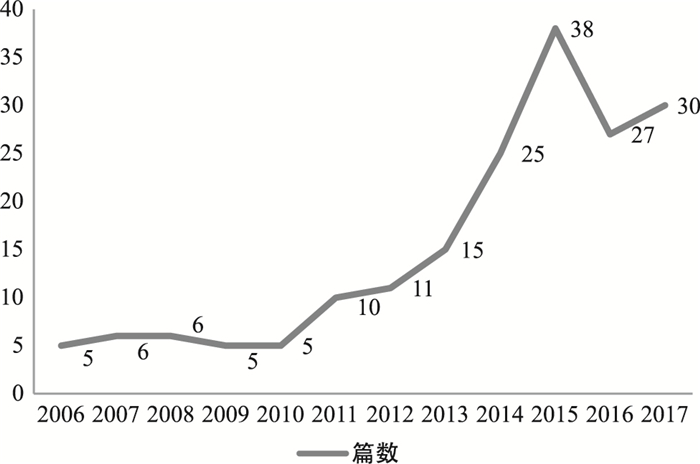
纳入的有关国际抗生素耐药性治理的文献中,最早的一篇发表于1983年,发表数量呈现逐年上涨的趋势,2000年以前发表的相关文献数量较少,仅占7%。2001—2010年文献发表数量变化趋于平缓,2011年开始明显增加。近几年间,有关抗生素耐药性全球治理的文献发表数量较之前翻了几倍,在2015年到达顶峰(图 1)。
|
图 1 抗生素耐药性全球治理文献发表年度分布 |
在纳入的相关文献中,原创性研究112篇,占48.5%;综述类文章65篇,占28.1%,主要描述世界各国抗生素耐药问题的严重性、探讨和比较各国治理策略和行动;会议学术报告类文章12篇;新闻报道类文章17篇,其中有9篇来自于WHO;其余25篇文献被归为其他类。
2.2 抗生素耐药性全球治理的发展历程 2.2.1 第一阶段:萌芽阶段(20世纪80—90年代)在可查阅的资料中,最早针对抗生素耐药问题的全球治理是WHO的抗生素耐药技术工作组于1981年11月23—27日召开的控制耐药细菌的会议,[4]提出了监测病原菌耐药以及控制抗生素在医院中的使用。之后近20年时间是全球开展抗生素耐药治理的萌芽阶段,主要有以下特点:
(1) 立足于医院,以监测为主要治理手段。在这一时期WHO、FAO等国际组织主要针对医院的抗生素滥用问题提出了促进合理用药和耐药监测的想法, 同时WHO牵头开展了相关的监测行动,并初步建立了全球性的监测网络,通过监测耐药情况和趋势以引起世界各国的注意。1989年WHO抗生素耐药监测合作中心开发了WHONET软件[5],至1996年包括中国在内有31个国家的160个临床、公卫、兽医及食品实验室使用了WHONET系统对抗生素耐药进行了监测,部分国家发表了监测结果[6]。该系统的使用有助于以统一的方式显示从各个地区获得的抗生素耐药数据,以帮助报告和跟踪各地区和全球的耐药性趋势,从而制定决策、采取行动。[7-8] 1998年,14个欧美国家合作成立了针对医院中出现的抗生素耐药性的国际监测项目(International Network for the Study and Prevention of Emerging Antimicrobial Resistance,INSPEAR),该项目的实施可迅速向世界各地的医院发送新出现的耐药生物信息,以此作为预防新病原体出现或传播的有效模式。[9]
(2) 由发达国家主导。这一阶段世界范围内还未真正重视到抗生素耐药性问题的严重性,治理行动由发达国家主导,同时主要由来自发达国家的有效监测数据为抗生素耐药全球治理策略的制定提供依据。1995年由美国微生物学会(American Society for Microbiology,ASM)建立的一个工作小组建议针对抗生素问题采取监测措施[10],后于1996年成立了国家抗生素耐药性监测系统(The National Antimicrobial Resistance Monitoring System for Enteric Bacteria,NARMS)[11];欧洲委员会也在1998年建立了欧洲最大的公共资助抗生素耐药性监测网(European Antimicrobial Resistance Surveillance Network,EARS-Net),该监测网络的出现提高了欧洲监测数据的质量,提供了大量有关抗生素耐药性的参考数据[12]。除此之外,许多发达国家在这个阶段就已经发布了本国的治理计划,如1995年丹麦开始监测可食用动物的抗生素药物使用情况,并发布了综合性抗生素耐药性监测和研究计划[13-14],同年瑞典也发布了一项全国性的应对抗生素耐药性的战略计划[15]。
2.2.2 第二阶段:快速发展阶段(21世纪初—2010年)2001年,WHO发布了当时非常具有影响力的一份治理策略“遏制抗生素耐药性全球战略”[16],其中包含14项重点干预措施和67项建议,该战略作为有针对性的宣传工具,进一步提高了世界范围内对抗生素耐药问题的认识[17]。21世纪初至2010年进入了抗生素耐药性全球治理的快速发展阶段,这个阶段的治理行动主要有以下特点:
(1) 国际组织推动下,治理行动蔓延至发展中国家。在这一时期国际组织开始频繁制定抗生素耐药性的全球治理策略并开展行动,号召世界各国加入到抗生素耐药问题的治理中。根据WHO的建议,欧美国家率先采取了更加广泛的行动,美国政府部门先后发布了几份公共卫生行动计划,其中较有影响力的一份是于2001年1月公布的呼吁采取“果断行动”遏制抗生素耐药性蔓延的全面公共卫生行动计划。[18]欧洲也成立了抗生素耐药性监测研究小组(ESCMID Study Group for Antimicrobial Resistance Surveillance,ESGARS),探讨耐药性监测技术的多样性,审查耐药性数据,建立监测项目网络之间的联系。[10]2005年第58届世界卫生大会通过了对《国际卫生条例》的修订,要求WHO和会员国加强合作,增加在发展中国家的抗生素耐药监测资源。[19]基于此,发展中国家也逐渐开展了本国的治理行动。2003年,泰国在成功控制SARS传播的基础上,通过政府的支持,于2004年建立了国家抗生素耐药性监测中心和食品生产动物抗生素耐药性监测中心。[20]中国为应对日益严重的抗生素耐药性问题,在2004年发布了在临床实践中使用抗菌药物的指南,旨在指导抗生素使用和禁止向没有处方的患者销售抗生素。[21-22]
(2) 全球治理向多领域拓展。这一阶段,除了监测措施外,对抗生素耐药性的治理行动开始拓宽,跨领域跨区域合作日益频繁,同时世界范围内开始重视社会和公众的参与。其中比较有代表性的行动是欧洲疾病预防与控制中心指定2008年11月18日为欧洲抗生素意识日(European Antibiotic Awareness Day,EAAD),并在每年的这一天举办宣传活动,抗生素意识日使全欧洲的社会公众对预防感染和合理使用抗生素的必要性有了更广泛的认识。[23]此外,FAO、WHO和OIE开展了卫生、农业、畜牧业的联合治理行动,其中于2007年联合发布的一项重要的抗生素联合分类,目的就是在动物卫生需求和公共卫生考虑之间找到适当的平衡。[24]
2.2.3 第三阶段:全面覆盖阶段(2011年至今)2015年,第68届世界卫生大会通过了抗生素耐药性全球行动计划(Global Action Plan,GAP),概述了在“One Health”框架下多个部门联合开展抗生素耐药的治理行动的主要目标,并要求会员国在两年内制定各自的国家行动计划[29]。这代表抗生素耐药治理开启跨地域、跨部门的全面治理阶段,其特点包括:
(1) 重要政策报告引起全世界关注。近十年间,国际组织和世界各国纷纷发布了针对抗生素耐药问题的政策报告,这些报告的发布使越来越多的国家,特别是发展中国家对抗生素耐药性问题有了更清楚地了解,并深刻意识到了其严重性。2014年5月,WHO发表了“抗生素耐药性:全球监测报告”和“抗生素耐药性全球地图”,并警示说“后抗生素”时代可能很快就会成为现实。[25-26]同年12月,英国政府委任经济学家吉姆奥尼尔组织撰写并出版的报告《抗生素耐药性:应对一场卫生和国家财富的危机》,是其根据2013年的“五年战略规划”发表的抗生素耐药性的年度进展和实施报告。这份报告预计未来35年内,将有3亿人死于抗菌素耐药性且将给世界经济带来灾难性的打击。[27]
(2) 最高政治层面聚焦抗生素耐药问题。全球化的加速使得抗生素耐药性问题愈加严峻,区域性的治理行动无法真正解决这一问题,几次国际会议将抗生素耐药问题提升到了新的政治高度。2016年的杭州G20以及2017年德国汉堡G20峰会,均指出抗生素不仅严重危害公众健康,同时对经济和社会发展均产生不利影响。此外,在WHO等国际组织及各类民间组织的推动下,抗生素耐药的议题被推至联合国。2016年9月21日,联合国第71届大会第四次会议上提出“解决这个迫在眉睫的全球性挑战:抗生素耐药性”。世界各国领导人在这次会议上签署了宣言,承诺要解决抗生素耐药性问题并制定国家行动计划[28],这是历史上第四次针对健康问题召开的高级别会议。
(3) 多国参与下的全面治理。此阶段,多数发展中国家制定了本国的全面治理计划并积极参与到全球治理行动中。印度、南非、越南、菲律宾等国在GAP发布后纷纷设立了国家监测机构,收集、跟踪和报告抗生素耐药的趋势。[29]其中南非于2014年发布了“抗生素耐药性国家战略框架”,截至2017年,非洲地区已有47个国家实施了“对抗抗生素耐药性的一揽子计划”。[30] 2016年,中国14部委联合发布了《遏制细菌耐药国家行动计划(2016—2020年)》[31],旨在从国家层面多个领域开展有效遏制细菌耐药的行动。2014年中国举办了“One Health”国际研讨会,来自7个国家的200多名国际代表共同讨论了“人畜共患病、食品安全、环境科学和抗生素耐药性”问题。该会议不仅建立了“One Health”的官方网站,同时也为抗生素耐药治理的国际合作提供了平台。[32]
3 讨论 3.1 抗生素耐药性全球治理不同阶段的特点和原因抗生素耐药问题全球治理的第一个阶段是20世纪80—90年代的萌芽阶段。从20世纪50年代初开始频繁报道医院发生的耐青霉素葡萄球菌感染[33-34],到80年代初耐多药金葡菌成为导致院内感染的主要因素[35-37],耐药菌在医院的传播开始引起WHO等国际组织以及欧美等发达国家关注。同期,新抗生素的出现也越来越少,人们逐渐意识到仅靠发现和研发新抗生素不能解决抗生素耐药的问题。因此,在这一阶段国际上主要采取了以发达国家为主导、针对医院、以监测为主要手段的治理策略。
21世纪以来,全球化使世界各国的关系越来越紧密,商贸、旅游的日益频繁使抗生素耐药性的危害日益凸显,同时农业上抗生素滥用越严重,以对医院监测为主的治理策略难以控制抗生素耐药问题。因此全球治理进入了第二阶段,即从21世纪初到2010年的快速发展阶段,治理策略从以耐药监测为主转变为多领域共同治理。此阶段基于WHO遏制抗生素耐药性全球战略,各国的抗生素耐药性治理有了方向,发展中国家也逐渐参与到全球治理行动中,治理行动逐渐向多地区多领域拓展。
第三阶段为全面覆盖阶段,越来越多的国家积极参与到抗生素耐药的全球治理中,联合国和各政治论坛的关注和重视将抗生素耐药问题提高到政治高度,各权威机构和领域的专家学者的政策报告引起全世界的关注,WHO出台了指导各国家开展全面治理行动的方案。越来越多的国家开始制定计划并采取严格的措施来控制、预防和监控抗生素耐药性,抗生素耐药性治理进入全球行动阶段。
3.2 抗生素耐药性全球治理对我国的借鉴意义 3.2.1 多领域协同治理抗生素耐药性目前中国抗生素耐药性的治理主要由国家卫健委医政医管局牵头,其工作重心主要在医院,很少涉及其他领域。但纵观国际越来越多的有效措施都是联合卫生、食品、农业、环境等多个领域共同开展。因此,我国政府和各领域专家学者应在国家行动计划的带动下,积极开展跨领域跨部门的合作。比如可制定全链条的监测计划,农业部负责监测动物使用及耐药情况,疾控中心监测人类的使用和耐药情况,环境部监测水和土壤中抗生素残留以及耐药情况等,并建立数据平台共享各部门监测数据。
3.2.2 以更加积极主动的姿态参与全球治理任何国家都难以单独应对抗生素耐药性问题,因此,下一步中国应主动加入全球抗生素耐药监测系统(Global antimicrobial resistance surveillance system, GLASS),逐步与国际分享现有的耐药数据,实时参与和关注全球监测工作。此外,与其他国家开展研究合作。
3.2.3 提高社会公众对抗生素耐药性的重视我国从21世纪初已经开始关注抗生素耐药问题,但侧重于临床实践,然而抗生素耐药性的发展影响每一个人,因此社会各界和公众都可以为遏制抗生素耐药性的发展做出贡献。我国政府和可以参考欧洲抗生素意识日,每年选取一天集中开展抗生素使用和耐药现状的宣传活动,加强公众对抗生素耐药性问题的了解,有针对性的对不同人群进行抗生素耐药性知识宣传,使公众自觉参与到抗生素耐药治理行动中。
作者声明本文无实际或潜在的利益冲突。
| [1] |
Elder D P, Kuentz M, Holm R. Antibiotic Resistance:The Need For a Global Strategy[J]. J Pharm Sci, 2016, 105(8): 2278-2287. DOI:10.1016/j.xphs.2016.06.002 |
| [2] |
Tiong J J, Loo J S, Mai C W. Global Antimicrobial Stewardship:A Closer Look at the Formidable Implementation Challenges[J]. Front Microbiol, 2016(7): 1860. |
| [3] |
Mendelson M, Matsoso M P. The World Health Organization Global Action Plan for antimicrobial resistance[J]. S Afr Med J, 2015, 105(5): 325. DOI:10.7196/SAMJ.9644 |
| [4] |
W HO. Antimicrobial resistance[J]. Bulletin of the World Health Organization, 1983, 61(3): 383-394. |
| [5] |
WHO. Emerging and other communicable diseases: antimicrobial resistance[R]. 1998.
|
| [6] |
Rahal K, Wang F, Schindler J, et al. Reports on surveillance of antimicrobial resistance in individual countries[J]. Clin Infect Dis, 1997, 24(Suppl 1): S169-S175. |
| [7] |
Sharma A, Grover P S. Application of WHONET for the surveillance of antimicrobial resistance[J]. Indian J Med Microbiol, 2004, 22(2): 115-118. |
| [8] |
Okeke I N, Klugman K P, Bhutta Z A, et al. Antimicrobial resistance in developing countries. Part Ⅱ:strategies for containment[J]. Lancet Infect Dis, 2005, 5(9): 568-580. DOI:10.1016/S1473-3099(05)70217-6 |
| [9] |
Putman L. Keeping global tabs on antimicrobial resistance[J]. The Lancet, 1998, 351(9111): 1264. |
| [10] |
Bax R, Bywater R, Cornaglia G, et al. Surveillance of antimicrobial resistance——what, how and whither?[J]. Clin Microbiol Infect, 2001, 7(6): 316-325. DOI:10.1046/j.1198-743x.2001.00239.x |
| [11] |
McDermott P F, Zhao S, Wagner D D, et al. The food safety perspective of antibiotic resistance[J]. Anim Biotechnol, 2002, 13(1): 71-84. DOI:10.1081/ABIO-120005771 |
| [12] |
Tacconelli E, Sifakis F, Harbarth S, et al. Surveillance for control of antimicrobial resistance[J]. The Lancet Infectious Diseases, 2017, S1473309917304851. |
| [13] |
Dibner J J, Richards J D. Antibiotic growth promoters in agriculture:history and mode of action[J]. Poult Sci, 2005, 84(4): 634-643. DOI:10.1093/ps/84.4.634 |
| [14] |
Wallinga D, Rayner G, Lang T. Antimicrobial resistance and biological governance:explanations for policy failure[J]. Public Health, 2015, 129(10): 1314-1325. DOI:10.1016/j.puhe.2015.08.012 |
| [15] |
Molstad S, Lofmark S, Carlin K, et al. Lessons learnt during 20 years of the Swedish strategic programme against antibiotic resistance[J]. Bull World Health Organ, 2017, 95(11): 764-773. DOI:10.2471/BLT.16.184374 |
| [16] |
Simonsen G S, Tapsall J W, Allegranzi B, et al. The antimicrobial resistance containment and surveillance approach——a public health tool[J]. Bull World Health Organ, 2004, 82(12): 928-934. |
| [17] |
Campbell S. The need for a global response to antimicrobial resistance[J]. Nurs Stand, 2007, 21(44): 35-40. DOI:10.7748/ns.21.44.35.s53 |
| [18] |
Burke J P. Antibiotic resistance:closing the loop[J]. Curr Opin Infect Dis, 2001, 14(4): 433-436. DOI:10.1097/00001432-200108000-00006 |
| [19] |
WHO. Antimicrobial resistance: a threat to global health security[R]. 2005.
|
| [20] |
Sirinavin S, Dowell S F. Antimicrobial resistance in countries with limited resources:unique challenges and limited alternatives[J]. Semin Pediatr Infect Dis, 2004, 15(2): 94-98. DOI:10.1053/j.spid.2004.01.012 |
| [21] |
Wang X M, Zhou X D, Hesketh T. Massive misuse of antibiotics by university students in China:a cross-sectional survey[J]. Lancet, 2016, 388(Supp1): S94. |
| [22] |
Dar O A, Hasan R, Schlundt J, et al. Exploring the evidence base for national and regional policy interventions to combat resistance[J]. Lancet, 2016, 387(10015): 285-295. DOI:10.1016/S0140-6736(15)00520-6 |
| [23] |
Charani E, Cooke J, Holmes A. Antibiotic stewardship programmes——what's missing?[J]. J Antimicrob Chemother, 2010, 65(11): 2275-2277. DOI:10.1093/jac/dkq357 |
| [24] |
Guardabassi L. Sixty years of antimicrobial use in animals:what is next?[J]. Vet Rec, 2013, 173(24): 599-603. DOI:10.1136/vr.f7276 |
| [25] |
WHO. Antimicrobial Resistance: Global Report on Surveillance 2014[R]. WHO: Genova.
|
| [26] |
Woolhouse M, Farrar J. Policy:An intergovernmental panel on antimicrobial resistance[J]. Nature, 2014, 509(7502): 555-557. DOI:10.1038/509555a |
| [27] |
Antimicrobial resistance: in terms politicians understand[J]. Lancet, 2014, 384(9961): 2173.
|
| [28] |
Gulland A. World leaders pledge action on antimicrobial resistance[J]. BMJ, 2016, 354: 5171. |
| [29] |
Chaudhary A S. A review of global initiatives to fight antibiotic resistance and recent antibiotics discovery[J]. Acta Pharm Sin B, 2016, 6(6): 552-556. DOI:10.1016/j.apsb.2016.06.004 |
| [30] |
Essack S Y, Desta A T, Abotsi R E, et al. Antimicrobial resistance in the WHO African region:current status and roadmap for action[J]. J Public Health (Oxf), 2017, 39(1): 8-13. |
| [31] |
Cui D, Liu X, Hawkey P, et al. Use of and microbial resistance to antibiotics in China:a path to reducing antimicrobial resistance[J]. J Int Med Res, 2017, 45(6): 1768-1778. DOI:10.1177/0300060516686230 |
| [32] |
Wu J, Liu L, Wang G, et al. One Health in China[J]. Infect Ecol Epidemiol, 2016, 6: 33843. |
| [33] |
Serck-Hanssen F. Penicillin-resistant staphylococci in a hospital's environment and in acute puerperal mastitis[J]. Acta Chir Scand, 1952, 104(2-3): 236-243. |
| [34] |
Rountree P M, Barbour R G. Incidence of penicillin-resistant and streptomycin-resistant staphylococci in a hospital[J]. Lancet, 1951, 1(6652): 435-436. |
| [35] |
Price E H, Brain A, Dickson J A. An outbreak of infection with a gentamicin and methicillin-resistant Staphylococcus aureus in a neonatal unit[J]. J Hosp Infect, 1980, 1(3): 221-228. DOI:10.1016/0195-6701(80)90059-6 |
| [36] |
Rubin L G, Medeiros A A, Yolken R H, et al. Ampicillin treatment failure of apparently beta-lactamase-negative Haemophilus influenzae type b meningitis due to novel beta-lactamase[J]. Lancet, 1981, 2(8254): 1008-1010. |
| [37] |
Gragan D, King K, Brady L, et al. Gentamicin-resistant staphylococci[J]. Lancet, 1981, 2(8248): 698-699. |
(编辑 赵晓娟)





