2018年3月,第十三届全国人大会议通过了国务院机构改革的议案,成立了国家医保局。国家医保局拥有城镇职工和城镇居民基本医保、生育保险职责,新农合医疗职责,医疗救助职责与药品和医疗服务价格管理职责,表明了我国对医疗保障及医药价格改革的重视。文章将通过对英国药品报销制度、价值定价理念的介绍,理顺药品价值评估、药品再评价制度、医保目录准入及报销价格制定间的关系,为我国的医疗保障改革提出建议。
1 价值定价理念的发展 1.1 英国早期价格管理方法英国几乎所有药品的费用全部由政府买单,国家医疗服务体系(National Health Service,NHS)根据社区药房协议框架(the community pharmacy contractual framework)向协议药房(Pharmacy Contractors)购买药品服务[1],从医疗保险的角度进行解读,即英国绝大部分药品的报销比例为100%。因此进行英国目录准入、药品定价的研究从一定意义上等同于对其药品医保准入及医保支付标准/价格的探索。20世纪50年代英国实行的是药品价格直接规制法,在后来的发展与探索过程中转为对药品实行利润管控的方式。[2]
1.2 药品价格管制方案的发展——利润控制导向1957年英国政府为控制药品价格、减轻患者用药负担,出台志愿药价管制方案(Voluntary Price Regulation Scheme, VPRS)对药品价格进行直接管控;1969年,对药品费用的控制重点逐渐向利润管控方面转移;1978年VPRS正式更名为药品价格管制方案(Pharmaceutical Price Regulation Scheme, PPRS)[3],对品牌处方药进行利润①控制。英国国家医疗服务体系(NHS)规定利润率上限为17%~21%,具体由卫生部根据药品的创新程度、企业经营状况,并参考制药行业协会(ABPI)与制药公司代表的协商结果共同决定。
① 利润=药房采购价—NHS报销价(即NHS补偿价)。
1.3 药品价格管制方案的实施绩效在利润管制规则下,自1999年开始,英国药品价格年均下降4.5%[4],对药品价格起到了一定的管控作用。但1967—1997年NHS的药品费用支出却上涨了近10%,药品企业年终返利总额只占销售额的0.01%;大量药品涌向市场,NHS忽略了对药品价值的关注。[5]
专利药在药品价格管制方案(PPRS)下实行利润限制、非专利药又实行最高限价,最终依据《药品价格目录》从国家医疗服务体系(NHS)进行报销,这样单纯以控费为目的的定价方式掣肘了英国的医药创新进程,未考虑药品实际价值和功效、未引入药品评价机制导致创新动力不足,新药的研发效率迟缓。[6]
1.4 药品价值定价理念的发展——价值评估导向英国的药品定价机制在1997年进行整改后就已显示出强大作用,尤其值得我们借鉴。1997年10月,英国成立国立临床规范研究所(NICE),主要负责药物的经济学评价。但同时英国认为新药价格加成的激励作用也微不足道,价值定价将会在加权质量调整生命年(weighted QALY)的比较之下更全面、客观地凸显真正优秀的产品,促进药品研发和创新。
因此,英国开始探索价值定价(Value-Based Pricing, VBP)机制。有学者称,以价值为导向的药品价格改革可以使NHS节省5亿英镑的药品费用开支。2010年12月,英国出台了新定价方法征求意见稿,规定自2014年起开始执行基于药品价值评价的新定价机制,改善了药品的评估程序、发展高价值目录药品,重视临床疗效和成本效益。其基于的是对技术的预期效益评估,利用药物警戒系统(pharmacovigilance)进行上市后再评价以证明更高的价格会有更高的回报,主要原则有三:(1)确保NHS基金能给患者带来最大可能的价值;(2)设定药品基于意愿支付定价的阈值和可报销阈值;(3)对药品的成本、功效和设定的阈值进行再评价以做调整。这种新的定价方式对新药的影响力最为突出,NHS将不会再利用其垄断力量削弱药品的专利保护市场,开始重点强调药品的社会价值。
2 英国VBP理念中价值的内涵药品价值包括临床疗效、安全性、存活率、质量调整生命年的增量、药物依从性几个方面。[7]英国的价值定价(VBP)理念实际上融合了定价和补偿两方面内容,价值评估(Value-Based Assessment, VBA)完成后所制定的药品价格实际上就是其“医保支付价”,通过短期和长期的报销价补充效应给予药品企业以合理的回报。[8]
英国的《The Pharmaceutical Price Regulation Scheme 2014》和《Value-based pricing for pharmaceuticals: Its role, specification and prospects in a newly devolved NHS》官方文件中,以法规的形式明确了价值定价机制的基础理论为广义的药物经济学,对价值优势的再评价过程中主要考量药品的临床疗效、患者需求度、创新性、上市后改进情况、疾病负担和社会效益等方面[9-10],重视药品的临床价值评估,使药品反映临床和治疗价值、对患者的价值、对NHS的价值。并提出从医患双方角度考察药品功效的新思路,以更全面地测绘质量调整生命年(quality-adjusted life years,QALYs)和增量成本效果比(incremental cost-effectiveness ratios,ICERs)。
近期,英国又对价值的定义有了新的倾向性,认为价值的测算指标不仅局限在单一的成本—效果上,对于社会价值的开发也应当纳入进去。比如对于社会生产力的提高、对医药创新的启示与铺垫和对企业的激励作用等。
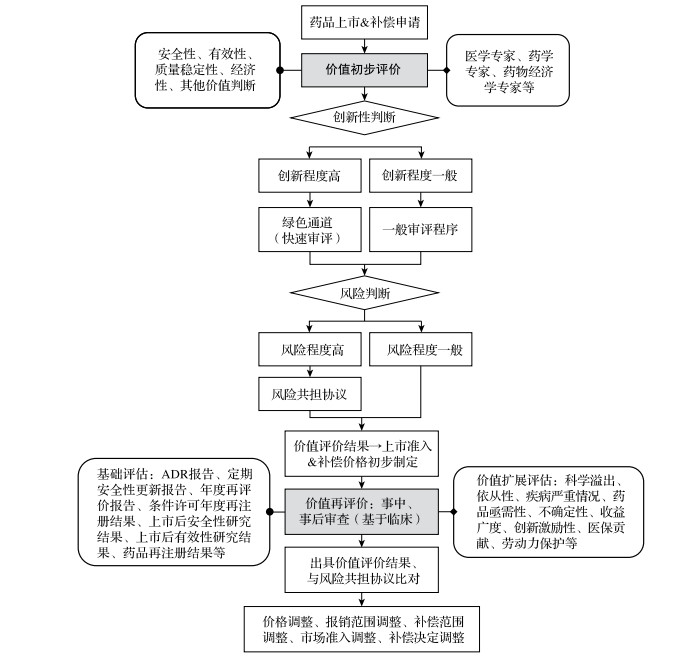
3 英国价值定价理念在药品报销政策中的具体实践 3.1 价值定价理念在报销目录遴选流程中的应用自药品企业申请进入NHS国家药品补偿系统,国立临床规范研究所(NICE)组织医学专家、药学专家、药物经济学专家等对药品的价值进行审查,创新性强的药品则会开启绿色审评通道如进行快速评价,对药品的综合价值优先评估并决定报销补偿政策(图 2)。部分创新程度高、用药风险大的药品企业要与政府签订风险共担协议,以对其药品的成本—效果作出保证。成本—效果的计算公式如下[11]:

|
|
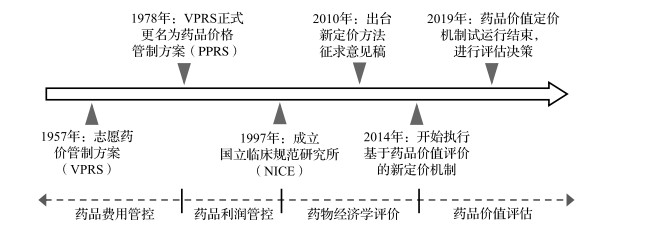
图 1 英国价值定价理念的发展 |
|
图 2 VBP与英国报销目录动态准入的衔接机制 |
成本—效果及价值评价结论将作为药品补偿价格确定的主要依据,通过对临床试验的回顾、价值的评定以及临床价值的预测制定最终的药品价格。对于不同症状、不同适应人群的不同价值评估结果,即使是同一药品也采取非线性定价方式。此外对于仿制药品应当进行生物等效性评估并确保价值等同。
药品一旦允许上市并进入报销系统后,NICE将对其进行事中和事后审查,通过对药品采取再评估和滚动评估,确定药品的临床信息,评价药品的临床价值。临床价值的重新认定和调整将影响药品报销价格的调整。
以上通过价值评估进行药品市场准入和补偿价格确定的过程即为价值定价(VBP)理念的运用。随着卫生经济学和医疗技术评估的发展,人们意识到QALY等效果或效用评价方法无法完全反映药品的价值,尤其是临床感受和用药过程。因此,药品价值的评估范围扩展至疾病负担、科学溢出效应、劳动生产力的改善、不确定性的减少等。[12]
3.2 VBP理念在药品价值测算中的应用和最终效益评估 3.2.1 VBP的测算指标VBP应用于报销决策时,现在为止英国政府仍以QALY = length of life × quality of life为测量单位,以ICERs=(C_sample-C_standard)/(E_sample-E_standard)为评估指标,设定报销阈值。NICE和苏格兰指南表示倾向于使用Euro Qol-5D①量表收集患者的健康状况,使用从一般人群调查得出的时间权衡法(TTO)应用效用权重。
① 欧洲五维健康量表(EQ-5D),用来测量健康效用,间接表示药品使用后的健康产出或改善。
3.2.2 VBP依托药品再评价与非线性报销政策的衔接英国药品报销时,价格和药品用量是非线性的,不同处方量的药品可以设定不同的报销价格,效果最优的剂量会给予其最高报销优惠。[13]同时此理论也是药品上市后再评价与量价调整的根本依据,随着药品市场上价格的浮动,再评价的结论将通过非线性报销政策对药品报销的覆盖范围产生影响。
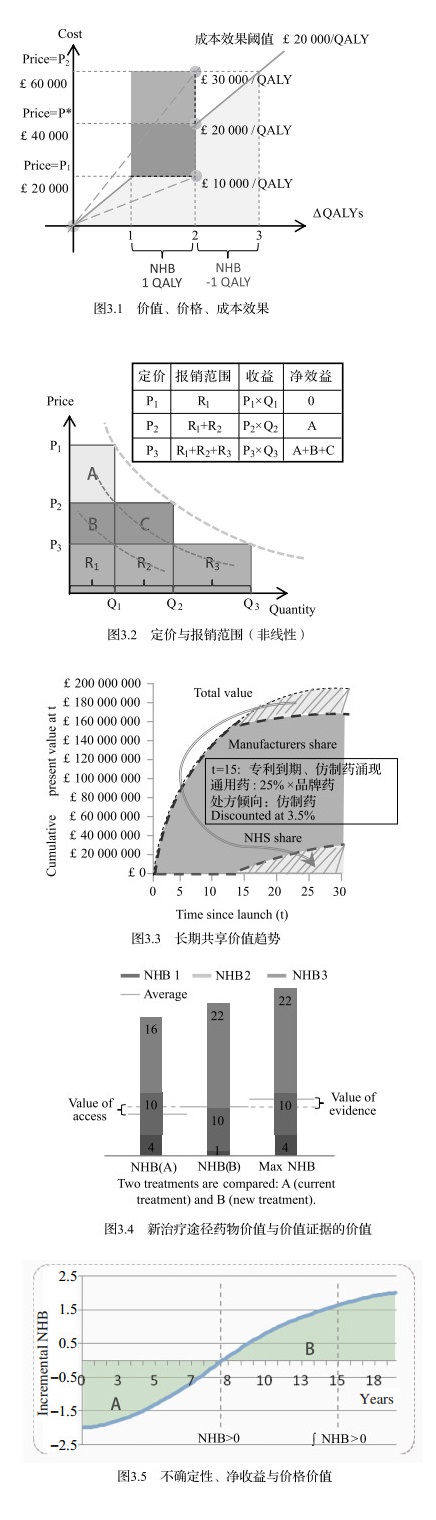
NICE设定了意愿支付“门槛”,约20 000~30 000£/ QALY。如图 3.1所示,假设新药品可提供2个单位QALY,测定出的阈值为£20 000/QALY,若报销价格设定为P1,那么根据NICE采用的成本效用阈值,额外的20 000英镑NHS成本预计将在其他地方产出1 QALY的价值。因此,以P1的价格,该技术为NHS提供净健康益处(预计将具有较高成本-效用)。在更高的价格下:当价格相当于P*时,健康结果的预期收益被NHS上涨的成本抵消(40 000英镑),净效益为零。P*代表基于价值(利益)的价格,如果NHS支出超过P*(例如P2),该技术将会损害整体效益。所以由于NICE非线性的报销范围和优惠政策会产生图 3.2的结果,价格较高如P1时,使用量为Q1,总成本与总效益均为R1×P1(= Q1×P1),净价值为零;当专利过期,价格稍降低时如P2,使用量达到Q2,收益为P2×Q2、总效益为P1×R1+P2×R2,从R1处获得净效益为A;同理,仿制药大量涌入市场时,价格低至P3,从R1、R2处获得净效益为A+B+C。[14]
|
注:NHB:净健康收益;NHS:英国国民健康保险制度;Discount:此处指折现率;图 3.3假设药品专利到期后(t=15)原研药降价幅度大至与仿制药价格差别不大。 数据来源:https://www.york.ac.uk/media/che/documents/papers/researchpapers/CHERP60_value_based_pricing_for_ pharmaceuticals.pdf. 图 3 再评价与价值定价、社会收益 |
已经报销的药品,英国会通过药物警戒系统对其持续进行再评估以调整药品的价格、阈值,并通过临床核查对成本—效果等确定指标进行打分,反映药品的真实价值。同时,在测算药品价值与价格的基础上,对基金支出作出动态调整。若其真实价值严重偏离预期,则直接剔除报销目录或责令撤市。
癌症药物被NICE接受的ICERs阈值高于其他药物。此外,对于无治疗—预期寿命短(< 24个月)、治疗延长中位寿命至少3个月、获得治疗许可的患者人口数小的药品,尽管没有预先规定的阈值,但如果确无更优秀的替代品和临床的亟待需求,治疗药品同样会得到一定的资助。实证工作表明,根据疾病面积分析图(Claxton 2011),NHS目前的消费额约为7 000~26 000英镑/QALY(Claxton 2011),由于NICE批准高价新药,对于其他药品而言NHS支出的平均下降幅度约为13 000£,即将导致1个QALY的损失(Claxton 2013)。可以看出,其他一般药物支出的下降和高价的新药报销之间在努力形成一个稳定的动态平衡以维持NHS的正常运行。
3.2.4 药物警戒背景下VBP与报销政策的最终总效益经过再评价进入报销目录后,高价的创新药可能最初给报销部门带来的效益是负的,但是一旦专利到期、新药使用范围得以扩散后,得到的效益将是正的,仿制药上市后,后期的效益将会弥补前期损失并使最终的净效益为正。如图 3.3,其显示了创新随时间的累积价值(采用3.5%的折现率)以及制造商与医疗保健系统之间共享价值的累积值。最初,在VBP的专利保护期间(对于单一适应症和无其他可识别亚组适应症患者),基本所有价值都由制造商享用。一旦产品专利到期,竞争性仿制药进入,该产品的市场价格将下降。假设:(1)竞争性仿制药价格降低到品牌药的25%;(2)所有处方几乎都转为仿制药(和/或品牌药价格大大降低);(3)任何新的专利药物将参考通用药品版本定价。在产品推出8年前后,医疗保健系统将开始受益于创新,并开始与制造商分享创新产生的部分价值,如图 3.5,在Years=15时,B部分面积将可抵消掉A,净效益为正。然而,即使从长远来看,制造商仍将保留大部分的回报价值。在这个例子中,30年来,制造商将占用所有价值的72%,即使在无限的时间范围内,它仍然保留57%。因为新药更广泛的经济效益(Claxton 2011)还可能包括对患者的直接成本和社会收益的影响,如无薪照顾者的时间、病人的自付费用、更快的返回工作、失去的休息时间;对经济其他部分的间接外部影响(成本和收益),如生产力提升,所以长期来看,这项政策应有利于英国和全球的经济增长,更大的经济增长(理论上)提供了增加税收以支付更高价格药物的财政能力。
当然,如果上述三个假设中的任何一个均不成立,那么制造商的利润份额将会更高(且NHS的份额会降低),即可能实际情况中的成本效用没有达到预期效果或厂商执意不进行降价,则政府会产生纯损失,若欲将损失减小到极致,就离不开基于药物警戒的滚动式再评价,并在发现问题后及时将药品撤出报销目录。
3.2.5 VBP中对价值定义与评价指标的扩展在一系列的指标评价过程中,英国所指的价值除了包括通过药物经济学测算的成本-效果指标,还可能包括创新附加值(包括药品的期望收益、创新和区位激励效果、革新程度和未满足的需求),疾病严重性、负担和亟需性,经济收益的广度(恰当评估机会成本、平衡替代药品的价值、对实际价值的质证),不确定性、治疗依据和投资情况(准入价值和附加证据价值的关系、价格与附加证据价值的关系、投资及不确定性与价格的关系)等。这一系列指标的纳入将会对上市后药品意愿支付阈值(ICERs阈值)的调整产生影响。
因此,具有广泛价值不单单等于成本—效果优势的显著,如下文的图 3.4中举例,平均而言,新技术的净健康效益(NHB(B)= 11)预计将大于目前的治疗水平(NHB(A)= 10),所以以现在的价格提早获得新技术预计可以为每位病人提供1个额外的QALY。然而,这种评估是不确定的,且有可能新治疗药品并不具有成本—效益。如果可以获得更多的证据来解决这种不确定性,那么可以做出更好的决策,从而提高净健康效益(最大NHB = 12,如最后一栏所示)。因此,附加证据价值的上限是与不确定性得以解决的最佳方法之间的差异,即每个患者1 QALY。因此,有关新技术和表现有效技术的证据是同样有价值的。[15]附加证据越充分,测算药品价值的可信度就越高,报销决策也就越能得到保证,获得预计产出的可能性也就相应越大(风险越小),社会总收益受到损失的可能性越小。
在这样的背景下,单一的QALY值无法满足价值的测算,因此英国选择对QALY加权,QALY将针对特定于药物的VBP属性进行调整(如更广泛的社会效益)。如在疾病负担被认为更严重的地区获得的收益可以赋予更大比例的权重或罕用药(孤儿药)可能被认为更具社会价值。基本阈值也会在赋予权重的基础上做出微调。
英国主要选择在疾病负担(Burden of Illness,BOI)和广泛社会效益(Wider Social Benefits,WSB)上进行权重赋加。Brazier更倾向于将BOI作为考虑因素。公式为Adjusted cost / QALY threshold in population“X” = basic threshold ×(1 + BOIx)/(1 + average BOI),X表示药品针对的疾病种类。例如,肾癌的BOI权重约为19%,阈值设为25 000,替代疾病治疗的平均BOI权重为7%,则调整后阈值为25 000×1.1896/1.07 = 27 794£/QALY(Boyson 2013)。最终的VBP价格最大值(Maximum VBP price)即为获得的QALY收益(QALY gain)×调整后的ICERs阈值(Adjusted cost per QALY threshold)。[16]其他疾病阈值的调整如表 1所示。
| 表 1 BOI权重对阈值的影响(举例) |
有学者认为可以对不同适应症设置单一价格以显示真正价值的加权运算结果,经过政府的研究讨论,决定对不同疾病患者给予药品不同的报销价格来解决同一药品不同适应症产生不同效果的情形,以公正价值定价原则,但是需要一个复杂的监控系统推动政策的运行,目前仍在探索当中。
4 英国经验对中国的启示 4.1 理念层面英国在药品的定价方面考虑药品实际价值和功效,关注药品的临床疗效和成本效益,并且扩展药品价值内涵,重视药品的临床价值、经济性价值、社会价值等。英国通过基于价值定价(VBP)理念将药品的市场准入、补偿决定、价格制定、上市后再评估、报销范畴及价格的调整紧密联系起来,使得英国的上市药品在安全性、有效性、临床价值、经济性等诸多方面得到可靠保证,造福患者。当前我国虽然也在探索基于价值的付费方式,但是更多还是关注药品数量和价格本身。建议我国提高在医保基金使用的效率和提升购买服务内在价值层面,借鉴英国这种将价值定价理念融入各环节的做法,使医保购买服务的价格更贴近于服务实际价值本身,增加基金的使用效率,让真正有价值的药品与医疗造福患者,让医保基金的花费更加“有所值”。对于药品价格的形成过程中,真正基于其实际的临床价值、经济性价值与社会价值进行全方位考虑,确保药品的安全性、有效性和经济性。
4.2 制度设计层面英国在制度设计方面,首先对申请上市或补偿的药品进行基础性的安全性、有效性、质量稳定性、经济性、其他价值判断,再利用药物经济学判断药品的创新性与风险,对药品价值的评价更加中肯、全面、客观。根据价值评价结果初步制定补偿价格。药品允许上市并进入报销系统后,英国将对其进行事中和事后审查,通过药物警戒系统对其持续进行再评估确定药品的真实价值,并且根据价值评价结果进行价格调整、报销范围调整、补偿范围调整、市场准入调整、补偿决定调整。同时对基金支出作出动态调整。若其真实价值严重偏离预期,则会有被剔除报销目录或责令撤市的风险。
我国应当在医保制度改革中,进一步完善药品的评价标准及方式,优化医保目录的准入原则和支付标准的制定过程,使药品评价结果反映临床真实情况,以药品价值评估结果为依据进行医保准入及支付标准(价格)的决策。同时,进一步完善药物警戒与再评价制度,对于药品进行持续性的评估与监控,得到药品真实的临床价值,并及时调整医保目录和报销价格。再评价安全性方面需统计不良反应发生率及严重程度、不良事件报告率及缘由、药品相互作用、定期安全性更新报告及临床Ⅳ期试验研究报告。有效性方面需考察临床研究、药品有效率、可替代性等方面。进入目录的药品根据再评价结果进行相应的调整:临床价值高并与预期吻合甚至高于预期的药品继续留在目录中,维持原支付价格;真实价值低于预期但与其他药品相比仍具有优势,下调支付价格后继续留在目录内;临床真实价值远低于预期或存在严重偏离要求的药品及时调出医保目录;存在安全性、有效性或质量方面严重风险的品种在剔除医保目录的同时进行撤市处理。
4.3 管理机构层面英国专门设置国立临床规范研究所(NICE),对申请药品进行经济学评价。NICE组织医学专家、药学专家、药物经济学专家等对药品的价值进行审查,同国立卫生研究院决定药品能否进入补偿范围,并给出推荐报销、可优化后报销、限制使用、仅在研究中使用和不推荐使用5种建议。英国NHS将根据NICE的建议做出药品报销与价格决策。NICE依据英国药物警戒系统,如不良反应报告、定期安全性更新报告、年度再评价报告等,对药品价格、报销目录与基金支出进行微调。
对于我国,也应当建立专门的药品价值与经济性评价机构。通过组织专家对药品安全性、有效性、经济性的综合性评价,评价药品的真正临床价值,并建立基于价值的药品价格形成与支付机制。同时利用药物警戒系统对药品的临床价值进行持续的追踪监测,根据持续评价的结果动态调整医保目录与目录中药品的支付价格。这方面同时需要医疗机构与医药企业的配合,提交日常的药品不良反应报告、Ⅳ期临床试验研究报告等信息,使得真实世界中药品的使用情况和实际临床效果得到科学地反映,让真正有价值的药品服务临床诊疗需要。
4.4 技术层面英国在药品价格定价方面,运用了众多药物经济学的评价方法,全方位、多角度地评估药品价值,如以质量调整生命年QALY为测量单位,以和增量成本—效用比ICERs为评估指标。客观公正的评价方法不仅使得医保基金的运行平稳可持续,同时也激励当地药品企业进行持续创新研发,通过研发创新性强、安全有效的药品获取利润和政府的补偿。对于我国,应当继续探索药物经济学评价的方法和内涵,通过学习与借鉴英国的经验发展我国药品评价环节中的药物经济学评价方法、医药技术评估方法等,尝试在卫生技术评估(HTA)的基础上通过权重的赋予和成本效益的调整等更科学地评估药品价值,以使真正安全有效、创新程度高、临床应用前景广阔、社会效益突出的药品进入国家基本药物目录和国家医保目录,保障患者用药权益、提高患者的健康效益。
作者声明本文无实际或潜在的利益冲突。
| [1] |
苏红. 英国、德国和瑞士的药品价格管控体系分析[J]. 药学与临床研究, 2016, 24(5): 353-356. |
| [2] |
Sedgley M D. An analysis of the governmentindustry relationship in the British pharmaceutical price regulation scheme[EB/OL]. http://etheses.lse.ac.uk/2300/1/U615247.pdf
|
| [3] |
陈文, 胡善联. 英国药品价格管制政策[J]. 卫生经济研究, 1997(7): 46-47. |
| [4] |
常以, 黄泰康. 英、德、日药品价格管制经验及其对我国的启示[J]. 价格月刊, 2013(8): 22-25. |
| [5] |
刘志民. 走在降价路上的英国医药产业[J]. 中药研究与信息, 2003, 5(2): 8-12. |
| [6] |
郭朗, 孙利华. 英国药品定价方法的调整趋势及对我国的启示[J]. 中国药房, 2012, 23(40): 3772-3774. |
| [7] |
胡善联. 国内外药品价格和费用控制政策的比较研究[J]. 中国药房, 2013, 24(44): 4129-4132. |
| [8] |
常峰, 罗修英, 崔鹏磊. 典型国家基于价值的新药定价机制及对我国的启示[J]. 中国新药杂志, 2015, 24(18): 2047-2051. |
| [9] |
DH. Pharmaceutical Price Regulation Scheme 2014[OB/OL]. (2013-12-03)[2018-01-03]. https://www.gov.uk/pharmaceutical-price-regulation-scheme
|
| [10] |
DH. The Pharmaceutical Price Regulation Scheme Twelfth Report to Parliament[EB/OL]. (2014-04-03)[2017-12-23]. https://www.gov.uk/government/uploads/system/uploads/attachment_data/file/300301/PPRS_Twelfth_Report_to_Parliament_Final.pdf
|
| [11] |
朱莉莎, 颜建周, 张伶俐, 等. 英国、比利时罕用药医保准入机制及其对我国的启示[J]. 卫生经济研究, 2016(8): 48-51. |
| [12] |
Louis P. Garrison Jr., Adrian Towse. Value-Based Pricing and Reimbursement in Personalised Healthcare: Introduction to the Basic Health Economics[J]. Journal of Personalized Medicine, 2017(7): 1-10.
|
| [13] |
茅鸯对, 常峰. 英国药品价值定价机制研究[J]. 上海医药, 2013, 34(19): 32-35. |
| [14] |
唐艳, 徐怀伏. 利润控制或价值导向定价?——英国药品价格政策的改革[J]. 中国药物经济学, 2008(3): 57-61. |
| [15] |
Karl Claxton, Mark Sculpher, Stuart Carroll. Value-based pricing for pharmaceu-ticals: Its role, specification and prospects in a newly devolved NHS[EB/OL].[2017-12-26].https://www.york.ac.uk/media/che/documents/papers/researchpapers/CHERP60_value_ba-sed_pricing_for_pharmaceuticals.pdf
|
| [16] |
David Epstein. Value Based Pricing of new pharmaceuticals in the United Kingdom National Health Service[EB/OL]. (2014-01-11)[2017-12-19] Value-Based Pricing in the UK, 2014-11-11/2017-04-30.http://www.ugr.es/~davidepstein/
|
(编辑 薛云)





