2. 中国人民大学卫生技术评估与医药政策研究中心 北京 100872
2. Health Technology Assessment and Policy Evaluation Group of Renmin University of China, Beijing 100872, China
目前我国正在进行一系列改革探索,将建立常态化、动态化的医保药品准入机制作为改革的重要举措,强调做好目录准入、支付标准、使用管理等环节的有机衔接,逐步实现药品在医保中的全流程、全周期管理,使保障范围与临床用药实际、医药技术进步相适应。从长远看,是实现医保药品目录动态调整的制度化。我国医保药品管理改革取得显著成效的同时也面临着未来发展方向的问题。日本与我国同属亚洲国家,其在药价管理上的一些做法值得我们探讨学习。20世纪70年代,药品支出在日本整体卫生支出中的占比普遍接近40%,而随着80年代开始的药品管理相关措施,这一比重一路从1980年的38.2%降低到2000年的20.2%,此后一直维持在21%~22%左右水平。本文将通过介绍和分析日本药品医保管理制度的做法和经验,为我国药品医保管理的政策制定者提供一些新的思路,以期探索符合我国国情的药品价格和医保药品目录管理模式。
1 日本的医疗卫生体系2018年日本实现GDP约4.97万亿美元,位居世界第三,人均GDP达到48 919.6美元。[1]在世界卫生组织(WHO)多次在世界卫生报告发布的全球医疗水平评比中,日本以“高品质的医疗服务”和“医疗负担的低水平程度”及“国民平均寿命高”等成就连续多年稳居第一。[2]日本所有医院均为非营利性,禁止营利性医院经营。[3]从国民医疗负担水平看,早在20世纪50年代,日本就已建立起全民医保制度。日本通过全民保险制度实现了世界最高水平的平均寿命和医疗保健水平,在20世纪80年代人均寿命就已达到全球第一位。2018年日本人均总体预期寿命为84.6岁,其中男性平均寿命为81.7岁,女性为87.26岁,均比30年前延长了5年左右,婴儿死亡率为1.7‰,在所有OECD国家中最低[4],每千人口医生数为2.4,每千人口护士数为11.3,每千人口床位数为13.1,实现了较高水平的医疗服务可及性。2018年卫生总费用占GDP的比重为10.9%,药品支出占卫生支出比例约为21%。
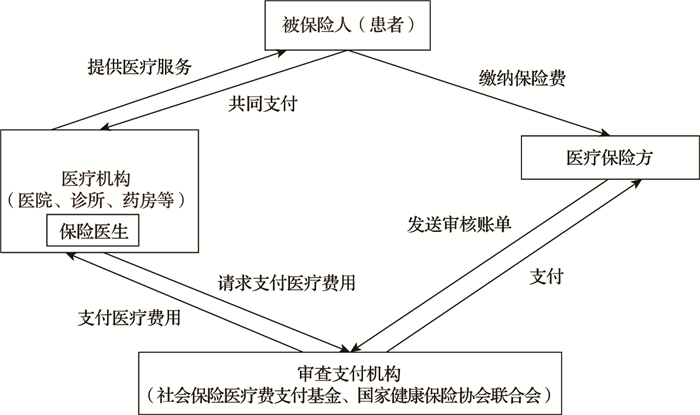
日本的医疗保险虽然由厚生劳动省(Ministry of Health, Labour and Welfare,MHLW)下属的医疗保险局统一管理,但具体的保险种类则根据被保险人的职业类型划分:(1)普通企业员工一般加入健康保险(Health Insurance);(2)私营业主和自由职业者以及企业退休员工参保国民健康保险(National Health Insurance,NHI);(3)国家或地方公务员、私立学校教师等加入共济组合(Mutual aid associations);(4)75岁及以上老年人一般参保市村町国保;(5)船员及其家属参加的海员保险。健康保险和国民健康保险为两种最主要的保险形式,覆盖了90%的日本民众。[5-6]日本医疗保险的筹资主要有两大来源:一是保险费,二是国家和地方政府的财政补贴。考虑到给付公平性问题,日本医疗保险的报销比例仅根据年收入加以区别,主要分为以下四档:义务教育就学前(未满6岁)的参保人,报销80%;入学后(6岁)到69岁,报销70%;70~74岁,报销80%,如年课税所得在145万日元(8.7万人民币)以上,则报销70%;75岁以上,报销90%,如年课税所得在145万日元(8.7万人民币)以上,则报销70%。日本实行先就医、后付费的制度[7],具体支付体系见图 1。
|
图 1 日本医疗保险支付体系 |
近年来,由于少子化和老龄化问题的加剧,日本面临着卫生费用急剧上涨的压力。卫生总费用占GDP的比重从1998年的6.6%上升到2018年的10.9%。医疗保障支出也呈现快速增长趋势,2018年,医疗保障支出约为42.6万亿日元(2.8万亿人民币),占GDP的8.3%,而10年前仅为6.4%。卫生费用增长的主要原因是人口老龄化和卫生保健技术(例如先进医疗设备和新的药物)的发展。自1958年全民医保的药品和医疗服务价格体系建立以来,药品定价工作一直由厚生劳动省统一负责,政府对所有纳入医疗保险目录的药品进行定价。如前所述,日本药品支出占比在20世纪70年代已普遍接近40%,而随着80年代厚生劳动省开始对医保目录内药品进行两年一次的价格调查与调整,医疗机构的药品进销价差不断得到缩减。此外,自1974年开始的医药分业也在强制推行中切断了医院、医生与药企的利益关系,医疗服务价格不断提升,药品加成在医院和医生收入中占比也不断下降。日本如何实现药品价格管理及如何维持较低水平的药品支出是本文要探究的主要问题。
2.1 药价形成相关主体与流程日本将药品大致分为两类:一类是医疗用药,其中绝大部分是处方药,另一类则是非处方药。与世界上绝大部分国家一样,日本政府只干涉前者价格,厚生劳动省作为主要的卫生行政部门,确定处方药在全国范围内统一的价格,并将几乎所有处方药纳入医保报销系统。由政府确定的上市价格也即医保支付价,药品定价的过程也即该药进入医保目录的过程。但同时,日本的药品价格体系又具有政府定价与市场定价相结合的特征,政府确定上市价格与医保报销价格,但实际的市场交易价格由医疗机构和药品厂商通过磋商自行确定。
在进行定价与医保准入之前,新药与仿制药都必须经过上市的审评审批。对于新药,通过再审查弥补上市前药效信息与上市后临床复杂使用间的差距。对于仿制药,日本通过药品品质再评价工程(药效再评价和品质再评价)对仿制药质量进行双重保障。1971年至今共进行了三次药效再评价,第一次再评价(1971—1978)、第二次再评价(1984—1989)和新再评价(1989—至今,成为对新上市的所有处方药进行常态再评价)。品质再评价即通过全面、细致、严格的体外溶出度试验对药品的内在品质进行评估。[8]
日本新药价格管理的参与主体包括厚生劳动省、制造商/市场授权持有人、医学、药学和医药经济学相关专家以及中央社会保险医疗委员会(Chuikyo)。Chuikyo由来自各方的代表组成,包括保险者代表、被保险者代表和医药企业代表委员8名,医师、牙科医师和药剂师代表委员8名,公众利益代表委员4名及数名其他专业委员。仿制药价格管理主体和流程与新药类似,但在具体定价方法上有所不同(具体在下节展开)。
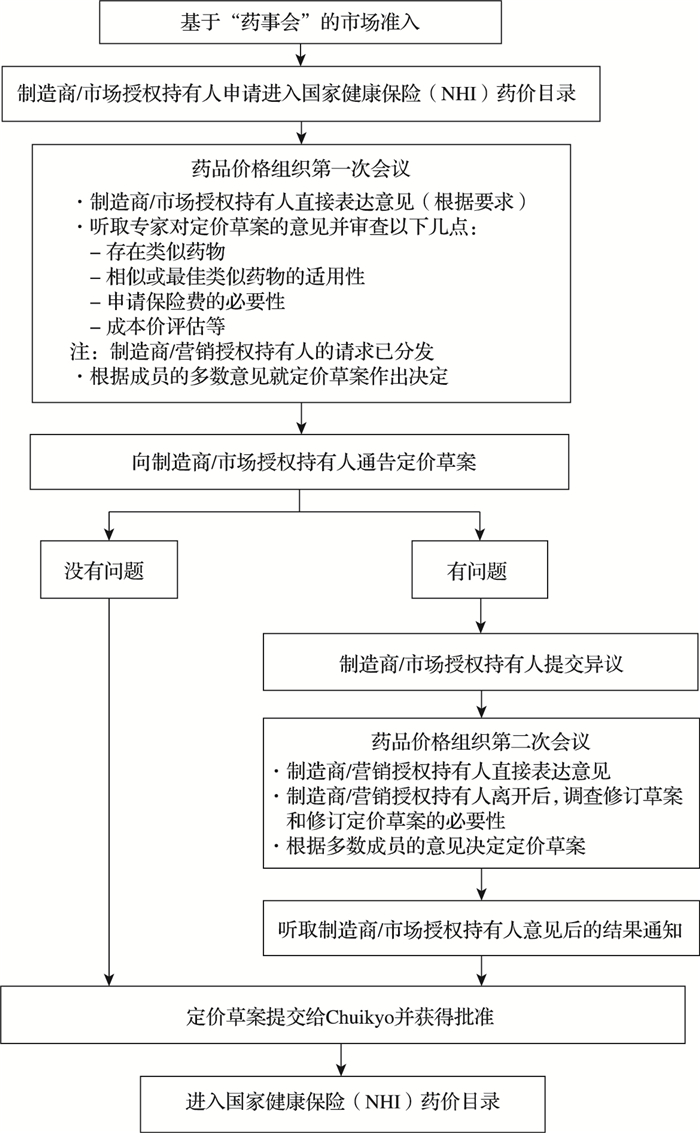
经过上市审批进入市场的新药,由制造商或市场授权持有人提交医保目录准入申请。[9]厚生劳动省下属医政局经济课是主要的药品价格管理部门,负责医药品价格调查和特定保险医疗材料价格调查等事务,包括组织第一次药品价格会议。在第一次会议上,首先由医政局经济课报告其研究提出的定价草案,制造商/市场授权持有人直接表达意见(根据要求),医学、药学和医药经济学专家发表对定价草案的意见并审查以下几点:是否存在类似药物、申请保险费的必要性、成本价评估等。[10]医政局经济课则根据多数成员的意见就原定价草案进行修改,确定最终定价草案并提交Chuikyo以及告知制造商或市场授权持有人。如果制药企业不接受厚生劳动省计算的价格,可以向Chuikyo提交一次复议申请进行药品价格第二次会议。Chuikyo下设的药价算定组织根据医政局经济课拟定的药价及核价原则,对申请药品进行核查,参照代表成员的多数意见,再次讨论并核定药价,告知制造商或市场授权持有人后再次提交给Chuikyo。Chuikyo对计算出的定价草案进行批准。[11-12]具体定价流程如图 2所示。
|
图 2 日本药品定价流程 |
新药每年有四次机会进入NHI药价目录,分别为2月、5月、8月和11月,与《药品管理法》规定的审批时间相对应,新药进入药价目录的时间原则上为批准后60天内,最迟90天内。仿制药进入药价目录的频率在1994年前为每两年一次,1994年起改为每年一次,自2008年起调整为每年两次。
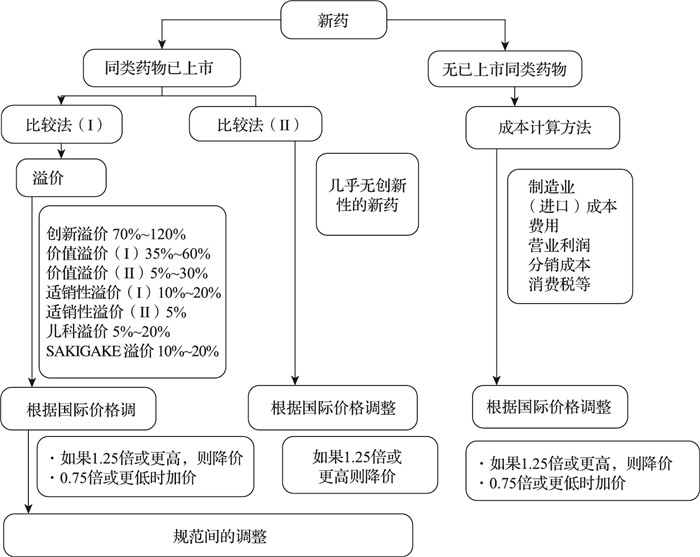
2.2 药价形成方法 2.2.1 新药价格形成方法根据1961年日本《药事法》(Pharmaceutical Affairs Law, PAL)的规定,新药的官方定价主要采用类似药比较法和成本核算法,此外国际参考定价也是新药定价的重要组成部分,但并不单独使用[8],三者构成了日本的定价方法体系(图 3)。
|
图 3 日本新药定价方法 |
当需要对一种新药进行定价时,如已有类似的收录药品,采用类似药比较法来核定新药的价格。如功效、药理特性、组成与化学结构、应用途径、制剂种类、剂型以及给药方式均相同,则新药的价格与已有药品价格相同以保证公平的市场竞争。[13]如果一种新药被评为创新药物,厚生劳动省会增加一个溢价。药品的创新程度根据以下四点判断:(1)新的作用机制;(2)更高的疗效或安全性;(3)改善目标疾病的治疗;(4)有益的药物配方。溢价的比例取决于创新的程度,可以获得5%~120%的溢价。此外,如果一种新药根据PAL定义为孤儿药或者小市场药物或在儿童(包括婴儿、哺乳期婴儿、新生儿和低出生体重儿)中具有使用潜力;又被定义为创新靶向药物,则都可以获得一定比例的溢价。
如果没有合适的类似药作比较,则采用成本计算方法。成本是通过生产、管理、营销、利润和增值税的成本加起来计算的,包括原料费、人工费、销售费、研发费用、营业利润和税收等。截至2016财年,营业利润率定为14.6%,这是所有行业的平均利润率。但基于药物的创新性、功效和安全性,其利润率可基于标准利润率进行调整(最高再上升100%,最低降至50%)。
此外,通过以上方式定价后还需要与国外同等药品价格进行比较。日本药品国际参考定价系统较为复杂,包括国际参考定价的品种、参考国家的确定、参考价格的获取,参考价格计算方法和药品价格调整方式涉及多方面内容[14-15]:(1)日本对于国际参考药品的选取原则做了明确规定,参考药品必须是与该新药的成分及剂型都相同,或规格和适用范围与该新药最相似,且收载于参考国家相关药物价格目录中的药品。(2)日本根据经济发展水平、汇率波动、市场规模等因素,选取了美国、英国、德国和法国4个国家作为参考国。(3)日本参考的主要是参考国公开的药品价格目录上的零售价格。(4)日本主要采用美、英、德、法药品零售价格的算术平均值来确定国际药品的平均价格水平。(5)在得到国际参考药品的平均价格后,需要利用国际价格调整本国的药品价格。[16]当新药计算的价格大于国际价格1.5倍时,要进行降价调整。值得注意的是,日本从2019年4月开始引入基于卫生技术评估的新药价格调整机制,将在下文重点阐述。
2.2.2 仿制药价格形成方法日本仿制药主要按照原研药价格的一定比例进行确定。根据2016年药价改革要求,从2021年开始,新进入医保的仿制药价格从之前原研药的60%(超过10个品种的口服制剂是50%)下调到原研药的50%(超过10个品种的口服制剂是40%),生物类似药维持原研药价格的70%(超过10个品种的口服制剂是60%)。当已有同类仿制药列入药品目录时,新进仿制药价格应与已有仿制药最低价格持平。[17]此前,为鼓励仿制药使用,日本从品质监管和医保支付两方面对仿制药进行推广和使用,包括2002年开始的药店交付仿制药可以获得额外加成,更改处方样式将仿制药选择权交给药店和患者,2007年将“促进仿制药使用”作为国策写入改革纲领等。2005年日本仿制药占市场比例为32.5%,2017年这一比例达到65.1%,2020年的目标是80%。
2.3 药价调整与再定价新药由厚生劳动省确定价格后即进入医保目录,药品采购方与经销商被允许通过二次议价以低于医保支付价的单价购入且结余可以留用。政府则在一定周期内(原为两年一次,2021年开始为每年一次)基于价格调查(drug price survey)获取的真实市场信息对目录内药品进行价格调整。[19]价格调查由Chuikyo主导,调查对象为药品经销商和按一定比例选定的医疗机构,调查内容主要是目录中的所有项目(现约16 000个项目)的真实价格信息。除价格信息外,价格调整还需要依靠具体公式,包括1953年的90%百分位点法(90%Bulk line)、1982年的81%百分位点法(81%Bulk line)以及1992年以来的合理区间法(Reasonable Zone)。[20]合理区间法即新的报销价格等于计算出的加权平均市场价格加上当前报销价格的一定百分比(自2000年至今比例为2%)。与百分位法相比,合理区间法更能准确地反映市场价格,纠正价格的非自然波动。此外,对药品价格的调整还包括其他一些特殊政策,如满足市场销售额扩大、药品效能发生变化、药品用法用量发生变化和界定为亏损品种四种情况的药品有提价的可能;上市未满15年的新药在实际价格与医保支付价差不大于市场平均价差的情况下可进行提价调整;原研药的价格可依据仿制药替代率进行调整以进一步缩小仿制药与原研药的价差。[17]
2.4 医保药品价格改革新动向为应对日益增长的医疗技术费用及其财政影响,自2012年开始,日本开始探索建立一个新系统以评估创新药物、医疗器械和干预措施的成本效益,即采用成本效益评估(Cost-Effectiveness Assessment,CEA)结果对目录中的药品价格进行调整。2012年“成本效益特别委员会”的成立标志着探索的开始,2016年4月,CEA迎来了第一次试点,其结果也在2018年6月的价格调整中得以应用。2019年4月,日本开始正式实施成本效益评估,规定已进入和新进入医保目录的企业均需要提交药品的经济性数据。
日本CEA的流程主要分为评估对象的选择、分析流程、综合评价和价格调整四部分。
(1) 评估对象的选择。考虑到对医疗保险基金的影响,具有高度创新性和医保基金影响力的药物和医疗设备是CEA的主要目标,具体评估项目由Chuikyo进行选择。
(2) 分析流程。整个分析流程分为企业分析和官方分析两个阶段。企业分析时长9个月左右,其模型参数框架由日本国立公共卫生研究所(National Institute of Public Health,NIPH)确定,官方分析时长3个月左右(进行再分析则为6个月左右)。
(3) 综合评价。综合评价主要是对增量成本效果比(Incremental cost-effectiveness ratio,ICER)进行科学性分析。例如,当存在多个适合分析的数据以及ICER的确定有困难时,容许有宽度的评价。综合评价后,对分析框架和ICER的主要分析结果进行报告和公布。
(4) 价格调整。根据CEA结果进行具体调整,当ICER超过基准值时,由中立的专门性组织讨论决定价格调整率。根据现有报销水平、过去支付意愿调查结果、人均GDP和各国基准值,试行期将500万日元/QALY、750万日元/QALY和1 000万日元/QALY作为基准值。对于特殊药品单独设定基准值,治疗方法有限的罕见病(指定疑难重症、血友病及HIV感染症)、小儿疾病、恶性肿瘤等治疗药品基准值为750万/QALY、1 125万/QALY、1 500万/QALY。
3 日本医保药品管理经验小结日本通过上述医保药品管理和制度建设使得药占比长期稳定在21%~22%左右,取得了显著成就,实现了从药品上市、分类管理、定价、医保准入到价格调整的制度化管理。
3.1 药品上市与医保准入同步进行,强调医保准入的重要性日本新药一旦获得上市准入,大部分在60天内(最长90天)进入医保目录,体现了药品上市与医保准入的同步化。企业是在药物的研发阶段即考虑是否进入医保。对民众来说,上市即纳入医保大大提升了患者用药的可及性,改善了患者生存质量。对制造商或药品市场授权持有者来说,上市与医保准入的同步进行意味着药品需要回归价值本身,即是否有创新机制、明确的疗效和安全性。日本将所有的处方药纳入医保,新药一方面获得了市场份额增加的可能,另一方面也面临着同类药竞争的压力,能够实现市场竞争下的自然降价。
3.2 实行药品价格分类管理,充分鼓励药品创新日本新药的定价方法充分体现了药品的创新程度,有利于提高新药研发的积极性。[10]日本根据是否已有同类药,首先将药品分为两类,分别采取“类似药比较法”和“成本核算法”定价。在类似药效比较定价的方法中,又通过制定创新药品药效分类及创新程度的评价标准将药品分为若干类,并以此确定溢价率,创新程度越高溢价率也越高。通过前两种方式定价后的药价还需要参考国外平均价格进行调整,尽量与国际水平保持一致。且不论是类似药比较还是成本核算,亦或是国际药价参考,都规定了明确的计算公式和比例范围。日本通过分类定价的方式既体现了药品的创新程度,又形成了一套结合本国实际并与国际接轨的药品定价体系。
3.3 政府价格管制的同时,注重发挥市场的作用日本虽然对几乎所有的处方药品均实行价格管制,但对药品流通环节不进行限制,而是交由市场交易主体(药品厂商、流通商和医疗机构)谈判决定流通差率。医疗机构进行药品采购时,为获得更高的折扣,往往采用医院联合体的集团化采购模式,就厂商自行确定的销售价格与厂商或流通商进行谈判以获取更低的批发采购价。因采购价与医保支付价之间的价格差为医院留存的合法利润,医疗机构具有与生产商或经销商进行价格谈判的动力,价格差越大,医疗机构获益越多。通过放开市场交易价格,能够不断压低药品价格,挤压药价水分,充分发挥了市场机制的调节作用。
3.4 进行药品价格定期调查,动态调整医保药价初始阶段,每两年一次(即将开始每年一次)的价格调查与调整能够充分了解市场真实价格,掌握市场价格动态,有利于政府在掌握市场实际价格的条件下进行宏观调控[10],真正用好市场这只看不见的手。同时,在进行具体价格调整时还设定了科学的价格调整公式以确保稳定的药品供应。此外,定期的药品市场价格调查也能够作为引导医药市场健康发展的一种有效手段。
4 对我国药品医保生命周期管理的启示基于对日本药品价格及医保管理经验的总结,本文提出了“药品医保生命周期”的概念及相应的管理方法。“药品医保生命周期”这一概念是对“药品生命周期”概念的发展,从市场角度来说,“药品生命周期”是指从药品的研发开始,到注册评价、上市使用、再评价,直至由于安全性问题等原因撤市的整个过程。“药品生命周期”对企业来说意义重大,做好药品生命周期管理是企业抢占市场份额和维持长久发展的关键。由于药品不同于一般商品特殊性,药品的研发、注册上市、生产经营、价格形成、医保准入、供应储备以及监督管理均与患者用药直接相关,每一环节都离不开政府的引导、调控、决策和服务。基于此,本文将“药品医保生命周期”定义为药品从定价、医保准入、目录内价格调整到退出目录的全过程,其管理主体无疑是医保部门,但具体的职责和功能有待进一步探讨。
4.1 提升部门职能,实现药品定价与医保准入的同步化新成立的国家医保局整合了多个部门的医保相关职能,所带来的医保治理体系的重大变革为探索形成合理的医药价格形成机制提供了契机。未来,对于新上市药品,由医保部门统一制定支付标准并纳入医保目录,实现药品定价与医保准入的同步化,为此,需要进一步提升医保部门职能,尤其是医保药品定价的科学能力建设。此前我国开展的创新药价格谈判及医保准入即是药品定价与医保准入同步化的一大探索,未来将进一步优化。
4.2 厘清政府职责,做好药价市场形成与宏观调控相结合就药品价格来说,我国药品价格自2015年发改委发文取消绝大多数药品的政府定价后,转为按照分类管理的原则,通过不同方式由市场形成,政府角色也从直接定价转为价格监管。在医药领域,探索建立开放灵活、多方参与的价格形成机制有利于激发医疗市场活力,引导提供适宜服务。就药品价格而言,医保部门针对不同类别药品设计不同方案通过不同方法制定统一支付价格,但对于市场实际交易价格则不应过多干预,应充分发挥医疗机构与市场活力,允许医疗机构与药商通过招标就采购价格进行谈判,而不应该由政府招标机构代替具体使用药品的医疗机构决定药品种类和用量并代为招标。
4.3 进行分类管理,鼓励药品与医药产业的创新发展医保部门在进行医保支付标准制定的过程中,对不同类别的新药应制定不同的分类评价标准,并依据此标准决定采用类似药比较还是实际成本调查方法,并采用公开、明确的计算方法予以科学的核算[18],最后参考国际价格水平进行调节,逐渐形成既符合我国国情又与国际接轨的创新药价格管理办法。对于新药的分类,可借鉴日本创新药品药效及创新程度的分类方法,客观评价新药的创新程度,对创新药、原研药和仿制药采用不同的定价标准,激励我国药品的研发与创新。
4.4 开展药价调查,定期对目录内药品价格进行调整医保支付标准制定后并不是一成不变的,而是要根据药品实际市场交易价格、医保基金和患者承受能力、药品实际供应及使用情况等因素对支付标准实行动态调整。具体的操作可通过定期、深入的市场调查,根据实际价格情况进行动态调整和宏观调控。具体调整周期可根据实际情况每年或每两年进行一次。再进行具体的药品价格调整时,同样需要建立一套科学的计算公式,针对调整公式和降价比例等都必须做出科学的规定。
4.5 探索退出机制,完善医保药品目录动态调进调出机制对任何一个国家来说,如何实现临床需求、支持创新与医保基金承受能力的平衡都是一大难题,日本也未曾找到一条完美的道路。在当前老龄化日益加剧,医疗技术飞速发展的背景下,医保基金面临的挑战也越来越大。医保药品退出机制的出现无疑给不符合医保准入标准的药品亮起了红灯。此前药品被调出医保目录往往只集中在医保目录整体进行调整时,未来需探索建立常态化和制度化的退出机制, 卫生技术评估(Health Technology Assessment, HTA)作为重要的评估手段将成为决定药品是进入或调出的重要工具。
作者声明本文无实际或潜在的利益冲突。
| [1] |
IMF: World Economic Outlook Databases[R]. 2019.
|
| [2] |
Fullman N, Yearwood J, Abay SM, et al. Measuring performance on the Healthcare Access and Quality Index for 195countries andterritories and selected subnational locations:a systematic analysisfrom the Global Burden of Disease Study 2016[J]. Lancet, 2018, 391(10136): 2236-2271. DOI:10.1016/S0140-6736(18)30994-2 |
| [3] |
日本厚生劳动省.Ministry of Health, Labour and Welfare[EB/OL].[2019-10-21].https://www.mhlw.go.jp/policy/health-medical/health-insurance/index.html
|
| [4] |
经济合作与发展组织[EB/OL].[2019-11-01].http://www.oecd.org/.http://www.oecd.org/health/health-at-a-glance-19991312.htm
|
| [5] |
陈金葵.日本医疗保险制度对我国的启示[D].大连: 东北财经大学, 2018.
|
| [6] |
冯泽昀, 王海银, 陈多, 等. 日本医保支付政策及启示:以实验室项目为例[J]. 中国卫生质量管理, 2018, 25(1): 104-106. |
| [7] |
钱永峰. 日本医疗保障模式对完善我国医疗保障制度的启示[J]. 现代医院管理, 2012, 10(2): 24-26. DOI:10.3969/j.issn.1672-4232.2012.02.009 |
| [8] |
宋春黎, 牛剑钊, 张启明, 等. 日本药品再评价制度介绍[J]. 中国药学杂志, 2014, 49(12): 1087-1090. |
| [9] |
陈成.日本药品定价方法研究[A].中国药学会药事管理专业委员会.2013年中国药学会药事管理专业委员会年会暨"医药安全与科学发展"学术论坛论文集(下册)[C].中国药学会药事管理专业委员会: 中国药学会, 2013.
|
| [10] |
李磊. 日本创新药品价格管理及对我国的启示[J]. 中国新药杂志, 2013, 22(5): 502-504. |
| [11] |
常峰, 李思函. 药品国际参考定价制度对我国的启示——以加拿大、荷兰、日本三国为例[J]. 价格理论与实践, 2013(7): 62-63. |
| [12] |
Zhang Xing, Tatsuo Oyama. Measuring the impact of Japanese local public hospital reform on national medical expenditure via panel data regression[J]. Technological Forecasting & Social Change, 2016, 113. |
| [13] |
日本中央社保医学委员会讨论NHI药价改革与市场扩张[J].中国药物经济学, 2009(6): 96.
|
| [14] |
高艳. 日本药品价格管理制度及其启示[J]. 宏观经济管理, 2015(10): 84-85,92. |
| [15] |
郭莹, 张惠玲, 陈晶, 等. 日本药品价格政策研究及对我国的启示[J]. 中国药物经济学, 2010(4): 63-67. DOI:10.3969/j.issn.1673-5846.2010.04.008 |
| [16] |
常峰, 孙洁. 日本新药国际参考定价方法对我国的启示[J]. 中国新药杂志, 2014, 23(5): 510-512,522. |
| [17] |
陈敬, 赵熙子, 赵亮, 等. 德国、日本和我国台湾地区药品价格规制经验及启示[J]. 中国药房, 2017, 28(25): 3464-3467. DOI:10.6039/j.issn.1001-0408.2017.25.03 |
| [18] |
王亮, 李爱花, 岳晓萌, 等. 日本药品价格制度研究及对我国药品价格管理的启示[J]. 中国卫生经济, 2017, 36(10): 87-91. |
| [19] |
郭丽岩. 日本医保体系与药价管理制度及对我国的启示[J]. 中国物价, 2013(7): 60-62. |
| [20] |
申静静.药品价格形成机制与医保支付标准的研究[D].北京: 首都经济贸易大学, 2017.
|
(编辑 刘 博)




