2. 国家卫生健康委国家药物和卫生技术综合评估中心 北京 100191;
3. 清华大学医院管理研究院 广东深圳 518055
2. National Center for Drug and Technology Assessment, Beijing 100191, China;
3. Institute for Hospital Management of Tsinghua University, Shenzhen Guangdong 518055, China
英国在2011年由英国国家医疗服务体系(National Health Service, NHS)牵头成立了癌症药物基金(Cancer Drugs Fund, CDF),该基金致力于帮助癌症患者更快获得并使用创新药。[1]该基金的成立大大缩短了癌症患者获得创新药治疗的等待时间,也极大降低了患者负担,使大量患者受益,在提高癌症创新药品及创新技术可及性方面起到一定积极作用。
和英国类似,中国随着老龄化程度加深,癌症发病率和死亡率不断上升。为此国家采取了多项卫生政策提高创新药可及性和可负担性,通过降税和医保集中谈判极大减轻了患者负担。但处于专利期的多种癌症治疗药物费用昂贵,基本医疗保险基金可持续性存在风险。如何在加快创新药准入、遴选成本效果更好的药物纳入基本医保支付,同时防范基本医保预算超支,兼顾医疗效率和社会公平,成为亟待解决的关键难点。
英国CDF运行已近9年,在改革过程中多次遇到筹资难题、预算严重超支、纳入药物成本效益争议大、影响NHS支付公平性等诸多问题,并针对问题进行了持续管理优化。英国CDF持续改革中面临的困难、经验及教训,对我国应对创新药准入带来的医保及财政资金压力,具有现实的借鉴价值。本文通过文献梳理和政策分析,对CDF成立后的历史沿革,现阶段CDF的药品评估流程和预算资金管理办法,CDF改革历程中的优化管理策略进行梳理研究,并提出中国癌症创新药准入及管理政策制定的相关建议,以供相关决策及研究参考。
2 CDF历史沿革英国政府于2011年设立了CDF,用于支付部分癌症创新药,CDF由NHS联合国家卫生和临床技术优化研究所(National Institute of Health and Clinical Excellence, NICE)及药品生厂商等联合成立。CDF初始资金约2亿英镑,主要针对部分在NICE评估中未获得推荐纳入NHS支付的癌症创新药。部分癌症创新药因证据不充分或增量成本效果(ICER)在可接受支付阈值之外,但疗效预期较好、临床急需,或者因为患者没有更好的替代药物,为了满足部分患者尽快使用创新药物,减轻患者的经济负担,临时被纳入CDF进行支付,作为进一步评估的过渡期,经过进一步使用评估后,决定是否纳入NHS支付。
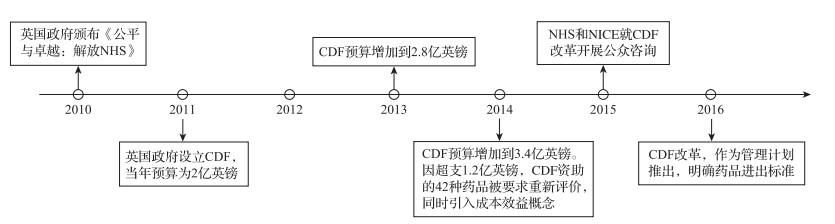
但随着CDF项目推进,患者和纳入药物均出现较快增长,CDF的资金开始面临严重超支和社会公众对医疗效率和公平性等争议。在诸多压力下,CDF经广泛收集意见和建议出台了一系列改革措施。包括2014年重建准入退出机制,对已纳入支付药品启动再评价,增加成本效果等新的模型指标作为价值判断依据,将再评价不具有成本效果优势的药品及时退出支付清单。[2]2016年采用CDF管理准入协议管理办法(managed access agreement)(图 1)。[3]
|
图 1 CDF重要事件发展时间轴 |
改革后的CDF管理权重新纳入NHS的部署,评价标准重回NICE的评估体系中,同时在资金预算管理、动态管理机制、审批流程规范等方面做出具体安排,以应对旧版CDF在基金预算超支、准入标准不明和退出机制缺失等方面的问题。[4]2017—2018年间,CDF总计支出约2亿英镑,大幅低于预估的3.4亿英镑,一定程度上缓解了CDF基金持续预算超支的压力。[5]
3 改革后CDF的药品评估流程和预算资金管理新版CDF协议重回NICE的评估体系,根据评价结果形成3类评审意见:“推荐(Yes)”、“不推荐(No)”和“CDF内有限推荐”。获得“推荐”意见的药品可直接进入NHS的支付目录;获得“不推荐”意见的药品因价值不足,直接退出CDF支付清单;获得“CDF内有限推荐”的药品,则被评审专家组认为虽具有一定价值,但药品临床证据尚不充分,需要在使用中继续收集相关证据后再评估。因此有限推荐药品获得CDF2年支付的过渡期,在此期间被重新评估。[6]改革过渡期结束后,所有进入CDF支持范围的药品都需要经过标准的评估流程。
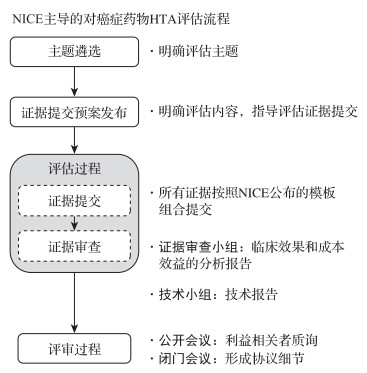
3.1 CDF的药品评估流程根据CDF的评估指南[7],评估流程包括以下几个环节:主题遴选、证据提交预案发布、证据提交、证据审查和评审过程(图 2)。
|
图 2 CDF的癌症药物HTA评估流程 |
多数评估主题遴选由国家健康研究所(National Institute for Health Research, NIHR)完成。厂家在药品上市20个月前和新增适应症15个月前,向NICE提出评估申请。评估对象优先考虑以下情况:1)是否对NHS有重大健康收益?2)是否对相关健康政策有重大影响?3)是否对NHS资源配置有重大影响?4)在全国范围内使用是否违背相关法条规定?5)NICE是否可以通过发布国家指南来增加药品价值?利用现有临床、卫生经济学证据得到的结论是否充分,能够不引起争议?
3.1.2 证据提交预案发布确定评估主题以后,NICE会根据该项技术特征列出证据提交预案,预案用以指导评估证据提交,内容包括技术适宜人群、参比对象、潜在患者亚组、健康结局指标、特殊问题(如伦理问题、平等性)等要素。预案完成后,NICE会识别并组织利益相关者,举行专题研讨会,共同商议修改或调整预案内容,明确范围界定细节,形成证据提交预案终版。
3.1.3 评估过程(1) 证据提交。在开始评估之前,厂商能够与NICE沟通范围预案的细节,明确证据提交的具体要求,并获得协议签订的官方建议。所有证据需要按照NICE公布的证据提交预案进行组合,如果厂商准备提交卫生经济学模型作为支持材料,则应告知相应的操作软件,并允许该模型能够进行验证和调试。
(2) 证据审查。NICE内部将组建证据审查小组和技术小组。证据审查小组分析厂商递交的证据,测试材料中模型的稳定性和结果的准确性,完成该技术的临床效果和成本效益的分析报告。其后技术小组会参考这份报告,同时征询相关专家意见,形成一份技术报告,内容包括:证据审核结果、技术概括性评论、技术改善建议、NICE决策过程的建议等。报告会反馈给厂商,指导降低证据结果中的不确定性,同时与其他文件一起作为评审参考材料。
3.1.4 评审过程评审过程以评审会议的方式进行,包括两部分。第一部分为公开会议,由NICE组建的评审委员会和利益相关者共同参与。NICE以技术报告为基础向评审专家和其他与会人员介绍待评审技术,并鼓励临床专家、NHS专员、患者等利益相关者提问和质询,厂商代表做解答。第一部分不会讨论涉密内容,其后会方要求公众、媒体以及包括临床专家、NHS专员在内的利益相关者离场,举行第二部分闭门会,会上将审议保密商业信息并形成推荐建议。推荐建议及结果将在7日后向公众发布,并同时发布在NICE的官方网站上。
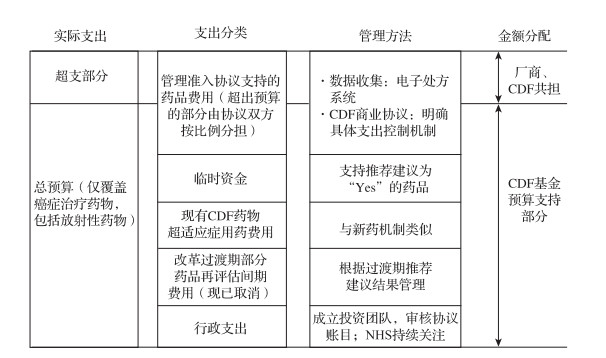
3.2 改革后CDF的资金预算管理2016年改革后,新版CDF预算由NHS结合当年总体卫生保健需求和保障重点制定,CDF遴选药物清单仅涉及癌症治疗药物,包括一些放射性治疗药品。一些癌症治疗药物,如获得关税补偿、激素类、放射性治疗技术及医疗设备,则均不会被纳入CDF遴选范围。CDF年度预算包括以下几个部分:管理准入协议内药品;临时资金(interim funding);CDF超说明书药品(Off-label Cancer Drug Indication);行政支出等。[8]
|
图 3 新版CDF预算管理协议及分配方案示意图 |
为了确保癌症患者能够尽快从新药中受益,获得“CDF内有限推荐”建议的药品能够与CDF协商签订管理准入协议,协议签订后CDF开始对该药费用进行补偿,补偿价格为协议中商定的保密价格。根据协议有药品生产商对基金超支部分进行分担,且金额不设上限。协议同时包括数据收集协议和预算风险分担协议。数据收集协议是用于评估需要的数据规范和要求,基于药品特性及患者、专家意见,由NHS、NICE、生产商等共同协商制定。协议对服务规范和数据质量提出要求,所有诊疗服务需配备电子处方系统。一方面,使用电子处方能够减少与处方、药品供应、储存管理有关的错误,减少药物浪费;另一方面,电子处方能够支持系统性抗癌治疗(Systemic Anti-Cancer Therapy, SACT)数据收集[9],使评估充分使用临床真实世界数据。预算风险分担协议由NHS与厂商协商形成保密价格,同时涵盖超支风险分担比例及具体支出控制办法。
CDF主要通过以上办法在药品临床使用过程中规定疗效指标、数据标准和服务规范,帮助评估实施及决策者进行总体把握,对超支风险进行控制和调整支付政策。
3.2.2 临时资金和现有CDF药物超说明书用药获得“推荐”建议的药品生产商可以向CDF申请临时资金,申请通过后药品将立即供应给患者。临时资金补偿比为推荐价格的100%,用以支付药品退出CDF进入NHS常规报销的过渡期费用。CDF药物超说明书用药支付机制与新药机制类似,也需要通过相应评估流程,获得推荐建议后,申请预算补偿。
3.2.3 CDF行政支出行政支出一般设定为预算的2%,为专业运营团队支付管理费用。CDF运营团队工作包括:准入协议制定、审核,支付周期执行进度,支出审查和财务报告。此外,NHS作为上级部门也会对运营机制进行持续审查,评估运行情况,及时调整风险环节,保障基金平稳运行。
4 CDF改革历程中的经验借鉴 4.1 CDF改革历程中的波折和经验CDF作为癌症创新药专项基金,普遍受到了癌症患者群体的支持,但同时也遭到了一些专家学者和民众的质疑。评估显示,CDF初期支付的药物临床效益较差,仅有42%达到了美国临床肿瘤学会(ASCO)价值评价推荐标准[10],仅18%达到欧洲医学肿瘤学会(ESMO)价值推荐意见要求[11];此外纳入CDF支付的药物往往因为价值证据始终不充分,引发广泛争议。有观点认为CDF造成了卫生保健资金的浪费,降低了国民总体健康水平,减少其他患者的健康机会,给NHS医疗服务供给带来新的不平等。[12-13]此外,CDF准入药物在使用过程中未能同步提供真实世界研究数据,缺乏对药品疗效的评价,削弱了NHS对药品进一步议价的能力。[14]
以上是CDF在历次改革过程中出现的问题,NHS历经数年、数次政策修正和管理办法调整,其中经验教训值得我国借鉴。[15]
4.2 对我国医保癌症创新药准入及管理政策的建议 4.2.1 建立多方筹资机制成立专项癌症基金在中国现有老龄化和癌症患者数不断攀升压力下,医保基金赤字风险增加,应综合我国现有发展中国家支付能力,应设计可负担、可稳定运行的多元筹资癌症创新药物基金。为了加快癌症创新药纳入报销,减轻癌症患者家庭负担及增加创新药品可及性,建议在基本医疗保险基金以外,成立多元化筹资途径的癌症基金,或发展商业保险作为辅助支付途径,以缓解基本医保在癌症治疗的压力。
对一些证据不充分、成本效果不明确、但临床急需药物,在纳入基本医保支付前,通过建立过渡期使用试点或临床医学中心有限范围内支付,同时做好预算风险分担协议,使用临时癌症专项基金支付,在试点临床使用的同时收集新的价值证据,经临床再评估,给出评审推荐意见。
4.2.2 使用HTA工具筛选创新药国际多项经验表明,通过建立完善的卫生技术评估(HTA)体系,利用药品临床综合价值评估工具及方法,遴选成本效果好、预算影响可控的癌症创新药纳入基本医保,有利于提高基金使用效率,防范基金预算超支风险。从国家层面建立创新药价值评价指标体系及方法流程,展开药品价值综合评估,有利于形成科学规范的支付标准,实现价值购买和患者群体健康收益最大化。
4.2.3 充分利用药品使用真实世界数据进行使用后再评价药品真实世界数据,可以弥补早期上市审批中RCT有限证据的不足,补充药品在实际使用中不同亚组患者、不同使用场景、长期用药等情况下的效果及不良反应、疾病负担等信息。真实世界证据是医保准入、报销及预算管理中重要的决策依据。在实际评价过程中,真实世界数据收集需要建立跨部门、多中心、持续、完整、标准化信息系统。实现真实世界证据的汇总和梳理,需要整合目前卫健、财政、民政和医保等管理部门的健康大数据,实现数据共享,同时需要培育大数据、人工智能在内的多学科专业队伍从事用药分析、数据挖掘、生存分析及因果准则等内容。
4.2.4 设计合理的基金预算风险分担管理协议现阶段我国医保基金管理主要包括总额控制、DRGs、按病种、按项目支付方式,距离实现按价值支付仍有较大差距。实现医保的价值购买,需要在充分获取药品价值证据基础上,探索建立以健康结果为导向、根据循证证据动态调整报销政策,灵活运用基于财务的协议(量价协议、使用上限),基于疗效协议(按证据发展支付、按时间节点支付、按疗效支付),增值配套协议(配套赠药及折扣、产品)等多种风险分担协议,在提高癌症创新药可及性的同时,维护医保基金稳定运行。
作者声明本文无实际或潜在的利益冲突。
| [1] |
Stephens P, Thomson D. The Cancer Drug Fund 1 year on——success or failure?[J]. The Lancet Oncology, 2012, 13(8): 754-757. DOI:10.1016/S1470-2045(12)70273-5 |
| [2] |
NHS England. Operation of the Cancer Drugs Fund 2014/15 and 2015/16.(2014-11-12)[2020-03-15]. http://www.england.nhs.uk/wp-content/uploads/2014/11/item9-board-1114.pdf
|
| [3] |
Claxton K P. Pharmaceutical pricing: early access. The Cancer Drugs Fund and the Role of NICE[R]. Centre for Health Economics, University of York, 2016.
|
| [4] |
Littlejohns P, Weale A, Kieslich K, et al. Challenges for the new Cancer Drugs Fund[J]. The Lancet Oncology, 2016. |
| [5] |
Wood E M, Hughes D A. The New and Non-Transparent Cancer Drugs Fund[J]. Pharmacoeconomics, 2020, 38(1): 1-4. |
| [6] |
NICE technology appraisals and the Cancer Drugs Fund Frequently Asked Questions for patient groups[EB/OL].[2020-03-15]. https://www.nice.org.uk/Media/Default/About/NICE-Communities/Public-involvement/Developing-NICE-guidance/CDF-QandA-sep-16.pdf
|
| [7] |
Guide to the processes of technology appraisal[EB/OL].[2020-03-15]. https://www.nice.org.uk/process/pmg19/resources/guide-to-the-processes-of-technology-appraisal-pdf-72286663351237
|
| [8] |
Appraisal and Funding of Cancer Drugs from July 2016(including the new Cancer Drugs Fund)-A new deal for patients, taxpayers and industry[EB/OL].[2020-03-15]. https://www.england.nhs.uk/wp-content/uploads/2013/04/cdf-sop.pdf
|
| [9] |
National Chemotherapy Board, Consent for Systemic Anti-Cancer Therapy (SACT)[R]. 2016.
|
| [10] |
Fojo T, Mailankody S, Lo A. Unintended consequences of expensive cancer therapeutics-the pursuit of marginal indications and a me-too mentality that stifles innovation and creativity:the John Conley Lecture[J]. JAMA Otolaryngol Head Neck Surg, 2014, 140: 1225-1236. DOI:10.1001/jamaoto.2014.1570 |
| [11] |
Cherny NI, Sullivan R, Dafni U. et al. A standardised, generic, validated approach to stratify the magnitude of clinical benefit that can be anticipated from anti-cancer therapies: the European Society for Medical Oncology Magnitude of Clinical Benefit Scale (ESMO-MCBS). Ann Oncol, 2015, 26: 1547-1573.
|
| [12] |
Claxton K, Martin S, Soares M. et al. Methods for the estimation of the National Institute for Health and Care Excellence cost-effectiveness threshold[J]. Health Technol Assess, 2015, 19: 1-503.
|
| [13] |
National Audit Office. Investigation into the Cancer Drugs Fund. Department of Health and NHS England (ed)[EB/OL].[2020-03-20]. https://www.nao.org.uk/wp-content/uploads/2015/09/Investigation-into-the-Cancer-Drugs-Fund1.pdf
|
| [14] |
Chamberlain C, Collin S M, Stephens P, et al. Does the cancer drugs fund lead to faster uptake of cost-effective drugs? A time-trend analysis comparing England and Wales[J]. Br J Cancer, 2014, 111: 1693-1702. DOI:10.1038/bjc.2014.86 |
| [15] |
刘跃华, 郭武栋, 赵琨, 等. 癌症创新药支付管理政策建议——以英国癌症药物基金(CDF)改革历程为鉴[J]. 中国医疗保险, 2020(5): 76-80. |
(编辑 薛 云)





