中国丙型肝炎病毒感染者约为1 000万例。[1] 2005—2014年我国丙肝发病率呈逐年上升趋势,2012—2016年每年报告的发病人数均超过20万。[2, 3]丙肝病毒慢性感染可导致肝脏炎症坏死及纤维化,部分患者可发展为肝硬化或肝癌,这些肝癌患者死亡率在近25年内明显提高。[4]丙肝患者进入进展期后会占用越来越多的医疗资源,并给卫生筹资系统和患者家庭带来极大的经济负担。[5]
丙肝直接作用抗病毒药物(DAA)是创新性治疗药物。与干扰素相比,DAA给药方便、不良反应少、病毒学应答率高、疗程短[1],但DAA高昂的价格也给患者带来沉重的经济负担。
天津和成都地区作为经济较发达的城市,于2018年相继出台了丙肝创新药医保政策。根据国家统计局数据,2018年天津和成都的GDP分别为13 362.92亿元和15 342.77亿元,年末总人口分别为1 560万和1 476万,良好的经济发展和医保管理水平为创新药医保准入支付政策(简称“创新药政策”)的出台打下了基础。两地首先通过谈判降价将丙肝DAA药品纳入医保报销范围,并进一步实施了打包支付政策。天津将丙肝药费、诊疗费等所有费用统一打包按人头支付,最高支付限额为40 500元;成都采取药费按人头打包,药品限额标准为43 100元,其他费用按项目付费的“分类支付”思路。天津和成都出台丙肝创新药政策一年以后,2019年国家医保局将丙肝创新药纳入了国家医保谈判清单,4种丙肝创新药进入医保目录。
本研究旨在分析天津和成都两地丙肝创新药政策实施后对医药费用的影响,探究两地政策实施效果的差异及原因,从而为其他创新药国家谈判准入后地方支付政策的制定提供参考和建议。
2 研究方法 2.1 研究设计本研究采用中断时间序列(Interrupted Time Series,ITS)研究设计。天津的政策干预前观察期2014年5月—2018年3月,政策干预后观察期从创新药政策实施的2018年4月—2018年10月。成都的干预前观察期从2016年1月—2018年10月,干预后观察期从政策实施的2018年11月—2019年4月。
2.2 数据来源天津的数据主要来自于定点医院的病历记录。在天津市创新药政策实施以前,医保部门指定了一家医院作为丙肝医保患者的定点治疗医院,在创新药政策实施以后指定了两家定点医院,本研究选取了前后两个时期均为定点医院的病历数据,由于定点医院数量不超过两家,且定点医院的专科治疗水平较高,享有特殊医保报销政策,其收治患者覆盖范围广,故定点医院的样本对天津总体有代表性。2014年5月—2018年10月,凡是在该定点医院完成过一个治疗疗程的丙肝患者皆被纳入到研究范围中。本研究成都的数据主要来自于成都医保数据库,包括2016年1月—2019年6月期间该数据库中第一诊断ICD编码为B18.2慢性病毒性丙型肝炎的全部患者。
研究抽取的数据包含患者的诊断、治疗费用等信息,采用医药费用(人均医药总费用、人均药费、除药费以外的人均其他费用)作为结果变量,其他影响因素作为自变量,进行统计分析。
2.3 分析方法中断时间序列分析是收集干预前后多个时间点的结果数据,在控制了结果变量干预前变化趋势后,用统计学模型评价干预措施的效果。其公式如下:

|
其中Yt为在t时间点的因变量,在本研究中为“医药费用”,包括人均医药总费用、人均药费、除药费以外的人均其他费用;Tt为时间变量,在本研究中为“患者开始治疗月份”(考虑到丙肝治疗一个疗程至少需要3个月的时间,故采用“患者开始治疗月份”更方便ITS分析);Xt为政策变量,当处于创新药政策干预阶段时取值为1;XtTt为交互项。β0是结果指标基线水平的估计值,β1是基线趋势的估计值,β2是创新药政策实施前后结果指标水平值的差值,即水平瞬时变化的估计值;β3是创新药政策实施后患者结果指标变化趋势;εt是误差项。
3 研究结果 3.1 入组患者基本情况及费用描述本研究收集了政策实施前后的天津某医院病历记录共825份,成都市医保库中第一诊断为B18.2的患者共有952例(表 1)。创新药政策实施前,天津人均医药总费用(以下简称“人均总费用”)为44 421.08元,成都人均总费用为21 633.25元。创新药政策实施后,天津人均总费用为20 945.02元,人均药品费用为17 750.81元,约占总费用的85%;成都人均总费用为25 432.30元, 人均药品费用为19 140.70元,约占总费用的77%。
| 表 1 研究对象基本情况 |
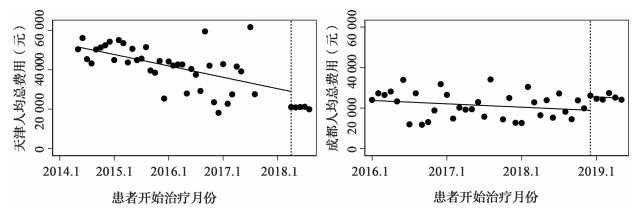
天津市丙肝治疗人均总费用中断时间序列分析结果如图 1和表 2所示。2018年4月天津创新药政策实施以后,人均总费用水平瞬时下降了7 753.43元,人均总费用随时间变化呈平稳趋势(P=0.13)。
|
图 1 创新药政策对天津、成都人均总费用的影响 |
| 表 2 中断时间序列分析结果 |
从2017年8月份开始到2018年4月创新药政策实施之前,图中数据出现了一段空白,这是由于2017年4月首款DAA原研药在中国大陆上市以来,患者社群内部一直传有该药可能会在近期进入医保的消息,有更多不耐受的患者选择中止治疗保持观望,或者使用仿制药,在这一段时间内,原政策下进行登记签约使用干扰素治疗的患者降为个位数,在一些月份甚至为0,计算出来的人均总费用波动较大,故将这一时期的数据不纳入中断时间序列分析。
成都市丙肝治疗人均总费用分析结果如图 1和表 2所示。在2018年11月成都创新药政策实施之前,人均总费用下降趋势不明显(P=0.16)。创新药政策实施后,人均总费用瞬时上升了6 680.78元(P<0.01),实施后治疗费用随时间变化的趋势改变没有统计学意义(P=0.84)。
3.3 创新药政策对人均药费和其他费用的影响人均药费和人均其他费用的中断时间序列分析结果如图 2和表 2所示。天津创新药政策实施以后,天津市人均药费瞬时下降了5 718.34元,人均其他费用降低2 035.09元(P<0.05)。成都创新药政策实施以后,成都人均药费瞬时上升了6 917.20元(P<0.01),人均其他费用瞬时下降了236.42元,下降没有统计学意义。

|
图 2 创新药政策对天津、成都两市人均药费和其他费用的影响 |
医保准入谈判降低了创新药单价是推动医药费用下降的基础。DAA药物在全球不同国家的定价差异较大,美国、英国、法国和澳大利亚等国家的每疗程价格在45 000~84 000美元不等,而埃及和孟加拉国的价格仅为900美元每疗程。[6, 7]国际定价不一致反映了丙肝患病率、人均收入、支付能力和政府监管政策的全球差异。[8]中国潜在丙肝患者数量庞大,并且作为发展中国家人均支付能力较低,中国医保部门作为药品市场主要支付方便具备了较强的议价能力。创新药医保政策出台后,天津和成都患者实际购买DAA时,一个疗程的总费用均不超过2万元,降幅分别达到了70.6%和71.1%。在2019年国家药品谈判中,DAA类药物的价格降幅更是由于创新性地采取了竞争性谈判的策略达到了85%以上。国家谈判覆盖了更大的市场,拥有更强的议价能力,本次国家谈判的结果充分体现了集中谈判制度的优越性。
丙肝治疗主要依赖于抗病毒药物治疗,对于创新药疗法,天津药品费用占总费用的比例达到了85%,是医药总费用的重要组成部分。医保准入谈判显著降低了抗病毒药物单价,使得创新药政策实施后,天津人均药费瞬时下降了5 718.34元,是天津人均总费用降低的重要因素之一。
尽管医保准入谈判是推动医药费用下降的重要因素,但是医药费用的改变幅度还取决于传统疗法和创新疗法的价格差异。传统干扰素治疗包括两个方案,一个方案采用聚乙二醇干扰素,单价在1 000元左右,另一个采用普通干扰素,单价一般低于100元。干扰素治疗一般每周一次,一个疗程长达48周,甚至72周。使用聚乙二醇干扰素治疗的药品费用高于谈判后使用创新药治疗的药品费用,而使用普通干扰素治疗的药品费用则略低于谈判后使用创新药治疗的药品费用,天津使用聚乙二醇干扰素进行治疗的患者比例较大,成都使用两种干扰素治疗的患者比例相近,所以在天津创新药政策实施后,人均药费瞬时下降幅度较大,成都创新药政策实施后,人均药费瞬时上升了6 917.20元(P<0.01)。由于药品费用占成都人均总费用的72%~77%,创新药政策实施后,成都人均总费用也出现明显上升的情况。
4.2 按人头付费政策对医药费用的影响天津和成都两地在按人头付费政策的设置上存在略微差异,这为观察按人头付费政策对医药费用的影响提供了一个机会。天津将药费和服务费一起按人头打包支付,并采用了“结余留用”的激励措施。成都将药费按人头打包支付,其他费用采用按项目支付。丙肝治疗费用主要由抗病毒药物费用和包括检查、诊疗在内的其他费用组成,在创新药按人头支付政策下,由于抗病毒药物DAA的疗程和单价较为固定,即抗病毒药物费用较为固定,支付政策影响的主要为除药费外的其他费用,将医药费用一起按人头打包付费,并结合“结余留用”的激励措施,避免了医疗机构诱导需求将医保额度用尽的过度医疗行为,在合理范围内减少其他检查和治疗的处方,减少医保开支和患者自付费用,并有效地调动了医疗机构管理患者预防复发的积极性。创新药政策实施后,天津人均其他费用瞬时下降了2 035.09元(P<0.05),而成都人均其他费用瞬时变化并没有统计学意义(P>0.05)。
4.3 政策建议天津的人均医药费用降低是创新药价格谈判和医药费用按人头打包支付共同作用的结果。在全面推进医保精细化管理的背景下,基于医疗机构门诊收入占总收入50%以上的现实,对门诊慢性病患者包括创新药在内的医药费用探索按人头打包支付或基于价值/效果的支付是对目前住院患者DRG支付方式改革的有益补充。基于本研究的结果,我们提出以下政策建议。
第一,继续积极推进创新药国家准入谈判。如前文所述,医保管理部门应充分发挥市场优势地位,在支付能力范围内,将社会反响大、疾病经济负担重、远期控费效果好的疾病及其创新药纳入谈判清单,采用包括管理准入协议在内的多种方式将药品价格推至合理区间,以期进一步降低目标疾病患者的经济负担,提高基金的使用效率和社会收益。
第二,积极推进实施门诊慢性病患者医药费用按人头支付或基于价值/疗效支付的改革。包括DAA在内的2019年国家医保谈判确定的97个药品都执行了全国统一的支付标准,对于地方医保部门来说,创新药品的价格在这一政策执行后是固定的,寻求降低医疗费用的努力应当通过降低其他药物和检查费用等来实现。故应当鼓励将药费、检查费等医保支付范围内的全部费用进行打包付费,并建立适宜的补偿激励机制,充分调动医生积极性,提高医疗服务水平,保障支付方式改革的控费目标达到预期效果。
第三,因地制宜,量力而为。不同省市的疾病谱、用药结构、医保基金支付能力等条件都存在着较大差异,将创新药纳入医保后,使用创新药患者比例增加会推高医疗费用,给医保基金带来压力。因此需要因地制宜地制定相关政策,以确保创新药纳入医保后能够更好的落地实施。
作者声明本文无实际或潜在的利益冲突。
| [1] |
中华医学会肝病学分会, 中华医学会感染病学分会. 丙型肝炎防治指南(2015年更新版)[J]. 传染病信息, 2016, 29(1): 1-19. |
| [2] |
常峰, 段承阿鑫, 金琇泽, 等. 我国丙型肝炎治疗现状与相关医疗保障补偿机制分析及建议[J]. 中国药房, 2018, 29(2): 151-155. |
| [3] |
万彬, 丁海霞, 占伊扬. 丙肝医疗费用现状及支付方式研究[J]. 中国医疗保险, 2017(10): 59-61. |
| [4] |
Gentile I, Maraolo A E, Niola M, et al. Limiting the access to direct-acting antivirals against HCV:an ethical dilemma[J]. Expert Rev Gastroenterol Hepatol, 2016, 10(11): 1227-1234. DOI:10.1080/17474124.2016.1234375 |
| [5] |
Mchutchison J G, Bacon B R, Owens G S. Making it happen:Managed care considerations in vanquishing hepatitis C[J]. The American Journal of Managed Care, 2008, 13(S12): 327-336, 337-340. |
| [6] |
Marshall A D, Saeed S, Barrett L, et al. Restrictions for reimbursement of direct-acting antiviral treatment for hepatitis C virus infection in Canada:a descriptive study[J]. CMAJ open, 2016, 4(4): 605-614. DOI:10.9778/cmajo.20160008 |
| [7] |
Phelan M, Cook C. A treatment revolution for those who can afford it? Hepatitis C treatment:new medications, profits and patients[J]. Bmc Infect Dis, 2014, 14: S5. |
(编辑 薛 云)





