2. 山东省医药卫生科技信息研究所 山东济南 250062
2. Shandong Institute of Medicine and health Information, Jinan Shandong 250062, China
2018年5月,国家卫生健康委员会等五部门联合发布了我国《第一批罕见病目录》,以目录准入的方式明确列举了121种罕见病,这是我国罕见病领域里程碑式的文件,对于罕见病的诊治、临床管理、科学研究、药物研发和医保支付以及慈善救助工作等都将具有重要的推进意义。[1]在我国,罕见病患者面临着早期诊断难、药物供应难和社会保障难这三道突出难题[2],对于解决罕见病患者的诊疗、用药和保障问题,政府多个部门也在积极作为,出台了一系列政策措施。本文基于政策工具视角对国家层面制定的罕见病领域相关政策文本进行量化分析,并通过构建“政策目标—政策工具”分析框架,深入探讨我国罕见病领域政策现状和面临的挑战,为罕见病领域相关政策的完善提供参考。
1 资料与方法 1.1 资料来源本研究对我国国家层面发布的罕见病领域相关政策进行了全面收集,政策文本来源于国务院、中国政府网、国家卫生健康委员会、国家药品监督管理局等政府官网,并以CNKI政府文件数据库为补充检索,政策收集时间截止到2020年10月26日,共收集到与研究相关的文件32份(表 1)。
| 表 1 我国国家层面罕见病相关的政策文本 |
以纳入分析的罕见病领域政策文本的政策条款作为分析单元,按照“政策编号—条款序列号”进行编码。政策中若出现同一个条款对应一个以上的文本内容分析单元,则在重复的编码后标注“*”以示区别。所有的编码结果运用EXCEL对编码内容进行描述性统计与内容分析。
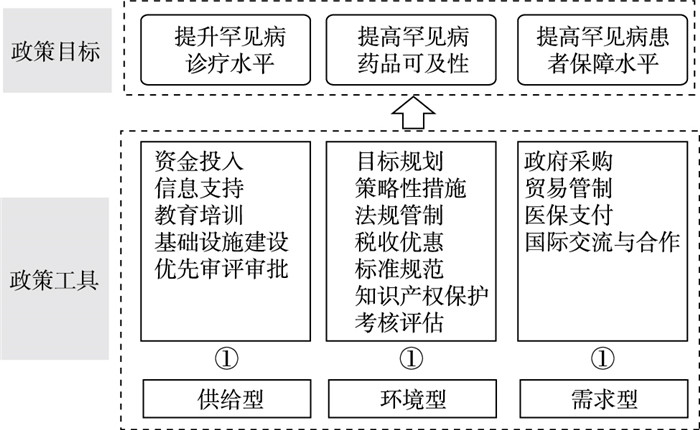
2 基于“政策目标—政策工具”的分析框架随着政策工具理论研究的不断成熟,政策分析框架也向多维发展,如司建平等[3]基于政策工具和政策过程两个维度构建二维分析框架对我国医养结合政策文本进行分析,熊烨[4]构建了一个包括政策工具类型、利益相关者、医疗活动类型的三维分析框架,对我国的医改中的政策工具使用状况进行描述与分析。本文从政策目标、政策工具两个维度来构建罕见病领域政策的分析框架,以政策工具维度分析为主线,以政策目标分析为辅助维度,对我国罕见病政策领域相关政策进行统计分析。分析框架如图 1所示。
|
图 1 我国罕见病领域政策目标—政策工具分析框架 |
政策目标是决策者希望通过政策所达到的目的和效果。在对相关政策进行精读和编码分析的过程中发现,我国罕见病领域的专项政策较少,因此具体成文的罕见病领域直接相关的目标规划类政策工具运用较少。经过对政策文本的分析及课题组反复讨论,本文梳理罕见病相关政策文本,并对政策目标进行总结提炼,将政策目标概括为提升罕见病诊疗水平、提高罕见病药品可及性和提高罕见病患者保障水平三个方面。
2.2 政策工具维度政策工具是政策主体实现政策目标的各种治理手段的统称,其正确选择是顺利实现政策目标的基本保证,亦可增加政策制定的科学性,改善政策执行过程与效果。[5]本文采用Rothwell和Zegveld提出的工具类型,将政策工具划分为供给型、环境型和需求型。[6]供给型政策工具指政府通过资金投入、基础设施建设、公共服务、人才和信息等要素的扶持,推动罕见病患者的诊疗、用药和保障水平提升;环境型政策工具即政府通过目标规划、金融、税收、法规管制等政策,间接影响罕见病患者的诊疗、用药和保障水平提升,为其创造有利的政策环境;需求型政策工具指政府对需求侧的培育,通过政府采购、医保支付等举措拉动罕见病药品和服务的需求(表 2)。
| 表 2 罕见病领域政策工具名称及含义 |
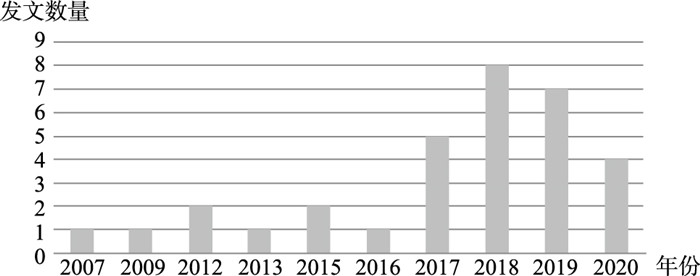
我国国家层面罕见病领域政策发文时间跨度在2007—2020年之间(图 2),政策文本发布集中在2017年之后,占发文总数的75%。我国专项罕见病政策很少,2018年之前仅仅是在相关医药政策文件中个别提及罕见病用药等问题。界定标准不明确导致我国罕见病患者分布难以统计,从而无法启动流行病学研究,相应的罕见病防治工作的开展也失去了基石。[7]2018年,《第一批罕见病目录》的出台,让大众对罕见病有了清晰的认识,之后罕见病领域进入政策支持的快速通道,诊断、新药审批、医保等各种政策密集推出。
|
图 2 我国罕见病领域相关政策年度分布 |
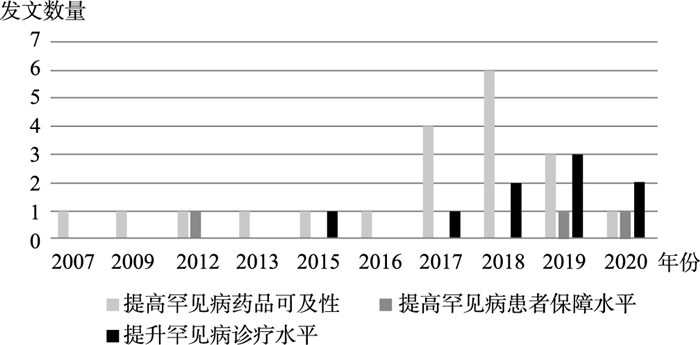
32个政策文本中直接提到政策目标的仅有4个,分布在提升罕见病诊疗水平的专项政策中,如《国家卫生健康委办公厅关于印发罕见病诊疗指南(2019年版)的通知》(国卫办医函〔2019〕198号)中明确提出,“为提高我国罕见病规范化诊疗水平,保障医疗质量和医疗安全,维护罕见病患者健康权益,根据我委等5部门印发的《第一批罕见病目录》,我委……牵头制定了《罕见病诊疗指南(2019年版)》。”总体来看,提升罕见病药品可及性是政策重点,有62.5%(20个)的政策是以此为目标;28.13%(9个)的政策文本目标是提升罕见病诊疗水平;仅有9.37%(3个)的政策文本目标为提高罕见病患者保障水平。从时间分布上看,“提升罕见病药品可及性”的政策目标始终贯穿始终,并在2017—2019年政策密集出台;从2015年开始,目标为“提升罕见病诊疗水平”的政策文本开始出台,并在2018—2020年达到高峰;相对而言,“提升罕见病患者保障水平”的政策目标较少,且分布在2019—2020年(图 3)。
|
图 3 我国罕见病领域政策目标的时间分布 |
78条政策工具文本中,环境型政策工具使用最多,占比55.13%;其次是供给型政策工具,占比35.90%;最少的是需求型政策工具,仅占8.97%(表 3)。这说明政府更倾向于宏观调控,为罕见病的诊疗、用药和保障领域创造良好的政策环境。
| 表 3 政策工具使用分布情况 |
在供给型政策工具中,使用最多的是公共服务类工具中的优先审评审批(53.57%),国家通过改革罕见病用药的审评审批制度,缩短时限,来促进急需的罕见病药物上市。除此之外,还针对罕见病的管理工作运用了教育培训(21.43%)、信息支持(14.29%)、基础设施建设(7.14%)和资金投入(3.57%)等工具,但数量较少,我国罕见病医疗急缺专业人才和资金投入,无法做到平衡状态满足患者需求,亟待完善巩固。[8]
环境型政策工具中,法规管制运用最多,占46.51%,其次为策略性措施(20.93%),标准规范(11.63%)、目标规划(9.30%)、考核评估(4.65%)、税收优惠(4.65%)和知识产权保护(2.33%)工具相对运用较少。政府更倾向运用法规管制和策略性措施,从约束性和鼓励性两侧入手来明确罕见病领域各利益相关者的责任,从而进行监督和管制。
需求型政策工具整体使用偏少,在需求型政策工具中,医保支付占比为57.14%,其次运用了政府采购(14.29%)、贸易管制(14.29%)及国际交流合作(14.29%)。
3.4 政策目标—政策工具的二维分析78条政策工具文本中,有39条(50%)用于提高罕见病药品可及性,有35条(44.87%)用于提升罕见病诊疗水平,用于提高罕见病患者保障水平的仅有4条(5.13%)。(表 4)
| 表 4 政策目标—工具使用分布情况 |
32个政策文本政策目标和政策工具分布占比不均衡,提升罕见病药品可及性是政策重点,并且该目标始终贯穿罕见病政策的始终,其次为提升罕见病诊疗水平,提升罕见病患者保障水平的政策目标较少。罕见病疾病负担相关研究表明罕见病治疗费用高昂,疾病负担较重,有的罕见病医疗费用报销比例低,医保补偿效果并不明显。[9-11]近两年随着国家医疗保障局的成立,国家已开始重视罕见病的保障工作。2019年医保目录调整的一大亮点是优先考虑癌症及罕见病等重大疾病治疗用药,但纳入国家医保目录的40种罕见病药物仅用于治疗22种罕见病适应症,仍有12种罕见病在我国上市的所有治疗药物未被纳入国家医保目录,涉及14种治疗药物,其中高值药物保障问题尤为突出。[12]我国基本医疗保障筹资水平和负担能力有限,医保部门如何在兼顾公平的情况下,尽可能多地保障罕见病患者的医保需求,是未来政策的重点。
4.2 政策工具的选择和使用存在一定失衡或缺失 4.2.1 供给型工具中,服务类工具运用较多,资金投入类工具运用较少供给型工具中运用最多的是对罕见病药品实施优先审评审批制度,是我国罕见病领域政策的重点。2019年以来,随着《药品管理法》与新《药品注册管理办法》相继修订,从法律与规章层面正式确立了罕见病药物优先审评审批制度,罕见病治疗药品、医疗器械注册申请人还可申请减免临床试验或附带条件批准上市。政策实施成效初现:全球首个脊髓性肌萎缩症(SMA)精准靶向治疗药物诺西那生钠注射液在国内的整个审批周期不到6个月(173天)[13];2018年和2019年分别有3个和6个罕见病药物品种通过了优先审评程序,得以加快上市;得益于国家加快临床急需境外新药审评审批相关政策,2019年药审中心批准了16个用于治疗罕见病、临床急需的药品,较2018年增长了60%,并在3个月之内完成审评,大大缩短了临床急需境外新药在我国上市的时间。[14]随着2018年《第一批罕见病目录》的出台、《罕见病诊疗指南(2019版)》的发布、我国罕见病的预防、诊断和治疗已处于起步阶段。2019年,随着全国罕见病诊疗协作网络相关政策的出台,我国已组建覆盖324家医院的全国罕见病诊疗协作网,在协作网内建立起双向转诊、远程会诊制度。国家重视信息支持工具的运用,通过开展罕见病病例诊疗信息登记工作全方位了解我国罕见病现状。但是,资金投入与基础设施建设等政策工具使用频率最低,充足的资金是投入推动罕用药研发和罕见病诊疗水平提升的关键要素,政府应进一步加大人力物力财力的支持力度。
4.2.2 环境型政策工具中,法规管制类工具运用过多,激励型工具运用较少环境型政策工具中运用了较多的法规管制、策略性措施,主要是对罕见病药品的注册以及罕见病管理等方面做出相关规定,明确管理责任和内容。策略性措施大多提及国家对罕见病治疗药物研发的鼓励与支持,但并无具体的实施路径与措施。激励性质的且具有操作性的金融支持、税收优惠和知识产权工具也运用较少,金融支持指政府通过放宽金融限制、创造融资条件等来推动对罕见病药品等企业的研发与创新,目前我国罕见病领域政策金融支持工具缺失,需要填补相关政策。在税收优惠方面,《关于罕见病药品增值税政策的通知》(财税〔2019〕24号)中提到,对国内罕见病药品选择简易办法依照3%征收率计算缴纳增值税,对进口罕见病药品,按3%征收进口环节增值税,以此鼓励罕见病制药产业发展,降低患者用药成本。《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》中提出,对罕见病治疗药品注册申请人提交的自行取得且未披露的试验数据和其他数据,给予一定的数据保护期,从知识产权这一角度来鼓励罕见病药品的研发。
4.2.3 需求型政策工具运用不足需求型政策工具仅占所有政策工具的8.97%。现阶段主要是通过医保支付措施来拉动罕见病用药及诊疗。2012年,原卫生部牵头发布的《关于做好2012年新型农村合作医疗工作的通知》优先将血友病等12个病种纳入大病保障试点范围;2019年,国家医保目录调整中重点考虑罕见病等重大疾病治疗用药,据统计,121种罕见病治疗药物中,目前已在我国上市且有适应症的50余种药品中,已有40余种纳入了国家医保药品目录。[15]
5 建议 5.1 重视供给型和环境型政策工具,加强罕见病防治与管理在提升罕见病诊疗水平层面,资金投入与基础设施建设等政策工具使用频率最低,政府应充分发挥供给型政策工具的作用,通过资金投入加强罕见病医疗卫生资源建设和临床研究,重视罕见病诊疗人才队伍建设,提升医务人员对罕见病的临床筛查和诊疗能力,为罕见病患者提供及时有效的医疗服务。政府还应充分发挥环境型政策工具的作用,推动罕见病管理工作的制度化与规范化,运用好罕见病诊疗服务信息系统,做好罕见病目录的动态更新,只有深入了解罕见病发病基数、费用情况,才能为企业罕用药研发、为药监部门对罕见病新药监管准入、为保障政策制定提供依据,如欧洲的Orphanet罕见病登记平台[16],通过收集罕见病相关知识和数据,提升对罕见病患者的诊断和治疗能力,为患者、医疗和药品研发搭建桥梁。有研究指出,罕见病患者的生活质量评价低,社会支持对改善罕见病患者各维度生命质量的评价具有促进作用[17],政府应运用好宣传推广等需求型政策工具,普及罕见病科普知识,加大社会宣传力度,建设社会支持性环境,让公众认识和了解罕见病,关爱并帮助罕见病患者及家庭。
5.2 优化现有政策工具结构,促进罕见病药品的研发、上市与使用我国罕见病药物研发和仿制的水平仍然较低,政府应充分利用资金投入、金融支持、知识产权保护、政府购买、医保支付等政策工具,为罕见病药品的研发、上市与使用提供可持续发展动力。通过美国、欧盟等颁布的罕见病药品研发激励制度可知,政府研发资助、税收减免、注册费用减免和市场独占政策,都成为了激励医药企业研发罕见病药物强有力的手段。[18-20]目前,我国并没有设立独立的罕见病药物资格认定流程,而是将其作为一种类型进行申报,我国可以效仿欧美国家,设立专门的罕用药管理机构,如美国FDA于1982年就设立了孤儿药开发办公室(OOPD),负责审评用于罕见病的药品、生物制品、医疗器械等。
5.3 以政府为主导,健全罕见病保障机制医保、财政和民政等部门还需要进一步加强关于罕见病保障类的政策力度。为提高罕见病患者的保障水平,政府在探索多方支付机制,如大病保险、医疗救助、慈善救助、补充商业保险等。[15]2020年,中共中央国务院关于深化医疗保障制度改革的意见也明确提出要“探索罕见病用药保障机制”。中央层面还未出台详细具体的实施方案,尽管有地方对罕见病保障作出有益探索,但大部分地区对罕见病的保障还存在政策未涉及、覆盖病种少、支付待遇低等问题,不同地区的保障方式也存在差异,急需出台国家层面的指导政策,推动建立可持续的罕见病保障机制。
5.4 统筹安排,加强协同,完善罕见病政策体系我国罕见病领域正迎来良好的发展机遇,需要注重政策的统筹性和系统性。要实现罕见病诊疗、药品可及性和保障水平的提升,仅依靠卫生健康部门、药监部门和医保部门单打独斗,只能是碎片化政策的堆砌,并不能解决根本问题。要推动我国罕见病药品产业的发展,需要产业政策的有力支持,包括财税政策、金融政策、投资政策、科技政策、人才政策、信息政策、市场政策等,涉及不同的政策主体。在保障体系的建设上,医保、医疗救助、慈善救助和商业保险等方面分属于不同的主管部门,相互之间如果缺乏有效协调,在人群覆盖上可能会存在既有交叉又有断档的现象,因此在罕见病保障工作领域,已有学者提出,要在国家或省市层面,成立独立的罕见病工作委员会(包括民政、卫生、医保、药监、慈善机构和科研部门等)。[21]完善罕见病政策体系,需要在国家层面统一规划、统筹安排,围绕罕见病政策目标和实施过程不断地调整、优化,加强多部门之间有效协同,政策之间的关联协调,形成整体合力,真正发挥政策体系和政策工具对罕见病诊疗、用药和保障等的支持和推动作用。
作者声明本文无实际或潜在的利益冲突。
| [1] |
重磅|国家首批罕见病目录公布, 7位专家解读[EB/OL]. (2018-05-23)[2020-10-27]. http://www.chinadevel-opmentbrief.org.cn/news-21368.html
|
| [2] |
林苗苗, 肖思思, 廖君, 等. 罕见病患者的三道难题[EB/OL]. (2019-02-28)[2020-10-27]. http://m.xinhuanet.com/bj/2019-02/28/c_1124176063.htm
|
| [3] |
司建平, 郭清, 王先菊, 等. 政策工具视角下我国医养结合政策文本研究[J]. 中国卫生政策研究, 2020, 13(6): 49-55. |
| [4] |
熊烨. 政策工具视角下的医疗卫生体制改革: 回顾与前瞻——基于1978-2015年医疗卫生政策的文本分析[J]. 社会保障研究, 2016(3): 51-60. |
| [5] |
丁煌, 杨代福. 政策工具选择的视角、研究途径与模型建构[J]. 行政论坛, 2009, 16(3): 21-26. |
| [6] |
Rothwell R, Zegveld W. An assessment of government innovation policies[J]. Review of Policy Research, 1984, 3(3-4): 436-444. DOI:10.1111/j.1541-1338.1984.tb00138.x |
| [7] |
陈永法, 伍琳. 我国罕见病界定标准初探[J]. 中国卫生政策研究, 2014, 7(10): 16-20. |
| [8] |
孙思萌, 孙梦婷, 王高玲. 基于政策工具量化分析的我国罕见病医药保障政策研究[J]. 现代医院管理, 2019, 17(5): 28-31, 63. |
| [9] |
信枭雄, 管晓东, 史录文. 基于5种罕见病可负担性评价的我国罕见病保障机制研究[J]. 中国药房, 2014(5): 404-407. |
| [10] |
赵艺皓, 王翔宇, 丁若溪, 等. 罕见病疾病负担研究进展与医疗保障政策的方向抉择[J]. 中国卫生事业管理, 2018, 35(9): 644-648, 656. |
| [11] |
陈馨仪, 符晓, 王安石, 等. 罕见病患者治疗及保障研究[J]. 卫生经济研究, 2020, 37(9): 40-42, 46. |
| [12] |
中国罕见病医疗保障城市报告2020[EB/OL]. (2020-11-16)[2020-12-25]. https://mp.weixin.qq.com/s/ycksmXEcTlw7wj6RwWSvbw
|
| [13] |
中国"天价"进口药诺西那生钠注射液的前世今生[EB/OL]. (2019-10-18)[2020-12-27] https://med.sina.com/article_detail_103_2_72889.html
|
| [14] |
2019年度药品审评报告[EB/OL]. (2020-07-30)[2020-12-28]. http://www.cde.org.cn/news.do?method=viewInfoCommon&id=68f4ec5a567a9c9a
|
| [15] |
国家医疗保障局对十三届全国人大三次会议第6365号建议的答复[EB/OL]. (2020-10-13)[2020-10-28] http://www.nhsa.gov.cn/art/2020/10/13/art_26_3714.html
|
| [16] |
Orphanet[EB/OL]. [2020-12-28].https://www.orpha.net/consor/cgi-bin/index.php?lng=EN
|
| [17] |
高嘉敏, 马正. 罕见病患者社会支持与生命质量的关系研究[J]. 中国卫生政策研究, 2020, 13(4): 38-44. |
| [18] |
信枭雄, 管晓东, 陈敬, 等. 国内外孤儿药注册制度比较研究[J]. 中国药学杂志, 2013, 48(15): 1323-1328. |
| [19] |
张奇林, 宋心璐. 美国罕用药市场的激励机制及其启示[J]. 中国卫生政策研究, 2016, 9(2): 36-44. |
| [20] |
王红, 武志昂. 欧美孤儿药研发激励政策及对我国的启示[J]. 中国新药杂志, 2015, 24(15): 1681-1685, 1693. |
| [21] |
何江江, 张崖冰, 夏苏建, 等. 欧盟罕见病保障体系及启示[J]. 中国卫生政策研究, 2012, 5(7): 52-59. |
(编辑 薛云)




