药品价格谈判是世界各国针对专利药、原研药等高价特殊药品的定价方式,已成为降低药价、提高患者用药可及性和保障医保基金平衡的国际惯例。纵观发达国家药品价格谈判实践情况,大多在协议中针对销量、疗效、患者人群等因素进行不同的支付安排,通过机密折扣、返利等方式实现机密定价,既保护了制药企业的商业信息,避免国际市场的药价连锁反应,又缓解了医疗费用支付方的支付压力。
以加拿大品牌药价格谈判的非正式省级政府间联盟——泛加拿大制药联盟(Pan-Canadian Pharmaceutical Alliance,pCPA)谈判为例,由于谈判达成的协议——意向书(Letter of Intent,LOI)和药品收录协议(Product Listing Agreement,PLA)以返利的方式形成机密折扣,并配以相应的保密条款,因此加拿大已成为全球运用药品价格保密协议最为成熟的国家之一。
本文通过介绍加拿大pCPA谈判药品返利协议的签订机制,并具体研究返利协议条款,分析其价格保密设定方式和保密要求,以期为我国医保谈判药品的价格保密协议设计提供借鉴。
1 泛加拿大制药联盟简介泛加拿大制药联盟(pCPA)成立于2010年8月,前身是泛加拿大药品定价联盟(Pan-Canadian Pricing Alliance,pCPA),旨在利用各省/地区的联合谈判能力以及联合购买力,增加患者的治疗选择,降低药品价格和实现一致定价,减少重复谈判,提高资源利用率。[1]
pCPA是加拿大进行公共医疗保险品牌药价格谈判的非正式省级政府间联盟,现已覆盖加拿大13个省和地区。截至2019年9月30日,pCPA已完成321个药品的联合谈判。[2]据pCPA估计,所得药价折扣每年将节约公共医疗保险药品支出4.9亿加元。[3]
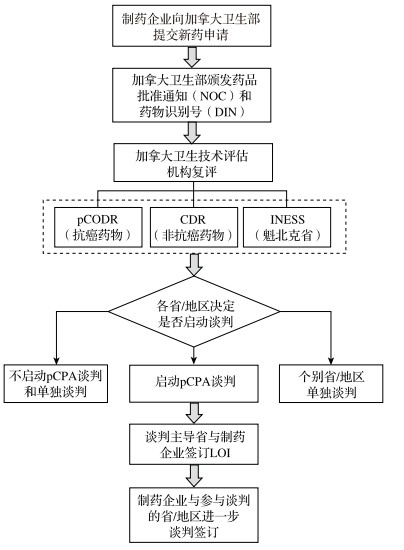
2 pCPA谈判药品返利协议签订机制pCPA谈判药品若要签订最终协议,需经历卫生部审核、卫生技术评估和推荐、启动pCPA谈判和签订返利协议4个步骤(图 1)。
|
图 1 加拿大药品收录协议签订机制 |
品牌药要通过谈判实现真正落地,首先要通过加拿大卫生部对其安全性、有效性以及质量的审核。审核通过后,品牌药会获得卫生部颁发的药品批准通知(Notice of Compliance,NOC)和药物识别号(Drug Identification Number,DIN)。
2.2 卫生技术评估和推荐品牌药获得上市批准后,由加拿大卫生技术评估局(Canadian Agency for Drugs and Technologies in Health,CADTH)负责对新药进行卫生技术评估,根据专家委员会的建议推荐各省/地区(魁北克省使用国家健康与社会服务卓越研究所(INESSS)推荐的目录为报销药品参考目录)将药品纳入公共药品计划。其中,药品统一审评(Common Drug Review,CDR)负责非抗癌药物的评价,泛加拿大抗肿瘤药物评审(pan-Canadian Oncology Drug Review,pCODR)负责抗癌药物的评价。
CADTH从临床效果和经济性综合考虑,对是否将药品列入省级报销目录,其推荐结果可分为“推荐列入”、“推荐有条件列入”、“不推荐以当前提交价格列入”和“不推荐列入”。[4]
2.3 启动pCPA谈判一旦CATDH或INESS发布其最终建议,pCPA将决定是否对该药品进行联合价格谈判。如果决定通过pCPA进行谈判,联盟中的一个省/地区将作为谈判主导省,代表所有有意愿参与的省/地区进行谈判。[5]不参与pCPA谈判的省份/地区也可以与制药企业单独谈判。
整个pCPA谈判过程是保密的。pCPA办公室、参与谈判的省/地区与制药企业之间讨论的价格信息、预算影响评估以及其他敏感信息将被保密,除非符合相关法律规定或谈判双方同意,否则这些信息不会被披露。
2.4 签订返利协议——LOI和PLA制药企业和谈判主导省在初始谈判达成协议后签订LOI。LOI是规定了制药企业返还利润方法、公式及保密要求的返利协议,但没有法律强制力。
由于pCPA谈判签订的LOI是没有法律强制力的返利协议,不规定收录时限,所以在签订LOI后,由各参与pCPA谈判的省/地区通过进一步谈判与制药企业签订具有法律效力的PLA。[6]最终,谈判结果以保密协议形式予以确权,实现双方权利义务关系的对等。[7]
3 pCPA谈判药品返利协议分析制药企业与pCPA谈判主导省初始谈判达成协议后签订LOI,罗列价格条款和药品收录条件。谈判后,每个参与谈判的省或地区决定是否通过其公共药品计划为该药品提供报销。如果决定纳入公共药品计划,该省或地区将根据LOI达成的条款,与制药企业进一步进行药品收录谈判并签订PLA。
3.1 意向书LOI是pCPA谈判主导省与制药企业谈判达成一致后签订的协议书,由pCPA提供协议书模板,谈判主导省根据LOI模板拟定协议书。
3.1.1 协议主要构成LOI协议书由正文和附录组成,模板正文包括制药企业的名称、地址、联系方式以及谈判药品的名称、药物识别号(DIN)、谈判参与的联邦/省/地区药物计划以及谈判主导省。[8]附录由11个部分组成,共有27条(表 1)。
| 表 1 LOI附录构成 |
LOI通过返利的方式形成机密定价,而药品的公开价格——药品出厂清单价(list price)则不受影响。其模板中规定了两种类型的返利方式。
第一种为制药企业每季度或者每半年或者每一年向各省/地区返还药品折扣费用,费用计算公式如下:
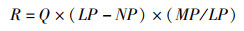
|
其中,R为返利金额;Q为该省/地区使用的药品总数;LP为每单位药品的出厂清单价;NP为净价;MP为给定剂量允许的最高报销价格,包括允许的加价但不包括配药费用。
第二种返利方式为增量返利(incremental rebate),指在一个支付年度内(自PLA协议生效后每12个月为一个支付年度)某省药品年度支出超过设定的阈值后,制药企业会提供额外的返利。每个谈判的省/地区需要根据实际情况列出协议期3年内所报销的药品数量阈值,并列出PLA期间的产品增量返利计算公式。增量返利通常作为给支付者提供预算确定性的机制,所以不一定会在LOI中使用。
3.1.3 价格保密要求(1) 保密内容
LOI协议附录中的第8部分对保密要求做了详细规定。除法律要求外,LOI和与此LOI有关的谈判信息应由制药企业和参与省/地区保密,不得向任何第三方披露。
参与谈判的省/地区或pCPA办公室可以公开宣布参与省/地区和制造企业已达成LOI,可以公开的内容包括药品信息和报销标准,但是不会透露除药品清单价之外的LOI中的任何财务或定价信息。
(2) 保密对象
保密对象为除制药企业和参与省份以外的任何第三方,包括但不限于任何其他制药企业,或任何非参与的公共或私人药物福利计划。
(3) 保密期限
pCPA谈判签署的LOI没有法律强制力,也不规定收录时限。在签署LOI之后,各参与谈判的省/地区需要与制药企业进一步协商确定PLA的协议期限。
(4) 披露方式
LOI可按照各自省级信息自由和隐私法保护的规定进行有关信息披露。
3.2 药品收录协议经过pCPA谈判的药品,各省在签订PLA时可以在LOI的基础上对返利公式进行调整,以便返利在本省能更好地实施。新药在HTA审查之后,各省与制造商谈判签订PLA已成为公共药物计划越来越常见的策略。[9]
各省对PLA的协议格式、签订要求、返利方式、保密要求、执行方式等均有不同的规定。标准的PLA协议有效期为3年。
曼尼托巴省PLA协议针对的是经过pCPA谈判并签署LOI协议的药品,本部分以曼尼托巴省PLA模板为例分析其协议条款以及协议内容保密机制。
3.2.1 协议构成新药在列入曼尼托巴药物福利和互换性处方集之前,除了要通过国家药物审查(CDR和pCODR)外,还要通过曼尼托巴药物标准与治疗委员会(Manitoba Drug Standards and Therapeutics Committee,MDSTC)的审查。制造商必须向MDSTC进行资料提交。
对于考虑列入曼尼托巴药物福利和互换性处方集的所有药物,制造商必须签署PLA。根据MDSTC的建议,曼尼托巴省卫生部负责和制造商协商签署PLA,卫生部部长通过签署特定药物法规和曼尼托巴药物福利和互换性处方集,最终批准Pharmacare药物福利计划。[10]
曼尼托巴省PLA正文包含15个部分,共55条,在LOI的基础上对其进行修改和补充,并将LOI和“正在进行的上市要求”作为PLA的附录。[11]
正文对协议生效和终止日期、早期终止及其义务、返利方式的计算、清单价、返利义务、保密义务、披露要求等作了详细规定(表 2)。
| 表 2 曼尼托巴省PLA条款构成 |
由于曼尼托巴省的PLA是根据LOI设计的,所以也是通过返利的方式进行机密定价。曼尼托巴省可以根据本省实际情况对LOI中的返利公式进行调整,以便制药企业的返利能在本省更好地实施。
3.2.3 价格保密要求(1) 保密内容
曼尼托巴省可以披露某一具体药品协议的存在,但不包括协议中包含的任何财务信息(可公开的清单价除外)。
“财务信息”包括有关根据协议及其附表应付的任何金额的所有信息,包括时间、金额和此类返利的计算方法、此类返利的任何公式,以及可能导致间接计算或识别此类信息的任何其他信息。
(2) 保密对象
制造企业不得向公司的员工、代理商、代表和承包商以及公司关联公司的员工、代理商、代表和承包商以外的任何第三方披露返利数据,并且上述主体利用返利数据是为了向制造企业提供建议或是为了使制造企业遵守协议规定的义务。
(3) 保密期限
虽然曼尼托巴省PLA中会规定协议生效和终止日期,但相关返利条款在协议到期后保密要求仍保持不变,不会因为协议终止而被披露。
(4) 披露方式
曼尼托巴省规定在以下三种情况下,若一方需要披露协议中包含或与之相关的任何和所有信息(包括协议附表)是允许的,但需要遵守本省的披露程序:
(a) 任何适用法律要求,包括但不限于省级信息获取的法律和审计长的立法;
(b) 由法院命令;
(c) 另一方提供书面同意在其允许的范围内进行披露。
(5) 违约救济
曼尼托巴省PLA中规定,若发生公司信息披露,仅凭损害赔偿金不足以作为补救措施,公司除法律规定的任何其他可用补救措施外,还可寻求宣告性救济。
3.2.4 协议执行方式加拿大各省/地区主导本辖区内的返利事项。在加拿大,PLA的返利可以直接进入政府公共药品计划,或者到卫生部门内的财务部门,甚至到所有政府支付的通用账户。极少数情况下制造商会返利至特定的医院(图 2)。

|
图 2 加拿大PLA协议返利执行方式 |
曼尼托巴省规定,省卫生部按照回款时间表根据协议中列出的回款公式计算制造商应还费用,公司应在收到曼尼托巴省卫生部书面回款通知后30天内向曼尼托巴省卫生部支付所有返利。
4 我国医保谈判药品价格保密协议现状自2015年以来,我国已开展了四次国家药品谈判,在降低药品价格上取得了一定成效。前三次国家药品谈判均将谈判达成的价格或医保支付标准对外公开,可能会造成全球药品价格的连锁反应,不利于制药企业的发展。
在2019年国家医保药品谈判中,国家医保局明确“对于谈判成功的药品,如企业申请保密,国家医保局可采取措施,官方不主动公布谈判药品支付标准(如有法律规定的除外),并在协议文本中予以明确”。[12]从谈判结果来看,共有47个药品的支付标准在协议期间是不公开的,反映了我国已经意识到维护全球药品价格体系的重要性。
在实际操作中,我国药品采购是由各地区自主完成。根据国家医保局和国家卫健委联合下发的《关于做好2019年国家医保谈判药品落地工作的通知》规定,要求各省(区、市)药品集中采购机构在2019年12月底前将97个谈判药品在省级药品集中采购平台上直接挂网。[13]随着通知下发,各地陆续将97个药品直接挂网采购,而其中有价格保密的47个药品的价格也随之曝光。
因此,虽然我国已开始尝试建立药品价格保密机制,国家医保局与相关企业在协议文本中明确了保密的义务,保密机制形同虚设。保密价格只是官方不公布,一旦药品挂网,保密的价格在地方层面仍然面临被披露的风险。
5 启示与建议采用药品返利协议可以解决当前我国药品直接挂网采购所导致的医保谈判药品价格保密无法落实的问题,且可以提供多种方式帮助医保部门有效运用医保基金,减少基金财务风险,同时加强药品的临床合理用药。然而返利协议在执行中需要制药企业向政府部门返还清单价与实际支付价格的差额,由于我国的药品采购以及医保支付是由各统筹地区自主进行,涉及地方医保基金经办机构、医疗机构医保办和采购等多个部门。因此,若在我国实施返利协议,返还至哪个部门,返还的金额用于何处是亟待考虑的问题。
我国的谈判药品实行价格保密机制刚刚起步,为发展我国医保药品谈判价格保密协议,本文从以下三个方面提出建议:
5.1 借助返利建立价格保密机制我国医保药品谈判方式采用的是协议定价,即政府和制药企业之间通过谈判而形成购买合同。医保药品谈判协议是在机关法人和盈利法人作为医保药品买卖双方的平等主体在价格博弈、为自己争取最大利益后达成的契约,药品谈判价格既是协议的核心也是企业的商业秘密,因此协议签订双方有必要就谈判价格规定双方的保密义务,对保密条款达成一致意思表示。
通过机密折扣或返利等方式而使制药企业在平等自愿的基础上让出部分利润,并在谈判协议中辅以相应的保密要求是全球通行的定价策略。我国可借鉴加拿大保密协议的实践,借助返利的形式建立谈判药品价格保密机制,提高药品降价的科学性和合理性。
5.2 规范谈判协议格式一个科学、规范的药品谈判协议是落实谈判的重要途径,也是保护各方权益的法律依据。谈判药品保密协议的设定应当在机密性和透明度两者平衡的基础上明确协议的原则、折扣或返利方式、协议期限、保密义务及救济措施等内容,在谈判双方平等协商的基础上形成一致,保证谈判药品价格的可持续性。
5.3 引入第三方评估机构药品价格谈判协议的关键是合理分担临床与经济不确定。在缺乏国家层面的卫生技术评估机构的情况下,我国可以引入第三方评估机构,通过卫生技术评估的手段对谈判药品进行临床和效益价值的评估,以评估结果作为医保部门进行谈判和协议制定的依据,从而提高价格保密协议的可行性和公平性。
作者声明本文无实际或潜在的利益冲突。
| [1] |
Pan-Canadian Pharmaceutical Alliance. pCPA Brand Process Guidelines[EB/OL]. [2020-10-28]. http://www.canadaspremiers.ca/wp-content/uploads/2019/04/pCPA_Brand_Process_Guidelines_FINAL.pdf
|
| [2] |
Pan-Canadian Pharmaceutical Alliance. Pan-Canadian Pharmaceutical Alliance: Completed Negotiations[EB/OL]. [2020-10-28]. https://www.canadaspremiers.ca/wp-content/uploads/2019/10/PCPA_completed_negotiations_2019-09.pdf
|
| [3] |
常峰, 席悦, 李世勇, 等. 加拿大品牌药价格联合谈判机制及其对我国的启示[J]. 价格理论与实践, 2016, 381(3): 85-88. |
| [4] |
周挺, 李洪超, 马爱霞, 等. 加拿大药品统一审评制度及价格管理体系简析[J]. 中国卫生经济, 2018(2): 94-96. |
| [5] |
Milliken D, Venkatesh J, Yu R, et al. Comparison of drug coverage in Canada before and after the establishment of the pan-Canadian Pharmaceutical Alliance[J]. Bmj Open, 2015, 5(9): e008100. DOI:10.1136/bmjopen-2015-008100 |
| [6] |
Husereau D, Dempster W, Blanchard A, et al. Evolution of drug reimbursement in Canada: the Pan-Canadian Pharmaceutical Alliance for new drugs[J]. Value in Health, 2014, 17(8): 888-894. DOI:10.1016/j.jval.2014.08.2673 |
| [7] |
陶田甜, 黄秋雨, 侯立丽, 等. 加拿大、澳大利亚专利药谈判模式对我国的启示[J]. 中国卫生资源, 2019, 22(5): 391-396. DOI:10.3969/j.issn.1007-953X.2019.05.016 |
| [8] |
Pan-Canadian Pharmaceutical Alliance. LOI Template[EB/OL]. [2020-10-28]. http://www.canadaspremiers.ca/wp-content/uploads/2018/05/LOI_Template.pdf
|
| [9] |
Morgan S G, Friesen M K, Thomson P A, et al. Use of product listing agreements by Canadian provincial drug benefit plans[J]. Health Policy, 2013, 8(4): 45-55. |
| [10] |
Government of Manitoba. Drug Benefits & Interchangeability Formulary[EB/OL]. [2020-09-02]. https://www.gov.mb.ca/health/mdbif/review.html
|
| [11] |
Government of Manitoba. Product Listing Agreement[EB/OL]. [2020-09-02]. https://www.gov.mb.ca/health/mdbif/docs/pla.pdf
|
| [12] |
国家医保局, 人力资源社会保障部. 关于将2019年谈判药品纳入《国家基本医疗保险、工伤保险和生育保险药品目录》乙类范围的通知[EB/OL]. (2019-11-22)[2020-09-02]. http://www.nhsa.gov.cn/art/2019/11/28/art_37_2050.html
|
| [13] |
国家医保局, 国家卫生健康委. 关于做好2019年国家医保谈判药品落地工作的通知[EB/OL]. (2019-12-16)[2020-09-02]. http://www.nhsa.gov.cn/art/2019/12/18/art_37_2181.html
|
(编辑 薛云)





