随着人口老龄化和疾病谱变化,全球范围内尤其是发展中国家的癌症负担呈现加重的趋势。[1]世界卫生组织(WHO)《2020年世界癌症报告》指出,我国新增癌症病例占全球的23%以上,死亡人数约占全球的30%。[2]恶性肿瘤已经成为威胁我国居民健康水平的重要因素。2006年,WHO首次明确将肿瘤疾病归入慢性病的范畴,指出患者通过接受及时有效的治疗其病情可以得到有效控制。当前,药物治疗是恶性肿瘤患者生活质量提升和疾病治愈的重要手段。
我国抗肿瘤药市场发展迅猛、规模庞大,进口药仍占据较大比重。我国为提升患者抗肿瘤药的可及性采取了多项举措。自2015年首批国家药品价格谈判试点以来,我国通过五轮价格谈判将抗肿瘤药等一系列临床价值高、价格相对高昂的独家药品纳入医保, 同时降低抗癌药的进口关税、增值税等,有效降低了患者的疾病经济负担。2019年国家卫生健康委等10部门联合制定的《健康中国行动—癌症防治实施方案(2019—2022年)》(以下简称“《癌症防治方案》”)鼓励境内抗肿瘤药的研发和加速审批,促进境外抗肿瘤新药的同步上市,实现抗肿瘤药可及性的提升。未来,我国抗肿瘤新药的发展即将进入“加速期”,促进抗肿瘤新药研发的激励政策以及加速新药上市的审评审批制度有待进一步完善。
2 资料与方法 2.1 “新药”概念的界定我国与美国、日本在“新药”概念的界定上有一定的差异,因此需先明确本研究中涉及的“新药”概念。2019年,我国化学药品注册分类采用2016年版《化学药品注册分类改革工作方案》(以下简称“《改革方案》”),我国对“新药”的定义包含了化学药1类(境内外均未上市的创新药)及5.1类(境外上市的原研药品)、生物制品1类(未在国内外上市的生物制品)及2类(单克隆抗体)、中药和疫苗;美国食品药品监督管理局(U.S. Food and Drug Administration, FDA)将“新型药物(Novel Drug)”定义为“药品中含有的新分子实体(New Molecular Entities, NMEs)的药物和新治疗性生物产品”,不包含疫苗、致敏产品、血液和血液制品、血浆衍生物、细胞和基因治疗产品[3];日本医疗器械审评审批机构(Pharmaceuticals and Medical Devices Agency, PMDA)在《上市药品清单》(List of Approved Products)中对上市新药评审类别也进行了详细的类别划分,将“新药”定义为具有新有效成分或化学结构,以及因剂型、规格、给药途径的变化导致药理作用发生改变的药物,主要包括具有新的活性成分、具有新的适应证、具有新的剂型、具有新的给药途径等[4]。综合各国对“新药”的评判标准,本研究纳入的“新药”指:在本国境内未上市的、药品中含有的新分子实体的药物和新治疗性生物产品,包括2019年我国适用的《药品注册管理办法》规定的化学药1类及5.1类、生物制品1类及2类、中药三大类别的药品,不包括疫苗、致敏产品、血液和血液制品、血浆衍生物、细胞和基因治疗产品。
2.2 数据来源基于中国、美国和日本2019年药品上市数据,针对符合“新药”标准的药品数量、原研厂家以及抗肿瘤新药的适应证、原研厂家、上市时效性等情况进行对比分析;数据源于美国食品药品监督管理局、日本医疗器械审评审批机构及我国的药品监督管理局官网。与肿瘤医院科室、药剂科、制药企业等利益相关方负责人开展深入访谈,了解我国抗肿瘤新药在研发和上市审批环节存在的问题,总结我国创新药发展的现状和挑战,结合国内外优秀经验提出政策建议,以推动我国抗肿瘤药的创新和发展。
3 结果 3.1 美国、日本与我国新药上市情况对比美国在药品研发领域拥有完整创新链与产业链,药品研发创新能力一直处于世界领先水平,美国FDA在支持鼓励新药的研发和上市方面也长期走在世界前列。日本则通过对国外先进药品的仿制实现自身研发技术的提升,当前也已步入药品研发强国的行列。[5]本研究从我国药监局、美国FDA和日本PMDA和官网获取2019年各国上市药品数据及药品分类标准,对比分析各国上市新药数量和研发企业的分布,以了解我国在创新药品上市和研发方面与国际先进水平的差异。
3.1.1 上市新药数量分析2019年,我国审批上市新药58个,其中抗肿瘤药14个,占比24.14%;美国FDA审批上市新药48个,其中抗肿瘤药12个(包含1种诊断用放射性显影剂),占比25.00%;日本PMDA批准上市新药37个,其中抗肿瘤药10个,占比27.03%(表 1)。
| 表 1 2018、2019年中美日三国新药上市情况 |
从上市审批新药的数量来看,2019年我国首次超过美国,我国在药品上市审批领域与国际领先水平的差距正逐渐缩小。在上市审批的药品中,我国抗肿瘤药的比例与日本和美国的水平接近,在《癌症防治方案》“加快境内外抗癌新药注册审批,促进境外新药在境内同步上市,畅通临床急需抗癌药临时进口渠道”的要求下,上市的58个新药中包含抗肿瘤新药14个,继2018年17个国家谈判抗肿瘤药进入医保提升患者的用药可及性之后,国家进一步加大对抗肿瘤药的研发和对临床急需新药的引进,从用药源头上提升患者的用药可及。
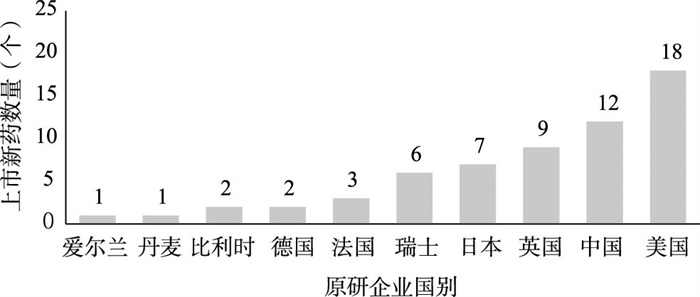
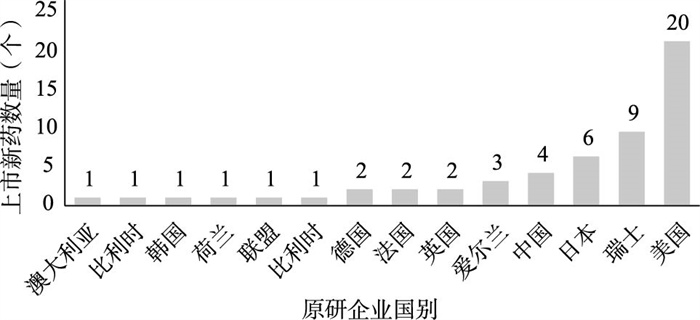
3.1.2 上市新药原研企业分布从新药原研企业的分布来看,我国上市的58个药品涵盖10个国家原研企业生产的产品,其中美国企业生产的药品最多,共18个,占比30.61%;其次为中国企业生产的药品,共12个,占比20.69%(图 1)。美国上市的48个药品涵盖14个国家的企业和组织生产研发的药品,美国企业生产的药品最多,共20个,占比41.67%;其次为瑞士企业生产的药品,共9个,占比18.75%(图 2)。从上市新药的企业分布来看,我国2019年上市的药品中,美国研发的创新药物仍占据较高的比例,而在国家新药政策的激励下,国产新药未来也将成为我国上市新药的重要来源;从上市新药的国际影响力来看,美国企业研发的药品仍在各国上市新药中占据较大的比重,而我国研发的药品在各国的占比相对较低,尽管我国的药品研发能力正逐步提升,但上市药品的国际影响力有待进一步增强。
|
图 1 2019年中国上市新药生产国分布 |
|
图 2 2019年美国上市新药生产国分布 |
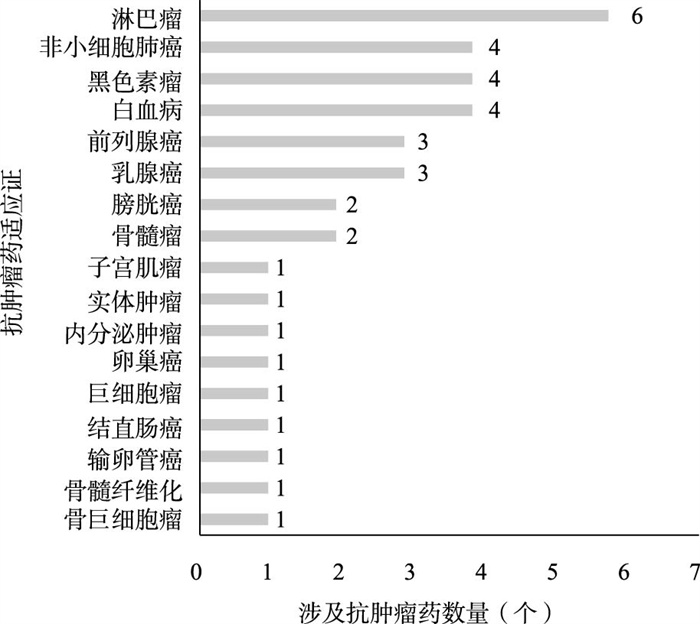
聚焦各国上市的抗肿瘤新药,2019年美国、日本和我国共上市抗肿瘤新药33个,其中有三款药品涉及两种癌症适应证,共涉及17个癌种,对应药品数量排名前三的癌种分别是淋巴瘤(16.22%)、非小细胞肺癌(10.81%)、黑色素瘤和白血病(图 3)。
|
图 3 2019年三国上市抗肿瘤新药癌种分布 |
我国上市的14个抗肿瘤药中肺癌、前列腺癌、淋巴瘤和黑色素瘤的占比最高,各涉及两个药品;美国上市的12个抗肿瘤药中乳腺癌、膀胱癌、淋巴瘤的药品占比最高,各涉及两个药品;日本上市的10个抗肿瘤药中肺癌的药品占比最高,共涉及三个药品。对比我国与美国、日本2019年上市抗肿瘤新药及适应证,我国与日本有达可替尼(Dacomitinib,商品名:Vizimpro)和阿帕他胺(Apalutamide,商品名:Erleada)两款药品均在2019年获批了相同的适应证;而美国和日本虽然都批准了罗氏制药(Roche)研发的广谱抗癌药恩曲替尼(Entrectinib,商品名:Rozlytrek),但在美国获批的适应证是非小细胞肺癌,在日本获批的适应证是慢性淋巴细胞白血病和小淋巴细胞淋巴瘤(表 2)。表明各国在选择药品及适应证上市审批时,尤其是临床需求较高的重点品种的审批过程中,考虑的因素会有所区别。除了兼顾临床治疗需求、药品的卫生经济学价值以及医保基金的使用可持续性[6],各国也将疾病谱及药品在本国临床研究数据等因素作为决策的重要依据,优先审批符合其药品评价体系的药品及适应证上市。
| 表 2 2019年中美日三国抗肿瘤新药上市情况 |
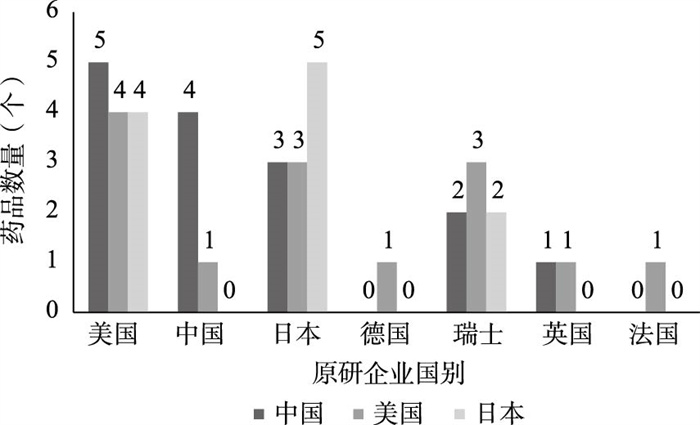
从上市抗肿瘤药的原研企业分布来看,2019年我国上市的14个抗肿瘤药涉及5个国家的原研企业,其中美国企业数量最多,共5个药品(占比35.71%);2019年美国上市的12个抗肿瘤药涉及7个国家的原研企业,其中美国的企业数量最多,共4个药品(占比36.36%);2019年日本上市的10个抗肿瘤药涉及日本、美国、瑞士3个国家的原研企业,其中日本企业数量最多,共5个药品(占比50%)(图 4)。整体而言,三个国家2019年上市抗肿瘤新药中,美国企业参与研发的药品肿瘤最多,共13个,占比40.63%;日本企业参与生产的药品位居第二,共9个,占比28.13%。可见,2019年上市的抗肿瘤药中,美国企业仍是抗肿瘤新药研发的重要力量,日本在抗肿瘤药的研发方面也发挥了重要作用,而我国在抗肿瘤新药研发方面仍处于起步阶段,国产新药上市数量与国际先进水平仍存在一定的差距,上市药品的国际影响力也有待提升。
|
图 4 2019年三国抗肿瘤新药生产企业分布 |
从获批抗肿瘤新药的时效性来看,我国2019年上市的14个抗肿瘤新药中,氟马替尼(Flumatinib,商品名:豪森昕福)、卡瑞利珠单抗(Camrelizumab,商品名:艾立妥)、替雷利珠单抗(Tislelizumab,商品名:百泽安)3个国产创新药为全球首批;美国上市的12个抗肿瘤新药中,有泽布替尼等9个药品为全球首批;日本上市的10个抗肿瘤新药中,奎扎替尼(Quizartinib,商品名:Vanflyta)、瑞卢戈利(Relugolix,商品名:Relumina)、恩曲替尼3个药品为全球首批[7](表 3)。
| 表 3 2019年中美日三国全球首批抗肿瘤新药情况 |
对比2019年我国上市新药在美国和日本的上市情况,在我国上市的14个抗肿瘤药中,2019年之前有11个药品就已经在美国上市,其中甲磺酸艾立布林注射液和地舒单抗注射液2个药品早在2010年就已经在美国获批上市。日本则有8个药品在2019年之前上市,而甲苯磺酸尼拉帕利胶囊的上市时间晚于我国(表 4)。可见,尽管近年来我国多项政策均在加快境内外抗癌新药注册审批,但由于整体起步较晚,我国近年来批准上市的新药多为国际已经上市的进口原研药,在创新药审批上市的时效性方面与美国、日本仍有一定的差距。
| 表 4 2019年中国上市抗肿瘤新药别国上市情况 |
党的十八大以来,党中央高度重视科技创新并将创新作为引领发展的第一动力。[8]在党中央、国务院确立的创新驱动发展战略引领下,我国药品自主创新能力大幅提升。[9]自2016年《改革方案》发布实施以来,我国的药品注册制度不断改革调整,向着国外先进水平不断靠拢。一方面,药品注册制度明确“创新药”和“仿制药”在药品注册流程上的区别,对不同类别的新药设置了多项加速审批政策,同时也对新药的临床价值和安全性等方面提出了更高的要求,引导药品产业转型,鼓励具备自主研发能力的企业开展药品创新研发;另一方面,药品注册制度也为企业药品研发方向的确定和药品剂型的选择提供了一定的指导,并配合《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》等多项创新扶持政策,提出“药品专利链接制度”、“药品专利期限补偿制度”、“药品试验数据保护制度”等一系列创新药专利保护措施,维护创新研发企业的合法权益,保护企业的研发积极性。[10]在此背景下,2019年我国创新药物的研发取得了举世瞩目的成就,诸多全球首创成果的面世彰显我国药品创新研发能力的飞速提升。由中国百济神州自主研发的创新抗癌药泽布替尼(Zanubrutinib,商品名:Brukinsa)于2019年11月15日被FDA批准上市,成为我国历史上第一个完全由本土自主研发并获得FDA批准的国内创新药[11],该药也是首获美国突破性疗法认定的国内创新药。
自国家药品价格谈判开展以来,抗肿瘤药一直是各界关注的重点领域(表 5),尤其是2018年组织开展的抗癌药医保准入专项谈判,将临床急需的17个抗肿瘤独家药品纳入医保,显著降低了患者用药的经济负担,极大地满足了患者的临床需求。在与药企负责人的访谈中我们了解到,随着五轮国家药品价格谈判结果的落地实施以及《关于抗癌药品增值税政策的通知》、《癌症防治方案》等相关政策的发布,企业逐渐认识到研发抗肿瘤新药广阔的市场前景,并希望能够通过国家药品价格谈判降价进入医保,惠及更多癌症患者。未来,在诸多政策的大力扶持下,将有更多中国企业和外资企业投身抗肿瘤新药的研发。
| 表 5 2016—2020年五次国家药品价格谈判抗肿瘤药情况 |
从近年来我国的新药审批情况可以发现,当前我国医药产业发展不均衡现象明显,化学药的创新研发仍是我国医药产业的重要力量,生物药的创新研发势头近年来也较为迅猛,但中药的研发能力有待进一步加强;进口原研药在我国上市药品中仍占有较大比重,我国的创新药品在美国和日本的影响力相对有限。
我国新药研发基础相对薄弱,基础研究向应用的转化也较为匮乏;加之我国药企规模较小,无论是企业市值还是新药研发投入,与美国等药品研发强国企业相比存在明显差距。因此当前药物政策不仅要完善对研发成功新药的扶持和保护,更应注重对药品研发源头的激励和引导。在药品研发过程中,企业多根据政府出台的相关政策法规了解我国对药品研发方向的引导,而我国企业在药品研发与政府的前期沟通方面相对被动,许多企业对国家的创新扶持政策不够了解,导致研发动力不足,研发方向偏差,药品上市滞后,缺乏市场竞争力,进而影响企业的研发成本回收,阻碍企业新一轮的研发创新。国家药品价格谈判、临床急需境外新药等政策让企业认识到药品创新所带来的巨大市场潜力,而此类政策在执行过程中多以专家遴选的方式由政府向企业发出邀请,缺乏企业与政府的双向互动。
4.3 我国创新药上市数量接近国际先进水平,但上市药品的时效性有待提升从2019年各国上市新药的数量来看,我国已超过美国和日本,表明我国在新药的上市审批速度已经逐步向美国等国际先进水平靠拢。但分析我国上市抗肿瘤新药在美国和日本的上市情况,可以发现除氟马替尼、卡瑞利珠单抗、替雷利珠单抗三款国产抗肿瘤创新药,另外11个抗肿瘤药均已在国外上市,且在我国的上市时间平均落后美国4.6年、落后日本2.9年;从2019年抗肿瘤新药上市的时效性来看,美国获得全球首批的抗肿瘤新药数量和比例均为最高,极大缩短了患者接受新技术、新疗法、新药品的时间。
在诸多新药政策的大力支持下,我国2019年上市新药的数量已超过美国和日本,但由于之前与发达国家新药进口及上市审批效率存在一定差距,导致国外新药需要经过几年的时间才能在我国上市。在与临床专家的访谈中,专家表示接受及时有效的治疗是恶性肿瘤患者改善生存质量、延长生存期限的重要手段,及时使用疗效更好、安全性更高的抗肿瘤药对于提升患者健康水平具有重要意义。当前恶性肿瘤领域的研究发展迅猛,其治疗方案也在不断优化,医生在临床治疗过程中受到药品未在国内上市的限制,因此加速抗肿瘤新药的上市审批、提升上市抗肿瘤新药的时效性是我们亟待解决的问题。
4.4 药品的临床价值成为新药上市的重要影响因素从2016年《改革方案》对“创新药”概念的提出,到《临床急需名单》的频繁更新,再到2020年对《化学药品注册分类及申报资料要求》的调整可以看出,我国对药品临床价值的高度重视。基于前期在药品方面评审与国际先进水平方面存在差距,为满足患者的临床需求,通过制定《临床急需名单》加速境外已上市新药在国内上市,逐步实现从“滞后进口”到“同步上市”的过渡。通过2019年美国、日本与我国上市药品情况可以发现,各国在考虑是否上市某药品及上市何种适应证受到诸多因素的影响,不仅需要考虑各国疾病谱和临床需求,也受到各国药物政策的影响。同时,企业也会根据当地政策结合临床试验开展情况及市场发展前景等综合因素有针对性地制定各国的药品上市策略,其具体影响因素需进一步探讨。
5 建议 5.1 建立完善的创新药物政策体系,全流程鼓励抗肿瘤新药的创新研发为保证抗肿瘤新药的持续可及,政府不仅要重视新药的上市审批和医保准入,更应从源头上提升我国的药品创新研发能力,促进药品产业的全面发展。结合国际政策的先进经验,进一步强化对抗肿瘤药创新研发全流程的政策扶持,主要包括以下几个方面:
5.1.1 倡导研发税收减免政策国际上,政府多采用税收减免或税收优惠的方式以分担制药企业的研发风险,激励企业加大创新投入,研发投入增加越多则享受的优惠力度越大。我国针对科技型企业出台一系列税收减免政策,但针对抗肿瘤药品的税收减免政策主要集中在药品流通环节,尚未明确对抗肿瘤药研发阶段的税收优惠政策[12];企业负责人也提出,当前我国对制药企业的税收处于相对较高的水平,且中国企业和外资企业的税收政策也有所差异。在抗肿瘤领域飞速发展的背景下,我国应加速出台相关法律对符合条件的抗肿瘤新药研发企业实施税收抵扣或减免,减轻制药企业的财务压力,发掘企业的研发能力。
5.1.2 优化政府与企业的双向互动政府与制药企业建立双向互动机制能够实现政府、企业和社会的多方“共赢”,是发挥政府引导作用的途径之一。从2018—2019年公布的两批《临床急需名单》落实情况来看,74个药品中仅有26个药品批准上市或完成评审,且仍有11个药品无上市计划,6个药品未与企业取得联系。我国在2020年版《药品注册管理办法》中针对“突破性治疗药物”提出了企业与药品评审中心的“双向沟通”机制,抗肿瘤新药基本符合此类药物的界定。今后,政府需进一步明确抗肿瘤新药在研发、生产、上市审批及流通等环节的政策和要求,与具备研发能力的企业开展早期沟通,了解企业的研发意向和困难,有针对性地开展政策、技术上的指导,提高企业的研发意愿和药品的研发效率。而企业也应在此过程中主动与政府部门沟通,规避研发过程中的可控风险,反馈企业的困难和诉求,以促进政府更好地完善政策,形成良性循环。
5.1.3 平衡专利保护与鼓励仿制的关系专利保护不仅能保护企业的创新成果不受侵害,更是保护企业研发积极性的重要手段。在专利保护期内,企业可以快速占领市场,回收研发成本,实现研发的可持续发展,国际上多采用药品数据保护、延长专利保护期、限制仿制药上市等方法。我国在《中华人民共和国专利法》第四次修正中新增新药专利期补偿的规定,明确药品专利纠纷早期解决机制,重视和保障研发企业的合法权益。而药品仿制则将打破原研企业的垄断地位,通过竞争将药品价格降至相对较低的水平,患者的用药负担得以减轻。对临床急需的抗肿瘤新药而言,一味地延长专利保护期并不一定是鼓励企业创新的最佳手段,尽管国家药品价格谈判可以将这些独家药品降价纳入医保,但同类药物的研发企业由于研发进度滞后,专利申请晚于原研企业,在专利保护政策的影响下产品的上市时间将大大延迟,对制药企业发展造成沉重的打击。因此,在当前我国制药企业规模普遍不大的情况下,促使企业间的研发合作可以集中力量提升研发效率,同时也可以避免因竞争而造成研发成果滞后上市的损失;而研发效率的提升和成本的降低则可以为仿制药品的尽早上市创造条件。
5.2 完善创新药品审评审批制度,加速抗肿瘤新药进入流通市场 5.2.1 科学探索,优化加速审批机制优化药品的上市审批流程,探索建立安全、高效的加速审批流程是世界各国共同面临的问题。专家指出,当前我国对新药的审评主要关注其“一致性”,不符合创新药物的研发规律。[13]近年来,我国修订和出台多项政策缩短药品的上市审批时间,在加速审批环节提出了四种加速审批程序,抗肿瘤新药作为临床价值较高的品种也属于加速审批的范畴,但与欧美等国相比,我国在新药申报临床试验阶段的技术评审要求相对更高[13],这无形中又拉长了新药的审批周期。因此,在未来审评制度的优化过程中,一方面需要借鉴人用药品技术要求国际协调理事会(ICH)等相关国际指南修订我国的审评技术指南,提升我国药品审评的科学性和严谨性,为我国原研药品的国际化发展奠定基础;另一方面,加强对加速审批药品上市后临床数据的追踪和监测,既保证患者用药的时效性,更要注重药品的安全性。
5.2.2 政府主导,稳步推进《癌症防治方案》《癌症防治方案》的实施对提升我国癌症防治能力、居民的健康素养及健康水平具有重要意义,其中“实现境外抗肿瘤新药在我国的同步上市”受到社会各界的广泛关注。2020年9月29日,治疗非小细胞肺癌的新型靶向药普拉替尼(Pralsetinib,商品名:普吉华)在海南博鳌超级医院开出了美国之外的全球首张处方,是乐城先行区第一个实现国际同步上市、同步使用的创新抗癌药,让患者和外资企业看到了未来广阔的前景。该方案的推进离不开政府的主导作用,要实现药品的同步上市,更需要政府部门与外资企业的早期沟通,使企业了解到我国广阔的市场,在试验阶段注重对我国数据的收集,为新药同步上市奠定基础。而新药同步上市后要想真正的惠及患者,临床的诊疗技术也要随之更新,因此需要加强临床医生对新疗法、新技术的培训和学习,配合药品落地政策实现药品进院可及,打通患者用药的“最后一公里”。
5.3 建立多维度的药品价值评价体系,全面评估创新药品的价值以价值为基础的卫生决策受到多方因素影响,因此仅从经济学的角度对药品的价值进行评价往往是片面的,尤其是创新药。抗肿瘤新药除了有较高的临床价值,在创新价值、社会价值等方面也要高于普通药品,因此构建多维度的药品价值评价体系对创新药实现全面评价显得尤为重要。国际药物经济学与结果研究协会(ISPOR)于2014年成立工作组专门研究多准则决策分析(Multi-criteria Decision Analysis, MCDA)在卫生领域的应用,而我国学者也提出此方法对我国《药品目录》药品遴选具有重要意义。[14]2018年,ISPOR提出多维度的药物价值框架的概念,并提出社会关注、医保部门关注、患者关注三个维度、十二个指标的评价体系,可较为全面的评价药品的价值。[15]未来,我国可借鉴MCDA的思想开发适合于我国的创新药价值评价体系,并应用于上市审批制度的改革,针对抗肿瘤新药等创新药品明确加速审批程序的筛选标准,为抗肿瘤新药的加速上市提供依据。
尽管当前进口原研药仍然是我国抗肿瘤新药的重要来源,但我国也已具备一定的药品研发能力,我国应大力扶持和引导中国企业集中研发新药,提升国产新药的研发效率和质量;与外资企业建立联系,鼓励进口新药在国内开展试验提交上市申请;同时完善我国药品上市审批制度,探索适合于抗肿瘤新药的加速审批程序,提升恶性肿瘤防治能力,切实提升患者的用药可及性和时效性。
作者声明本文无实际或潜在的利益冲突。
| [1] |
杨之洵, 陈万青. 癌症负担预测方法学的研究进展[J]. 中国肿瘤, 2019, 28(4): 241-245. |
| [2] |
侯延武, 怀国尹, 庞秀明, 等. 国家基本药物制度与医药卫生体制改革的协同与评述[J]. 黑龙江医学, 2018, 42(7): 710-712. DOI:10.3969/j.issn.1004-5775.2018.07.034 |
| [3] |
FDA. Novel Drug Approvals for 2019[EB/OL]. (2020-01-14)[2021-01-18]. https://www.fda.gov/drugs/new-drugs-fda-cders-new-molecular-entities-and-new-therapeutic-biological-products/novel-drug-approvals-2019
|
| [4] |
李赛赛, 徐伟, 王煜昊, 等. 创新药物医保目录准入研究[J]. 卫生经济研究, 2019, 36(10): 40-43. |
| [5] |
敖翼, 濮润, 卢姗, 等. 我国新药创制的模式选择与发展思考[J]. 中国新药杂志, 2020, 29(2): 136-142. DOI:10.3969/j.issn.1003-3734.2020.02.004 |
| [6] |
聂珏荃, 李皛. 中美两国医保目录调整工作程序和决策支持体系[J]. 中国药物经济学, 2020, 15(12): 32-38. DOI:10.12010/j.issn.1673-5846.2020.12.007 |
| [7] |
郭雷, 程思奇, 李嘉敏. 2019年全球肿瘤领域原创新药盘点[J]. 肿瘤综合治疗电子杂志, 2020, 6(1): 70-79. |
| [8] |
新华社. 习近平: 在科学家座谈会上的讲话[EB/OL]. (2020-09-11)[2021-01-18]. http://www.gov.cn/xinwen/2020-09/11/content_5542862.htm
|
| [9] |
国新网. 《国家创新驱动发展战略纲要》政策解读[EB/OL]. (2016-05-24)[2021-01-18]. http://www.scio.gov.cn/34473/Document/1478594/1478594.htm
|
| [10] |
韩蕊. 药品注册在新药研发中的作用研究[J]. 商品与质量, 2020(6): 250, 273. |
| [11] |
郭宗儒. 我国创制的抗肿瘤药物泽布替尼[J]. 药学学报, 2020, 55(8): 1978-1982. |
| [12] |
牟燕, 宋奎勐, 吴敏, 等. 基于政策工具视角的我国罕见病领域政策文本分析[J]. 中国卫生政策研究, 2021, 14(1): 17-23. |
| [13] |
任晓星, 史录文. 中美欧新药上市加快审评审批政策研究[J]. 中国新药杂志, 2020, 29(9): 961-971. DOI:10.3969/j.issn.1003-3734.2020.09.001 |
| [14] |
胡善联. 多准则决策分析在卫生决策领域中的应用价值[J]. 中国卫生资源, 2020, 23(4): 325. DOI:10.3969/j.issn.1007-953X.2020.04.004 |
| [15] |
胡善联. AD创新药难进医保?多维价值评价"利刃出鞘"[N]. 医药经济报, 2021-04-08.
|
(编辑 赵晓娟)





