2. 新南威尔士大学乔治全球健康研究院 澳大利亚新南威尔士州 悉尼 2052
2. George Institute for Global Health, University of New South Wales, Sydney NSW 2052, Australia
《中国居民营养与慢性病状况报告》指出,慢性病是我国主要死因,2019年我国因慢性病导致的死亡占总死亡的88.5%。[1]共病是慢性病的常见形式,世界卫生组织将同一患者同时患有两种或多种慢性病称为共病。[2]中国慢性病前瞻性研究(China Kadoorie Biobank, CKB)显示,我国慢性病共病患病率为15.9%。[3]相对于一般疾病和单一慢性病,共病具有更加严重的健康损害和社会危害,如不良健康预后、卫生服务资源利用失衡、多重用药和高额的医疗费用等。另外,共病损害具有累积效应,多种慢性病叠加、并存和组合,不仅导致患者病情错综复杂,而且会产生额外的、过度的卫生服务利用和医疗资源消耗,导致共病患者面临多重的疾病负担和经济负担。众多研究表明,管控慢性病危险因素是预防和诊疗慢性病的关键措施。[4-6]慢性病危险因素管控,包括预防慢性病患病的危险因素和控制慢性病患者接受诊疗服务后可能发生卫生服务资源过度消耗和疾病经济负担的危险因素。基于此,本研究探究和测量共病罹患风险、服务利用和经济影响的危险因素及其作用程度,从而为有效防范共病风险与合理规范共病服务,提供个性化、有针对性的循证依据和防治策略。
1 资料与方法 1.1 资料来源资料来源于2018年江苏省慢性病患者家庭入户调查。根据地理分布和经济水平,选择6个地级市,在各地级市随机选择1个县(市、区),每个县(市、区)抽取5个乡镇(街道),每个乡镇(街道)随机选取2个行政村(居委会),通过自行设计的调查问卷对当地慢性病患者进行家庭入户调查。本研究将被访者具有慢性病就诊经历或慢性病用药作为纳入标准,共计调查4 598名慢性病患者,其中单一慢性病患者3 053名,慢性病共病患者1 545名。
调查问卷内容包括三部分:一是被调查者的人口学与社会经济学特征,包括性别、年龄、户籍、教育程度、婚姻状况、就业状况、医保类型、收入支出水平、家庭结构等;二是健康状况和行为,包括是否有医疗机构确诊的慢性病及其名称、数量和种类,吸烟和饮酒史,每周锻炼频次;三是卫生服务利用情况,包括与慢性病相关的两周门诊次数和年住院天数。
1.2 主要观测变量(1) 门诊次数:询问慢性病确诊患者或慢性病服药者在调查前两周因慢性病到医疗机构进行门诊的次数;
(2) 住院床日:询问慢性病确诊患者或慢性病服药者在调查前一年内因慢性病在医疗机构住院的天数;
(3) 是否发生灾难性卫生支出:根据世界银行界定的阈值,将调查前一年慢性病自付医疗支出占家庭总支出比例超过25%作为发生灾难性卫生支出的标准[7];
(4) 户籍:分为“城市”和“农村”;
(5) 教育程度:分为“没上过学”“小学”“初中”“高中”“技校”“中专”“大专”“本科”;
(6) 婚姻状况:分为“未婚”“已婚”“丧偶”“离婚”;
(7) 就业状况:包括“在业”“离退休”“失业”“无业”;
(8) 基本医疗保险:由于本研究于2018年进行现场调查,在此时点包括城镇职工基本医疗保险、城镇居民基本医疗保险、城乡居民基本医疗保险、新型农村合作医疗;
(9) 收入水平:对收入水平进行五等分,形成“最低收入组”“中低收入组”“中等收入组”“中高收入组”“最高收入组”;
(10) 锻炼强度:将每周不锻炼或锻炼次数小于等于2次定义为“低度或不锻炼”,将每周锻炼次数3~5次定义为“中度锻炼”,将每周锻炼次数6次及以上定义为“高度锻炼”。
1.3 分析方法调查对象基本情况采用描述性分析,计算家庭等值人口以衡量家庭人口权重,采用Logistic回归分析慢性病共病罹患风险因素和共病患者发生灾难性卫生支出的危险因素,采用负二项回归分析共病患者门诊次数和住院床日的影响因素。本研究通过Epidata 3.1软件进行数据双录入,运用SPSS 24.0软件进行数据分析。
(1) 家庭等值人口(Adult Equivalent, AE)
鉴于不同家庭的年龄结构不同,为了合理测量和评价家庭实际的可支付能力(ability to pay, ATP),本研究采用世界银行推荐公式计算家庭等值人口[7],测量基于家庭等值人口的人均可支付能力。
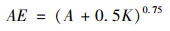
|
其中,A为家庭成年人数,K为家庭儿童(14岁以下)人数。
(2) Logistic回归(logistic regression)
鉴于健康人群与慢性病共病人群存在较大差异,为了准确甄别影响共病罹患的危险因素,本研究将单一慢性病患者(赋值=0)和慢性病共病患者(赋值=1)作为因变量,将研究对象的自然属性特征和经济社会属性特征,如年龄、性别、户籍、教育程度、婚姻状况、就业状况、收入水平、基本医疗保险险种、参加商业医疗保险、是否贫困户等作为自变量,以比值比(odds ratio, OR)为分析指标,通过Logistic回归模型分析罹患共病风险的因素。具体表达式如下:
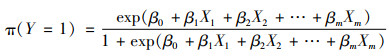
|
或
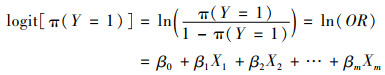
|
另外,为了探究共病人群发生灾难性卫生支出的危险因素,本研究将发生灾难性卫生支出的共病患者(赋值=1)和未发生灾难性卫生支出的共病患者(赋值=0)作为因变量,以前述自然属性特征和经济社会属性特征作为自变量,通过Logistic回归分析影响共病患者发生灾难性卫生支出的危险因素。
(3) 负二项回归(negative binomial regression)
本研究以共病患者为对象分析影响共病服务利用(门诊次数、住院床日)的因素。由于门诊次数、住院床日是计数变量,通常偏离正态性,一般线性回归模型不能适用。另外,计数变量不仅数据波动性很大,而且存在因变量观察值等于0的情况(例如共病患者没有进行门诊或住院),采用对数线性模型也不适用。因此,考虑门诊次数和住院床日是任意非负整数,服从泊松分布或负二项分布。
由于门诊次数和住院床日的数据类型往往具有过离散特征,如果使用泊松回归模型,可能会低估参数的标准误,高估其显著水平,导致分析结果不合理。为了消除此种不利影响,利用负二项回归模型代替泊松回归模型进行估计,既能适用计数型资料,又能适应过离散问题[8],具体分析公式如下:
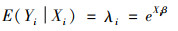
|
或
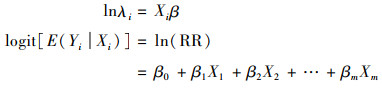
|
负二项回归模型实际上是扩展了线性模型的框架,允许非正态响应变量的分析,其中响应变量Yi不局限于正态性。[9]鉴于本研究采用的门诊次数、住院床日是计数变量,且卫生服务利用数据类型一般存在聚集性,因此,本研究通过负二项回归分析方法,仍然采用前述自变量,当其他自变量保持不变时,自变量Xm改变1个单位,取值由Xm变为Xm+1,以率比值(rate ratio, RR)指标分析某自变量的单位变化对于共病患者门诊次数或住院床日的影响程度。
1.4 质量控制质量控制贯穿现场调查及数据处理全过程。在研究设计阶段,通过文献复习、专家研讨和预调查形式,保证调查设计的科学性、有效性与可行性;在调查正式开始之前,对调查员统一培训,明确调查的目的、意义和原则,掌握调查指标的含义和填写要求,以及调查过程中可能出现问题的解决方法;在现场调查过程中,调查员全面检查填写内容,如有疑问、错误或遗漏则重新核实、改正或填补;在数据处理过程中,采取双人双录入,确保调查工作质量和数据完整准确。
2 结果 2.1 调查对象基本情况本研究共纳入4 598名慢性病患者,其中,单一慢性病患者3 053名(66.40%),慢性病共病患者1 545名(33.60%);50.20%为城市居民,49.80%为农村居民;男性(52.46%)略多于女性(47.54%);调查对象以50岁以上患者居多(71.66%);参加城镇职工基本医疗保险、城镇居民基本医疗保险、新型农村合作医疗(新农合)、城乡居民基本医疗保险和其它基本医疗保险的占比分别为41.24%、15.07%、5.35%、36.41%、0.13%,1.81%的被调查者没有参加基本医疗保险;调查对象中有2.61%患者为贫困户。
2.2 影响慢性病共病罹患风险的因素分析以“是否罹患共病”为因变量,1为慢性病共病患者,0为单一慢性病患者。根据调查对象一般性特征,自变量包括户籍、性别、年龄、教育程度、婚姻状况、就业状况、基本医疗保险险种、是否参加商业医疗保险、收入水平、是否为贫困户、锻炼强度。分析结果发现,城乡居民罹患共病存在显著差异,农村居民更易发生共病;年龄是罹患共病的正相关因素,随着年龄增长,罹患共病风险缓慢增长;罹患共病的风险随着被调查者受教育水平的提升而下降;已婚、丧偶和离婚人群相对于未婚人群罹患共病的风险更高;无业、离退休人群罹患共病的风险更高;在基本医疗保险方面,新型农村合作医疗和城乡基本医疗保险参保人群罹患共病的风险低;随着收入水平增加,罹患共病的趋势在增加,但仅中高收入组具有统计学差异;锻炼频度越高者,其罹患共病的风险更高。另外,性别、是否参加商业医疗保险和是否为贫困户,对于是否发生共病的影响不显著(表 1)。
| 表 1 慢性病共病影响因素Logistic回归结果 |
以慢性病共病患者为对象,分析共病患者门诊次数、住院床日和发生灾难性卫生支出风险的影响因素(表 2)。采用负二项回归分析方法,利用率比(RR)指标,分析影响共病患者门诊次数和住院床日的因素;采用Logistic回归分析方法,利用比值比(OR)指标,分析影响共病患者是否发生灾难性卫生支出的因素。随着共病患者罹患慢性病数量的增加,其门诊次数、住院床日和发生灾难性卫生支出的风险均增加:共病患者每增加1种慢性病,门诊次数、住院床日和发生灾难性卫生支出的风险分别增加1.44倍、1.73倍和1.34倍。
| 表 2 慢性病共病患者卫生服务利用与灾难性卫生支出影响因素分析 |
就共病患者门诊次数而言,除罹患慢性病数量外,仅无业是导致门诊次数增加的危险因素。就共病患者住院床日而言,除慢性病数量外,随年龄增长,患者住院床日有缓慢的增加;教育程度越高者,共病住院服务利用越少;未婚的共病患者,相对于已婚、丧偶或离婚状态的共病患者,有更长的住院床日;无业是导致住院床日增加的危险因素;参加城镇居民基本医疗保险和新农合的共病患者,住院床日较短;随着收入水平提升,共病患者住院床日变长;非贫困户、中等强度的锻炼,住院床日较短。就共病患者发生灾难性卫生支出的风险而言,除慢性病数量外,失业、无业是导致灾难性卫生支出发生风险增加的危险因素,收入是防止灾难性卫生支出发生的保护因素。
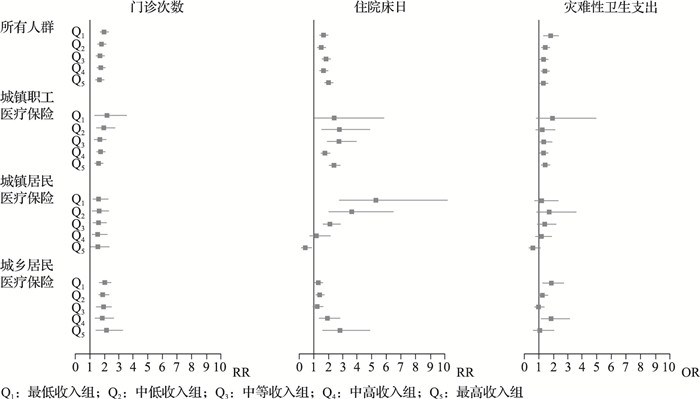
2.4 慢性病共病数量与门诊次数、住院床日和灾难性卫生支出的亚组分析进一步分析参加不同基本医疗保险及其不同收入水平的情况下,患者共病数量与卫生服务利用及发生灾难性卫生支出风险的关系。鉴于参加新农合的不同收入组的患者样本量偏少,因此不纳入亚组分析。本研究分别分析了不同收入水平下所有参加基本医疗保险的共病患者、城镇职工基本医疗保险的共病患者、城镇居民基本医疗保险的共病患者、城乡居民基本医疗保险的共病患者罹患慢性病数量与门诊次数、住院床日和是否发生灾难性卫生支出的关系(图 1)。结果表明,共病数量与卫生服务利用及灾难性卫生支出基本呈递增关系,即共病数量增加1,则门诊次数、住院床日和发生灾难性卫生支出可能性的增长倍数超过1。其中,需要特别关注城镇居民基本医疗保险不同收入组患者的共病数量与住院床日的关系:当罹患慢性病数量增加时,低收入患者的住院床日呈递增性增长(RR>1),而高收入患者的住院床日增长趋势呈递减状态(RR < 1),表明高收入患者住院服务利用呈现饱和状态,而低收入患者住院服务利用相对缺乏,更需要额外的住院服务。
|
图 1 慢性病共病数量与门诊次数、住院床日和发生灾难性卫生支出的关系 |
本研究分析慢性病共病及其卫生服务利用和灾难性卫生支出的关系。分析表明,随着患者共病数量增加,其门诊次数、住院床日和发生灾难性卫生支出的风险呈递增态势。该发现与国内外现有研究基本一致:印度尼西亚对50岁以上居民调查显示,患有三种及以上慢性病的当地居民,其四周就诊率是非慢性病居民4.25倍,而年住院次数是其3.68倍,灾难性卫生支出风险是其1.69倍[10];一项关于中国心血管代谢类疾病的社区老人的调查显示,分别患有1种、2种和3种心血管代谢类疾病的老人,其门诊次数分别是非心血管代谢类疾病老人的1.36倍、1.70倍和2.04倍,患有2种和3种心血管代谢类疾病的老人,其发生灾难性卫生支出风险是非心血管代谢类疾病老人的1.43倍和1.98倍[11]。进一步对参加不同险种及其不同收入组别人群进行亚组分析,共病患者罹患慢性病数量增加将促使卫生服务利用水平和灾难性卫生支出的发生水平更加快速增长。因此,共病患者慢性病累加,相对于单纯慢性病的简单加和,将产生更多的、额外的卫生资源消耗和更严重的经济风险。因此,关注慢性病共病重点人群,尤其是影响共病罹患风险、卫生服务利用和发生灾难性卫生支出的危险因素,通过强化风险前置的意识和措施,对于控制共病流行、有效节约和合理规划卫生服务资源使用,以及针对性地降低发生灾难性卫生支出的风险,具有科学的指导意义。
3.2 慢性病共病与社会风险因素密切相关本研究发现,共病罹患风险程度,以及共病患者的卫生服务利用水平和灾难性卫生支出发生风险,与患者的经济社会属性密切相关。世界银行指出,慢性病风险因素包括两个方面:自然风险因素和社会风险因素。[7]分析结果表明,性别、年龄等自然风险因素,对于共病的患病风险、卫生服务利用和是否发生灾难性卫生支出,作用不显著,或者作用程度极小。然而,一些社会风险因素对于共病发生及其卫生服务利用结果影响显著。农村地区、无业、低水平教育是罹患共病的危险因素,无业、失业、低收入是导致共病患者发生灾难性卫生支出的危险因素。《中国防治慢性病中长期规划(2017—2025年)》专门强调慢性病在社区早期发现的重要意义,可以为此提供实践支持:除了加强和规范健康体检,可以根据本研究分析思路明确社区共病及其利用的潜在危险因素,通过早发现、早诊断和早治疗,不仅可以降低社区人群的疾病风险,而且可以减少患病人群的疾病经济风险。另外,本研究在一定程度上支持英国著名的“白厅研究(Whitehall study)”观点:社会经济地位越高,人们的健康水平越高,反之则越低。[12]当然,与该研究不同的是,本研究发现随着收入水平提高,共病罹患风险在提升。这也说明不同的社会体制和不同经济发展阶段,可能会影响上述研究的既定结论。但是,前期研究和本研究均提示,降低共病罹患风险、防范灾难性卫生支出风险需要有的放矢,特别是促进当地经济与社会发展,是控制共病的根本性策略。
3.3 重视居民基本医疗保险对共病住院服务需要的保障作用研究结果显示,作为居民基本医疗保险,相对于城乡居民基本医疗保险,城镇居民基本医疗保险和新农合参保人群住院床日较短,说明这两种保险有可能抑制了共病患者的住院服务需要。相对于单一慢性病患者,共病患者的病情更加复杂,住院服务需求更高,医疗费用负担也更重。城镇居民基本医疗保险和新农合主要覆盖非从业居民和农民,但是报销保障力度相对有限。2016年,我国政府通过整合城镇居民基本医疗保险和新农合,建立统一的城乡居民基本医疗保险制度。在医保待遇方面,通过实行“六统一”的政策整合[13],提升了住院费用报销比例和提高门诊保障水平,对于更好地满足共病患者的住院需求,发挥了重要作用。随着医保整合工作的推进,我国城乡非从业居民将普遍参加城乡居民基本医疗保险,在完善医保费用覆盖的基础上,应当针对不同类型居民在性别、疾病类别、教育程度、收入能力、就业状况等方面的差别,形成差异化的医保报销政策,充分发挥基本医疗保险的经济杠杆作用,可以合理调节共病患者服务利用,降低灾难性卫生支出发生风险。
3.4 关注社区慢性病共病的高危人群,形成个性化共病防治策略共病患者具有一体多病、多病关联的特点,是多种慢性病的复杂组合,采取传统的社区慢性病防治策略,可能会出现管理效能低下、预治措施冲突等问题。因此,制定和实施科学合理的社区防治策略,针对共病高危人群,形成相应的防治方法和方案,可以有效提升社区工作效率和共病防治效果。
实施个性化干预是中央与地方政府均力主推行的策略,各地区也在尝试各具特色的个性化干预举措。共病作为若干慢性病的组合形式,对于个性化策略设计更具挑战。本研究分析了影响共病罹患风险、卫生服务利用和发生灾难性卫生支出风险的因素。随着卫生信息化建设、健康档案和家庭医生制度在基层建设和普及,社区可以充分利用信息化手段采集和标注居民的健康相关和经济社会相关特征,从而梳理和确定影响社区居民罹患共病、卫生服务利用和发生灾难性卫生支出等方面的危险因素。从本研究的思路方法和分析结果出发,可以定位和随访社区高危人群,将关口前移,实施源头管控,从而预防共病发生发展,合理规划卫生服务资源有效利用和针对性使用,最大程度降低共病患者发生灾难性卫生支出的风险。更为重要的是,共病患者虽然疾病类型不同、共病组合不同,但是可能是由相同危险因素造成的。换言之,社区不同类别的共病患者,是由固定的危险因素集造成的,例如本研究发现户籍、收入、教育水平、就业状况等,是影响共病罹患的易感因素或影响共病卫生服务利用和造成灾难性卫生支出的危险因素。因此,在社区共病防治措施方面,基层医疗机构通过循证或实证挖掘共病及其服务利用的危险因素集,针对可控危险因素采取社区一级预防的方式避免或减少致病因子暴露,对于不可控因素尽早定位社区重点人群和高危人群,采取二级或三级预防措施减缓共病发生发展和疾病损害影响。因此,社区共病防治策略不能仅以特定疾病为单位进行预防、治疗和控制,更要关注引发共病的可控危险因素和经济社会因素,通过采取对应性的防治策略和管理措施,可以在很大程度上提升社区共病防治效率和效果。
作者声明本文无实际或潜在的利益冲突。
| [1] |
国家卫生健康委. 中国居民营养与慢性病状况报告(2020年)[R]. 2020.
|
| [2] |
World Health Organization. The World Health Report 2008: primary health care-now more than ever[R]. New York, 2008.
|
| [3] |
Zou S, Wang Z, Bhura M, et al. Prevalence and associated socioeconomic factors of multimorbidity in 10 regions of China: an analysis of 0.5 million adults[J]. Journal of Public Health, 2020(9836). |
| [4] |
姜雯, 张蓝超, 李伟豪, 等. 中国居民2012-2017年慢性病防治素养水平变化趋势及其影响因素年龄-时期-队列分析[J]. 中国公共卫生, 2021, 37(6): 915-920. |
| [5] |
刘国峰, 简伟研. 城镇化与慢性病的关系研究现状及方法探究[J]. 中国卫生政策研究, 2016, 9(10): 31-37. |
| [6] |
MirandaJ J, KinraS, CasasJ P, 等. 中低收入国家的慢性病: 背景、决定因素与卫生政策[J]. 中国卫生政策研究, 2013, 6(10): 12-20. |
| [7] |
O O'Donnell, A Wagstaff. Analyzing health equity using household survey data: a guide to techniques and their implementation[R]. Washington, DC: World Bank, 2008.
|
| [8] |
张晓东, 张浩, 陈亮, 等. 基于负二项回归的水上交通事故分析与预测[J]. 上海海事大学学报, 2013, 34(2): 8-12. |
| [9] |
Cameron A C, Trivedi P K. Regression analysis of count data[M]. 2nd. Cambridge University Press, 2014.
|
| [10] |
Marthias T, Anindya K, Ng N, et al. Impact of non-communicable disease multimorbidity on health service use, catastrophic health expenditure and productivity loss in Indonesia: a population-based panel data analysis study[J]. BMJ Open, 2021, 11(2): e041870. DOI:10.1136/bmjopen-2020-041870 |
| [11] |
Gao K, Li B L, Yang L, et al. Cardiometabolic diseases, frailty, and healthcare utilization and expenditure in community-dwelling Chinese older adults[J]. Sci Rep, 2021, 11(1): 7776. DOI:10.1038/s41598-021-87444-z |
| [12] |
Dugravot A, Fayosse A, Dumurgier J, et al. Social inequalities in multimorbidity, frailty, disability, and transitions to mortality: a 24-year follow-up of the Whitehall II cohort study[J]. Lancet Public Health, 2020, 5(1): e42-e50. DOI:10.1016/S2468-2667(19)30226-9 |
| [13] |
国务院办公厅. 《国务院关于整合城乡居民基本医疗保险制度的意见》[EB/OL]. (2016-01-12)[2021-09-01]. http://www.gov.cn/zhengce/content/2016-01/12/content_10582.htm
|
(编辑 薛云)





