2. 北京大学医学部卫生政策与技术评估中心 北京 100083;
3. 北京医药卫生经济研究会 北京 100069
2. The Center of Health Policy and Technology Evaluation, Peking University Health Science Center, Beijing 100083, China;
3. Beijing Medical and Health Economic Research Association, Beijing 100069, China
经济性评价是指运用经济学理论对医疗技术的经济成本和健康产出进行比较,近年来已成为我国医保目录评审中的重要参考依据。[1]成本—效用分析是最常用的经济性评价方法,该方法以质量调整生命年(Quality-Adjusted Life Years,QALYs)代表效用作为健康产出指标,通过计算平均每额外获得一单位QALY的增量成本即增量成本—效果比(Incremental Cost-effectiveness Ratio,ICER),并与支付阈值相比来判断干预方案的经济性。其中,支付阈值代表平均每多获得一单位效用的货币价值,反映了社会的支付意愿,在我国一般为人均国内生产总值(Gross domestic product,GDP)的1~3倍。[1]许多价格较高的独家产品基于经济学评价,并通过价格谈判,已被纳入医保报销范围,有效减轻了患者负担。
罕见病是一类患病率极低的疾病。[2-6]专门治疗罕见病的药品,由于供给和需求都很少,难以引起人们足够重视,被形象地称为“孤儿药”。由于目标人群少,孤儿药的成本难以大规模分摊,因此价格很高。同时由于市场空间狭小,即使原研药已过专利期,也少有仿制,因此难以通过竞争降价。高价格使得很多孤儿药难以满足1~3倍人均GDP的支付阈值,难以被纳入医保目录。以国家卫生健康委员会公布的《第一批罕见病目录》中的121种罕见病为例[7],本研究通过梳理相关政策、数据统计核对并排除有非罕见病适应症的药物[8, 9],结果发现截至2021年6月我国共计有42种孤儿药上市,其中20种孤儿药被纳入医保目录,对应着10种罕见病,如血友病、帕金森、多发性硬化等;仍有22种孤儿药未被纳入医保目录,对应着14种罕见病。
在主要用药未被纳入医保报销的情况下,大部分罕见病患者无力承担最有效的或规范的治疗方案,严重影响自身健康,疾病负担沉重。但部分孤儿药能大幅改善初始QALYs几乎为零的重症罕见病患者的健康,带来10个甚至更多的QALYs[10-12],使患者的疾病状态得到缓解并趋于稳定,能够正常参与各种社会活动甚至正常工作,给家庭和社会带来巨大的经济价值。相比于能够挽救患者生存时间较短的许多抗肿瘤创新药,孤儿药在改善罕见病患者生命质量方面具有特殊的价值。从社会价值和创新价值来看,有必要探究这些孤儿药是否值得被纳入医保报销。大部分具备完善医保制度的国家和地区都积极探索将这些特效的孤儿药纳入保障范围、提高其可及性。[13-17]
已有的研究多从孤儿药本身的特性出发,从多个角度拓宽孤儿药的评价维度,如Mark Nuijten认为孤儿药的社会价值应包括创新价值,因此应给孤儿药设定较高的价格[18];李立红和胡善联则从公平角度分析罕见病患者具有公平获取资源配置、平等的机会改善自身健康的权利,因此医保应保障孤儿药[13, 19],张伟涛从基本医疗保障权角度分析应满足所有疾病患者包括罕见病患者的基本医疗需求[20]。还有学者针对经济性评价探讨如何调整评价指标:Everton Nunes da Silva认为应将疾病严重程度、有无可替代的方案、治疗费用占家庭预算等都考虑进孤儿药的效用中[21];Elena Nicod认为社会倾向于保障特殊群体如罕见病患者的健康,经济学评价应该综合考虑疾病严重程度、疾病状态等价值,为孤儿药设定更高的支付阈值[22]。可以看出,目前学者虽然对拓宽评价标准进行了探讨,但均为定性探讨,难以形成定量的调整方法,且均未与经济学评价的理论有效结合。
支付阈值作为反映社会支付意愿的指标,其制定的准确性与合理性对科学评估孤儿药的价值至关重要。因此,本研究通过深入分析传统的经济性评价支付阈值设定的理论基础,从健康效用理论角度探讨孤儿药支付阈值制定的不足,讨论如何基于按效用付费调整传统的孤儿药支付阈值,并通过检索文献和总结国际经验验证理论,以更加科学的方法评估孤儿药的经济性。
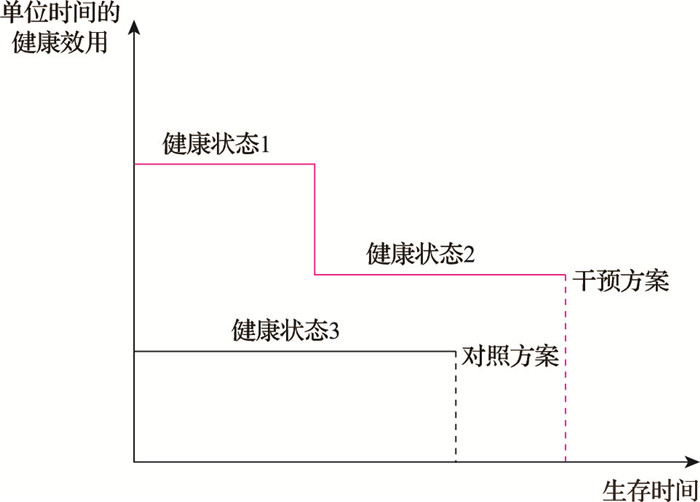
2 孤儿药支付阈值制定的理论难题 2.1 常规支付阈值设定的理念支付阈值的设定与成本—效用分析的健康产出指标、支付理念有关。从评估理念出发,成本—效用分析以QALYs代表健康效用作为产出指标,等于单位时间健康效用和生存时间的乘积(图 1),其中干预方案的QALYs等于患者在健康状态1对应的QALYs和在健康状态2对应的QALYs的加和,而患者在健康状态1、健康状态2对应的QALYs分别等于相应的单位时间健康效用乘以生存时间,同理对照方案给患者带来的QALYs等于健康状态3对应的单位时间的健康效用乘以生存时间,增量QALYs即等于红线下的面积减去黑线下的面积。可以看出,QALYs作为产出指标既能反映单位时间健康效用的改善、也能反映出患者生存时间的延长。该方法默认了每单位QALY对应的健康效用相等,且每多获得一单位QALY对应的边际健康效用也相等。由此,基于按效用付费的支付理念,平均每单位增量QALY的支付阈值应相同且恒定,因此在实际评价过程中,不论增量QALYs的大小,对应的支付阈值相同且恒定。
|
 图 1 QALYs与增量QALYs的计算方法
图 1 QALYs与增量QALYs的计算方法
|
当QALYs可以准确代表效用时,支付阈值可准确反映干预方案的经济性。但从测量方式来看,以QALYs代表效用存在一定偏差。这是因为QALYs等于患者在某种健康状态下的生存时间乘以这段时间内的生命质量[23],其中生命质量可通过直接测量法或间接测量法获得,直接测量法是利用标准博弈法(Standard Gamble,SG)、时间权衡法(Time Trade-Off,TTO)等方法测得,直接代表受访者在受访时间点处于某个健康状态的效用值;间接测量法则是让受访者根据受访时间点的健康状态填写健康效用测量量表的健康状态描述系统,再代入到健康效用积分体系中,间接测得在某个时间点某个健康状态的效用。无论是直接测量法还是间接测量法,测的都是患者在某个时间点即单位时间截面的效用值,与患者处于某个健康状态的时间长度无关。[13, 24]如果以该效用值代表患者在某个健康状态期间的效用值,无法反映时间跨度上的健康大幅改善对健康效用的影响。[13, 25]在考虑时间跨度时,如果只是将患者在该健康状态下的生存时长直接乘以恒定的单位时间截面效用,也无法反映患者健康效用的实际变化。
在QALYs代表效用存在偏差的情况下,仍以每获得一单位QALY对应的边际健康效用相等来制定支付阈值,会给评估药物带来一定偏差。对于仅能轻微改善重症患者健康的一般新药,QALYs和健康效用之间的偏差较小,可忽略不计,但对于能大幅改善罕见病患者健康的孤儿药而言,偏差较大,需要调整QALYs以准确反映孤儿药带来的效用,也可调整平均每单位增量QALY的支付阈值。综上,常规支付阈值的设定在理念上存在一定不足,无法准确评估孤儿药的经济性,如何根据患者的健康改善程度调整孤儿药的支付阈值是当前所面临的难题。
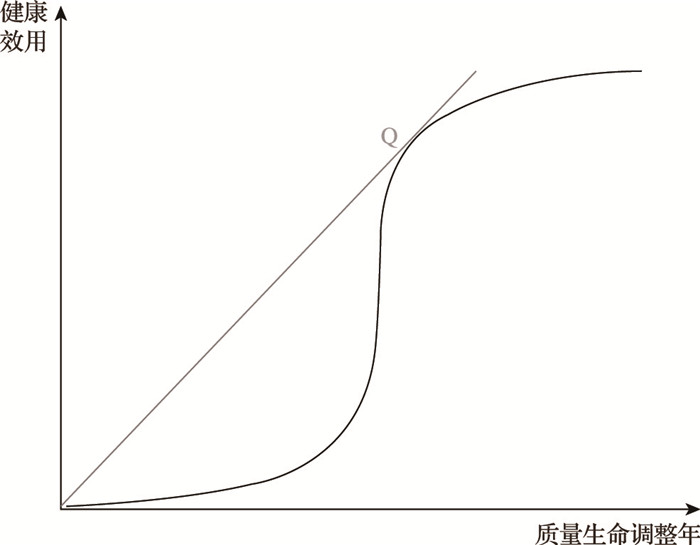
3 孤儿药支付阈值调整的理论方案 3.1 孤儿药支付阈值调整的理论基础基于传统的经济性评价方法,无论其罕见病患者的QALYs改善多少,平均每单位增量QALY对应的支付阈值均相同,但研究表明对于初始QALYs几乎为零的重症罕见病患者,QALYs的轻微改善与大幅变化带来的边际健康效用不同,可能呈现边际健康效用递增的现象。[26, 27]从理论上来看,随着单位时间内生命质量的提高、相同生命质量下生存时间的延长,罕见病患者的健康大幅改善,使得生存状态逐渐确定,患者的焦虑减轻,因此边际单位时间效用递增,直到罕见病患者能够正常工作和参与各种社会活动,之后罕见病患者的满足感逐渐减弱,边际单位时间效用逐渐减少,即边际单位时间效用呈现先递增后递减的趋势。罕见病患者的健康状态可能在边际单位时间效用递增时转换,也可能在边际单位时间效用递减时转换,但罕见病患者某个健康状态对应的单位时间效用并不是一个恒定值,也不随时间线性变化,因此以QALYs代表健康效用存在偏差。同理边际效用也呈现先递增后递减的趋势,即随着罕见病患者QALYs的增加,患者的健康效用逐渐增加且边际健康效用递增,直到罕见病患者能够正常参与各种社会活动,边际健康效用达到最大,随后边际健康效用递减。综上,对于初始QALYs几乎为零的重症罕见病患者,如果孤儿药能大幅改善罕见病患者的健康,随着QALYs的递增,罕见病患者的边际健康效用先递增后递减,QALYs与健康效用应呈现S型。以上理论也得到了实证研究的支持,研究发现对于重症患者,随着健康状况的逐步改善,即随着QALYs的增加,边际健康效用递增,直到患者能正常工作和参与各种社会活动,当QALYs达到9.1年时,边际效用达到最大,随着QALYs的继续增加,边际健康效用开始递减,总体来看QALYs与健康效用呈现S型变化(图 2)。[26]当然,在不同国家由于经济、文化等存在差异,S型曲线的拐点和曲率可能会有所不同。
|
图 2 QALYs与健康效用的关系 |
基于按效用付费的原则,支付阈值是指平均每单位增量效用的支付意愿,平均每单位增量QALY对应的健康效用不同,支付阈值也不同。随着增量QALYs从零开始增加,单位增量QALY对应的健康效用逐渐增加,孤儿药的支付阈值也逐渐增加,直到边际健康效用与平均每单位增量QALY对应的健康效用相等时,平均每单位增量QALY对应的健康效用达到最大,孤儿药平均每单位增量QALY对应的支付阈值达到最大,随后递减。对应到图 2,当曲线上一点与原点的连线与曲线相切时,即图中Q点,平均每单位增量QALY对应的健康效用达到最大,孤儿药平均每单位增量QALY对应的支付阈值达到最大。综上,对于可大幅改善重症罕见病患者QALYs的孤儿药,平均每单位QALY对应的健康效用高于只能轻微改善重症患者健康的一般药品,孤儿药的支付阈值也应高于一般药品,因此应根据罕见病患者QALYs的改善程度调孤儿药支付阈值。
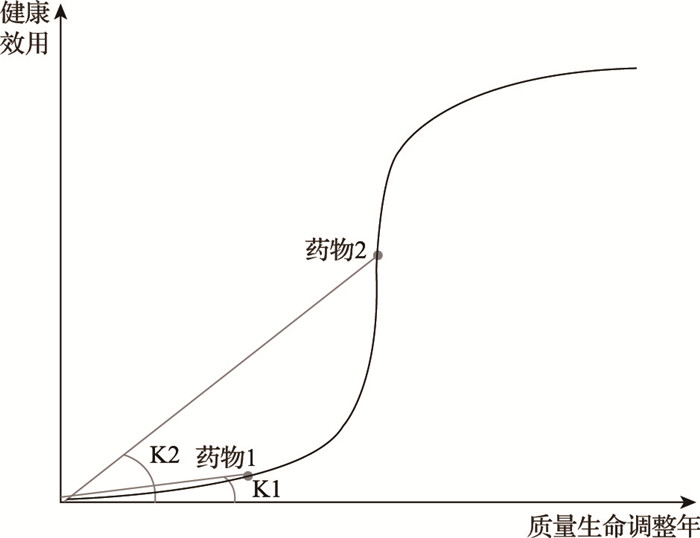
3.2 孤儿药支付阈值调整的方案基于上述理论分析,QALYs与健康效用呈现S型变化,应根据QALYs的改善程度探索孤儿药支付阈值调整的具体方案。根据前述的理论,对于治疗效果不同的药物,其平均每单位增量QALY的支付阈值比等于增量效用比。将仅能轻微改善患者健康的一般新药统称为药物1,将能大幅改善罕见病患者健康的孤儿药统称为药物2,药物1和药物2的支付阈值比等于平均每单位增量QALY的增量效用比。当药物1和药物2的增量QALYs已知时,可求得平均每单位增量QALYs对应的效用比。对应图 3,当以K1、K2表示药物1、药物2平均每单位增量QALY的增量效用,以T1、T2代表药物1、药物2平均每单位增量QALY的支付阈值,那T2、T1的比值就等于K2、K1的比值。当药物2和药物1的增量QALYs已知时,可根据S型曲线求得K2、K1,T1可取1~3倍人均GDP,此时可求得T2(公式2)。综上,对于可大幅改善重症罕见病患者QALYs的孤儿药,在调整支付阈值时,可根据支付阈值比等于增量效用比的关系,求得孤儿药的支付阈值,罕见病患者QALYs的改善程度越大,支付阈值调整的幅度往往越大。
|
 图 3 QALYs改善程度不同的药物对应的斜率
图 3 QALYs改善程度不同的药物对应的斜率
|
在实际评价过程中,相关部门可直接根据罕见病患者的QALYs改善程度调整孤儿药的支付阈值,即对于可带来不同增量QALYs的孤儿药,其支付阈值不同,此种方法可准确评价孤儿药的价值,但同时导致的支付阈值标准过多可能给医保评审造成一定的负担。英国国家卫生和临床优化研究院(National Institute for Health and Clinical Excellence,NICE)考虑到QALYs的大幅度提高带来的特殊价值,于2013年针对患病率小于0.02‰的罕见病实施高特技术评估(Highly Specialized Technology Evaluation,HSTE),将孤儿药给罕见病患者带来的QALYs分为≤10、11~29、≥30三个等级,并给QALYs分别赋予1、1~3、3的权重,即是阈值的权重,同时设定阈值为10万英镑。[28, 29]当NICE为某个孤儿药设定的权重是3时,阈值为10万英镑的3倍即30万英镑。在实际操作过程中,我国可借鉴英国经验先探索设置增量QALYs区间及对应的权重,若孤儿药符合对应的增量QALYs区间,可将传统的支付阈值乘以权重计算得调整后的支付阈值,如假设为增量QALYs处于5~15的孤儿药设置阈值权重为2,当孤儿药带来的增量QALYs为10时,支付阈值应调整为传统支付阈值(1~3倍GDP)的2倍,调整后的支付阈值为2~6倍GDP,此种方法虽然缺乏一定的精确度,但有利于提高医保评审的效率。还有的国家直接调整支付阈值,但不会根据健康改善程度设定权重,如美国直接将孤儿药的支付阈值从一般药物的5万美元增加到50万美元[30],此种方法更为简便,但缺乏精确度。我国可先探索不根据健康改善程度直接调整支付阈值,后续随着数据管理水平以及医保评审效率的提高,再设置增量QALYs区间及对应的权重,或针对不同增量QALYs的孤儿药设置对应的支付阈值,以体现那些能够大幅改善重症罕见病患者健康的孤儿药的价值,从而将具有经济性的孤儿药纳入医保目录、减轻重症罕见病患者的负担。
4 结论及启示综上,现有的经济性评价低估了那些能够大幅改善重症罕见病患者健康的孤儿药的价值。若孤儿药能较大幅度提高重症罕见病患者的QALYs,应结合健康改善程度提高平均每单位增量QALY的支付阈值,以促进治疗效果显著、疗效确切的孤儿药进入医保目录,减轻罕见病患者负担。
此外,孤儿药支付阈值的调整还会影响医保基金的支出。为控制医保基金支出,相关部门可先探索纳入部分孤儿药,后续逐步扩大保障范围。同时,随着孤儿药被纳入医保目录,会减轻罕见病患者的经济负担,使得无力承担费用而放弃治疗的罕见病患者继续治疗,市场分摊空间得以扩大,可通过价格谈判进一步降低药品价格并形成正向循环,从而可避免对医保基金造成较大影响。
作者声明本文无实际或潜在的利益冲突。
| [1] |
刘国恩. 中国药物经济学评价指南2020[M]. 北京: 中国市场出版社, 2020.
|
| [2] |
One Hundred Seventh Congress of the United States of America. Rare Diseases Act of 2002: H.R. 4013[EB/OL]. (2002-01-23)[2021-10-12]. https://www.govinfo.gov/content/pkg/BILLS-107hr4013enr/pdf/BILLS-107hr4013enr.pdf
|
| [3] |
Council of the European Union & European Parliament. Regulation (EC) No 141/2000 of the EuropeanParliament and of the Council of 16 December 1999 on Orphan Medicinal Products[EB/OL]. (1999-12-16)[2021-10-12]. https://publications.europa.eu/en/publication-detail/-/publication/445bbed6-7603-4f78-9c4a-1bae3b60465c
|
| [4] |
Ministry of Health Labour and Welfare of Japan. Overview of Orphan Drug/Medical Device DesignationSystem[EB/OL]. (2009-01-01)[2021-10-12]. https://www.mhlw.go.jp/english/policy/health-medical/pharmaceuticals/orphan_drug.html
|
| [5] |
中国台湾地区卫生福利部. Introduction and current situation of TAIWAN Rare Diseases Regulation[EB/OL]. [2021-10-12]. http://www.mohw.gov.tw
|
| [6] |
葛琳, 魏翠洁, 史录文, 等. 中国罕见病用药现状研究[J]. 北京医学, 2018, 40(5): 432-434. |
| [7] |
国家卫生健康委员会. 关于公布第一批罕见病目录的通知(国卫医发[2018] 10号)[EB/OL]. (2018-05-11)[2021-10-12]. http://www.gov.cn/gongbao/content/2018/content_5338244.htm
|
| [8] |
黄如方, 邵文斌. 中国罕见病医疗保障城市报告2020[R]. 北京: 蔻德罕见病中心, 2020.
|
| [9] |
佛山市医疗保障局. 关于印发《佛山市罕见病医疗救助药品、治疗性食品及医疗机构目录(2020版)》的通知[EB/OL]. (2020-05-29)[2021-10-12]. http://www.foshan.gov.cn/gzjg/fsylbzj/zwdt/tzgg/content/post_4363535.html
|
| [10] |
Kanters T A, Hoogenboom-Plug I M, Lken R V, et al. Cost-effectiveness of enzyme replacement therapy with alglucosidase alfa in classic-infantile patients with Pompe disease[J]. Orphanet Journal of Rare Diseases, 2014, 9(1): 75. DOI:10.1186/1750-1172-9-75 |
| [11] |
National Institute for Health and Care Excellence. Burosumab for treating X-linked hypophosphataemia in children and young people[EB/OL]. (2018-10-10)[2021-10-12]. https://www.nice.org.uk/guidance/hst8/chapter/4-Consideration-of-the-evidence
|
| [12] |
National Institute for Health and Care Excellence. Elosulfase alfa for treating mucopolysaccharidosis type IVa[EB/OL]. (2018-10-10)[2021-10-12]. https://www.nice.org.uk/guidance/hst2/chapter/4-Evidence-submissions.
|
| [13] |
胡善联. 罕见病药物政策和药物经济学研究的特征[J]. 国际药学研究杂志, 2019, 46(9): 652-658. |
| [14] |
胡娟娟, 陈昕, 龚时薇. 英国、加拿大和澳大利亚国家卫生服务保障体系下罕用药遴选原则分析[J]. 医学与社会, 2016, 29(1): 10-12, 16. |
| [15] |
徐昊鹏, 沈杨, 朱翀, 等. 罕见病卫生技术评估的挑战与应对[J]. 国际药学研究杂志, 2019, 46(9): 645-651. |
| [16] |
李洪, 王小岩, 岳晓萌, 等. 关于中国开展孤儿药卫生技术评估的思考[J]. 国际药学研究杂志, 2019, 46(9): 666-672. |
| [17] |
关轶茹, 相维, 张方. 澳大利亚救生药物计划及对我国罕见病医疗救助制度的启示[J]. 中国卫生政策研究, 2015, 8(8): 51-55. |
| [18] |
Nuijten M, Capri S. Pricing of orphan drugs in oncology and rare diseases[J]. Journal of Market Access & Health Policy, 2020, 8(1): 1-9. |
| [19] |
李立红, 杨小丽. 论平等权视域下罕见病药品可及性的制度困境[J]. 医学争鸣, 2016(6): 59-62. |
| [20] |
张伟涛. 平等权视阈下罕见病的医疗保障[J]. 理论探索, 2014(5): 117-120. DOI:10.3969/j.issn.1004-4175.2014.05.024 |
| [21] |
Silva E N D, Tanara Rosȃngela Vieira Sousa. Economic evaluation in the context of rare diseases: is it possible?[J]. Cadernos De Saude Publica, 2015, 31(3): 496-506. DOI:10.1590/0102-311x00213813 |
| [22] |
Elena Nicod, Panos Kanavos. Scientific and social value judgments for orphan drugs in health technology assessment. 2016, 32(4): 218-232.
|
| [23] |
Zuluaga-Sanchez S, Teynor M, Knight C, et al. Cost Effectiveness of Nusinersen in the Treatment of Patients with Infantile-Onset and Later-Onset Spinal Muscular Atrophy in Sweden[J]. PharmacoEconomics, 2019, 37(6): 845-865. DOI:10.1007/s40273-019-00769-6 |
| [24] |
官海静, 徐菲, 刘国恩. 基于EQ-5D量表的质量调整生命年计算方法探讨[J]. 中国卫生经济, 2015, 34(10): 5-8. |
| [25] |
宗欣, 吴晶. 质量调整生命年: 基础知识[J]. 中国药物经济学, 2009(5): 77-85. DOI:10.3969/j.issn.1673-5846.2009.05.011 |
| [26] |
Eva Rodríguez-Míguez, José-Luis Pinto-Prades. Measuring the social importance of concentration or dispersion of individual health benefits[J]. Health Economics, 2002, 11(1): 43-53. DOI:10.1002/hec.643 |
| [27] |
Kvamme M K, Gyrd-Hansen D, Olsen J A, et al. Increasing marginal utility of small increases in life-expectancy?: Results from a population survey[J]. Journal of Health Economics, 2010, 29(4): 541-548. DOI:10.1016/j.jhealeco.2010.03.010 |
| [28] |
National Institute for Health and Care Excellence. Interim Process and Methods of the Highly Specialised Technologies Programme[R]. London: National Institute for Health and Care Excellence (NICE), 2013.
|
| [29] |
National Institute for Health and Care Excellence. Interim Process and Methods of the Highly Specialised Technologies Programme Updated to reflect 2017 changes[EB/OL](2017-04-01)[2021-10-12]. https://www.nice.org.uk/Media/Default/About/what-we-do/NICE-guidance/NICE-highly-specialised-technologies-guidance/HST-interim-methods-process-guide-may-17.pdf
|
| [30] |
宣建伟, 孙巧. 中国罕见病药物经济学评估适用模型与支付阈值参考标准探讨[J]. 国际药学研究杂志, 2019, 46(9): 659-665. |
(编辑 赵晓娟)





