随着我国疫苗研产能力的提升、居民健康意识的提高,疫苗需求得到释放,2019年各省免疫规划疫苗总接种率普遍超过98%。[1]同时,非免疫规划疫苗的使用也呈现增速加快、覆盖扩面的特点[2],2020年我国非免疫规划疫苗共计批签发5 179批次,批签发数量达6.51亿支,供给保障能力进一步提升[3]。作为准公共产品,疫苗管理涉及研产、流通等复杂流程,适用主体有其特殊性,并具有涉及国民健康的战略意义,必须保障各环节安全、有效、可及。我国政府高度重视疫苗工作,以保障疫苗安全与完善全流程管理为政策着力点,出台了一系列法律法规、政策文件,引导和规制疫苗行业健康发展。2016年,国务院发布《疫苗流通和预防接种管理条例》(简称《条例》),彻底改变了非免疫规划疫苗市场化的流通方式,标志着我国进入全面疫苗监管的新阶段。此后,我国相继提出了“四个最严”“法制化”“标准化”“规范化”“两责任”等多项管理要求,各部门也相继出台相关政策,进一步完善疫苗管理体系。
政策文本是指政府或政党为实现一定的政治、经济、文化及社会目标所采取的行动或规定的行为准则,将一系列理念、措施、方法等上升为法定文本的总称。[4]从运行上看,国家层面的政策文本不仅能有效体现宏观设计的结构、主题等特征,也是地方政策扩散与执行的基本取向[5],更是政策主体调控与管理行为的基准。健康作为普惠性、基础性、长久性的事业,其发展更离不开国家宏观政策的影响,而在药品领域,目前学界多侧重研究行业发展、基本药物、短缺药物等主题的政策文本[6-10],缺少对疫苗这一特殊药品的关注。因此,学界亟需对现行疫苗管理体系的核心内容、演变脉络、价值导向、工具使用特征等进行梳理。本研究拟对2016年后国家层面疫苗管理的政策文本进行量化分析,构建多维分析框架,总结疫苗管理的侧重点,提出相应的优化建议。
1 数据来源与研究方法 1.1 数据来源本研究选取《条例》发布以来,涉及到疫苗管理内容的政策文本作为样本,检索起止时间为2016年4月23日—2022年7月1日,以“疫苗”“预防接种”“免疫”为关键词,检索国务院、国家卫生健康委员会、国家药品监督管理局、国家疾病预防控制中心等官方网站,并同时检索北大法宝、北大法意等法律文本数据库。为保证政策文本的准确性及代表性,纳排标准如下:(1)纳入标准:一是纳入国家层面的疫苗管理政策,即发文单位为全国人大、国务院及各部委颁布的相关政策;二是文本内容包含与疫苗管理相关的信息,并侧重于宏观层面的管理要求;三是文本类型为法律法规、行政规划、意见、通知等,能够充分反应行政意志;(2)排除标准:一是具体操作层面的技术性要求如疫苗储存的温度、疫苗运输的设备等;二是转发类文件。经检索与纳排,最终纳入政策文本17份(表 1)。
| 表 1 2016年以来疫苗管理政策文本基本信息 |
运用内容分析法对文本内容进行系统、客观的量化分析。首先梳理2016年以来疫苗管理政策的发展脉络,其次通过文献回顾、理论分析等确定政策分析框架,通过Nvivo 12.0 Plus软件对纳入的文本进行编码,以“句”为分析单元,并采用“政策文件编号—节点(子节点)—具体条文内容”的编码规则,如:编码3-A11-4表示“编号为3的文件—政策工具为A类的第11个子节点—第4条文本条款”。
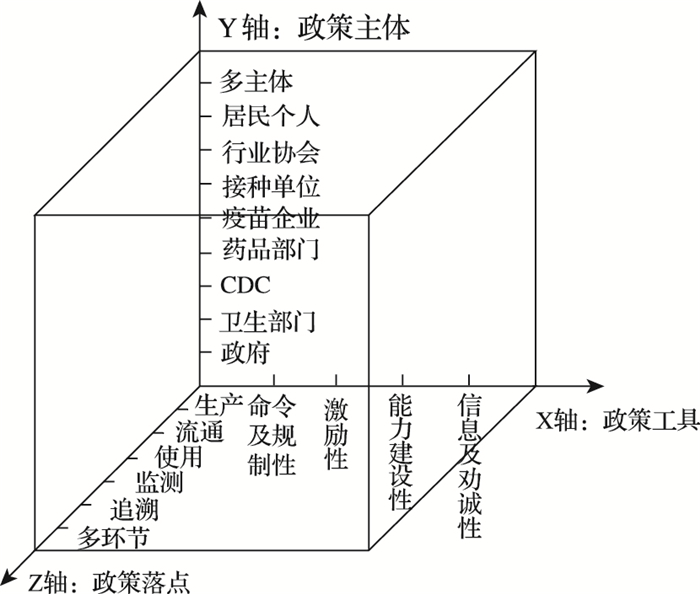
2 三维分析框架构建公共政策分析逐渐向多维、交叉构建,单一的分析框架无法涵盖现实中政策环境、政策作用机制的复杂性。从现实角度,疫苗管理政策涵盖了公众健康、产业发展、国家安全等多元价值,既需要考虑制度设计“度”的影响,也有行业结构“产”的因素,还有利益相关者“行”的逻辑,所以政策工具可以被视为实现政策目标的重要方法,而政策主体则是政策目标贯彻的推进力量,政策落点不仅能反映政策与现实的适配度,更能为政策完善提供参考。本文构建“政策工具—政策主体—政策落点”的多维分析框架(图 1)。
|
图 1 我国疫苗管理政策文本的三维分析框架 |
随着政策科学的发展、西方公共管理改革的深入以及公共政策的复杂化和专业化,学界注重公共决策过程和公共政策自身科学性的同时,更关注研究执行政策的不同方式和工具之间的权衡与选择。[11]政策工具理论(Policy Instrument Theory)率先由美国政治学家Lasswell提出,他认为政策工具是实现政策目标的手段和政策执行的依据,政策工具的设计、选择及运用将直接影响政策效果。[12]主流分类包括:McDonell和Elmore根据政策目标达成手段的强弱,分为规制性、激励性、能力建设性、信息与劝诫性、系统变化性工具[13];Howlett和Ramesh根据政府工具的强制性程度,分为自愿性、强制性和混合性工具[14];Rothwell和Zegveld根据政策工具的影响层面,分为供给型、需求型、环境型政策工具[15]。疫苗管理在政策工具的选择与运用上应充分考虑现实需求、治理目标、可用资源的平衡,因此本研究主要参考McDonell和Elmore的分类,即命令及规制性(mandate)、激励性(inducement)、能力建设性(capacity building)、信息与劝诫性(suasion),主要4种工具描述及21种子工具内涵见表 2。
| 表 2 政策工具内涵 |
政策主体是直接或间接参与政策制定、执行、评估、监测的个人、团体或组织,疫苗政策的贯彻离不开主体间的沟通、配合与协作。在疫苗管理中,相关主体包括:政府及其部门(卫生行政、药品监管等)、疾控机构、疫苗生产经营企业、接种单位、行业协会、居民个人等。
2.3 Z维度:政策落点政策落点即疫苗全流程管理过程中的核心环节。从疫苗的研发生产到受者接种,本研究将其梳理为五大落点,主要包括:疫苗生产(包括研发、注册、上市许可、批签发、产业布局等)、疫苗流通(包括采购、销售、供应、运输、接收、储存、分发等)、疫苗使用(包括个人接种、公共储备、应急接种、区域调用等)、疫苗监测(包括不良反应、安全事件、上市后评价等)、疫苗追溯。
3 研究结果 3.1 单维度分析本研究共形成251条编码。在政策工具上(X维度),以命令及规制性、能力建设性工具的使用为主,分别占比74.90%、16.73%。在规制性工具中,违法违规处理、业务标准、产品标准等子工具使用次数位于前列,占比分别为11.95%、11.55%、11.55%,考核与评价这一子工具的使用次数最少,占比2.39%。在能力与建设性工具中,信息平台、人员培养、战略支撑等子工具使用次数位于前列,占比分别为4.78%、3.98%、3.98%(表 3)。
| 表 3 政策工具维度频数分布情况 |
在政策主体维度(Y维度)上,药品监管部门、疫苗生产经营企业、卫生行政部门、疾病控制机构等主体的出现频次位于前列,分别占比21.51%、17.13%、9.96%、8.37%,同时,多主体的出现频次也较多,占17.53%,体现出了较多协作行动(表 4)。
| 表 4 政策主体与政策落点频数分布情况 |
在政策落点维度(Z维度)上,疫苗使用、疫苗流通、疫苗生产等出现频次位于前列,分别占比31.87%、20.32%、19.92%,同时,多环节融合出现的频次也较多,占比18.33%,意味着在实际操作中贯彻了全流程理念(表 4)。
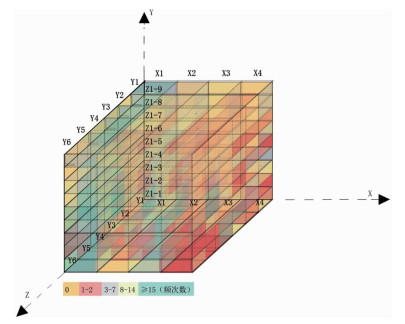
3.2 交叉维度分析不同侧重点的政策文本组成了疫苗管理政策体系。政策工具X、政策主体Y、政策落点Z共同形成了215个立方体,立方体的不同色块代表不同维度交叉出现的频次数,能够反映政策间的耦合程度及偏好特点(图 2)。
|
图 2 疫苗管理政策体系立体图 |
从政策工具—政策主体(即X-Y维度)上看,4种政策工具在不同主体中均有运用,仍以命令及规制性工具为主,以明确违法违规处理、制度建设、业务及操作标准等为前提,建立行为约束、划清行为红线,而其中对药品监管部门、疫苗生产经营企业的规制更多,占比分别为17.13%、15.53%。对居民个人而言,主要运用激励性工具以发挥其主动参与疫苗管理,但占比较少。
从政策工具—政策落点(即X-Z维度)上看,无论运用何种政策工具,疫苗管理的核心旨在建立全流程链条,数据结果显示不仅在各环节中均运用了政策工具,而且将同一政策工具贯彻在多环节,从而保证政策工具使用的连续性。而政策工具在“疫苗使用”这一政策落点中的运用比例最大,占比31.87%,虽然4类工具均有使用,但以命令及规制性工具、能力建设性工具为主。
从政策主体—政策落点(即Y-Z维度)上看,药品监管部门在不同落点的出现频次较多,占比18.31%;而疫苗生产经营企业在各环节都需要承担主体责任,企业主体既需完善自我管理机制,也要接受合理的全流程监管。各主体通过相互配合与共同参与,已经形成合作分工机制,从文本内容上来看,从省、直辖市、自治区,再到各县—乡—镇部门均明确了垂直管理,将各主体在政策落点的职责层层落实。
4 讨论及建议 4.1 政策工具存在结构性失衡,应提升互补性与协调性研究结果表明,我国疫苗管理更偏于选择高规制性、高直接性的政策工具,激励及引导性工具使用不足,其管理模式与药品集中采购政策类似。[7]主要在于疫苗管理与生命健康的强关联决定政府在选择政策工具时必须以效率优先,特别是免疫规划疫苗,各主体必须依靠强制性、半强制性措施来确保高人群接种率,同时规避疫苗管理不善带来的高风险。而随着人群健康需求的不断增加,各主体在人、财、技等配置性资源方面存在结构性短缺,如我国药品监管机构人员存在配备不足、专业能力不强等问题,虽然国务院已于2019年要求重点强化疫苗等高风险药品检查员队伍建设[16],但目前岗位数量有限、薪酬水平低、能否吸引人才还有待观察。因此,面对客观现实,需要主要通过命令及规制性工具以支撑疫苗管理,这一策略对打造疫苗管理新局面确是最适宜的选择。
从公共卫生角度,疫苗得到了高度重视,但从市场而言,其投资吸引力较低,常被置于生物制药研发的次要位置。国外经验表明,疫苗创新受到多种因素影响,包括法律激励、监管框架、合作伙伴互动、技术扩散程度等,其中,管理设计是重要的催化剂。[17]虽然严格的规制可以保障疫苗行业安全发展,但应避免对疫苗市场的过度干预,一方面对非免疫规划疫苗而言,疫苗生产商不能超过其他竞标者的水平,厂家间价格的博弈可能会失去市场份额。利润空间的缩减可能使疫苗公司降低生产成本,这可能不利于产品质量,也会抑制其创新热情。另一方面,相比于得到财政及研究力量支持的大公司,无法从政策中获益的小企业将逐渐被市场边缘化。[18]所以激励性、信息及劝诫性的政策工具可以更好的发挥促进作用,形成政策性合力,以弥补现行管理体系的短板。
综上,应进一步平衡各类政策工具的选取与使用,提高政策之间的互补性,发挥激励性与信息及劝诫性工具在激发主体活力、整合社会资源方面的优势。同时,强化规制性与能力建设性工具的良性互动,提升不同子工具间的适宜性与匹配性,把握疫苗公益性与企业生产性的最佳平衡点。
4.2 命令及规制性政策工具内部不均衡,应注重使用结构本文结果显示,整体上命令及规制性政策工具占比较大,但其内部子工具不均衡,在风险监测与控制、信息发布及公开、储备及调用、考核评价等重要环节的要求偏低,应结合各环节的现实问题,制定针对性的策略,加强不同子工具的配合使用,形成共力同向、协调并重的使用结构。从全局来看,防范和化解潜在风险与居民健康和免疫效果紧密相关,应建立起事前预防、事中处理、事后恢复的管理流程,定期检查风险预案的落实情况,并进一步明确处置环节的主体责任划分,加强从上至下的监测与沟通,促进各层级及各主体间的互联互通,提升监测接种不良事件的灵敏度与规范性,建立系统性的不良事件补偿机制与标准。[19-23]现阶段,虽然我国已对疫苗信息的公开主体与公开内容进行界定,但疫苗信息公开制度的刚性执行情况并不理想,存在信息碎片化、内容单一、更新速度慢、查询渠道少等问题[24-25],应进一步明确疫苗信息公开的程序、方式、期限等,考虑在政府网站设立专项疫苗监管信息公开指引[26],使监管部门、疫苗生产企业、公众都能充分了解可公开、应公开、快公开的信息及渠道,同时,建立对疫苗公开信息的监督及反馈机制,避免信息公开主体与责任主体兼任导致的信息失真。对于疫苗储备,我国建设时间较短,且疫苗产业的薄弱基础与有效储备的高投入、集聚化要求存在较大差距,应当坚持政府的主体责任,加强疫苗生产企业、流通企业、疾病预防控制中心的协作力量,组建疫苗供应保障高层次协同平台、根据“以需定产、适度宽裕、多措激励”的原则实施产业政策[27-28],促进组织架构、产业结构、协同网络的多维共建。目前,疫苗接种情况在接种单位及行政主管部门的绩效考核占比不大[29],并且考核具有滞后性,“他评”式的考核方式也容易产生依赖,难以主动发现工作短板及不足[30],应当发挥绩效的导向与激励作用,将疫苗的温度管理融入预防接种服务,将疫苗的安全管理嵌入行政管理,促进疫苗管理主体的自我完善与持续改进。
4.3 政策主体的分工与协作趋势明显,应深化参与程度我国疫苗管理体系从政府监管逐渐转型为公共治理,各级政府的领导责任、相关部门的监管责任、企业的主体责任、社会力量参与责任都得到较为清晰的界定[31],而多主体的合作趋势明显。但目前的发文机构集中在单一的卫生行政部门、药品监管部门等,客观上虽然能够保证行政命令的高度一致性,但疫苗管理的多环节、长链条离不开跨部门合作,各部门应从立场、政策、举措进行深度统一,贯彻疫苗管理部际联席会议制度,强化联席会商与联合督导。国际经验表明疫苗管理的资源应分散在不同参与者中,非政府行为者的监管能力越来越得到国家的重视与认可。[32]要实现疫苗监管目标,必须调动与挖掘非政府行为者的资源,通过优势互补形成共同的监管力量。例如,加拿大疫苗监管机构经常就免疫问题与非政府机构进行公开对话,不仅有助于制定高效的疫苗政策,也提高了疫苗审查过程的透明度并促进问责制的落实。[33]美国发动联邦、各州力量,共同为居民提供免疫接种的沟通资料,美国国家公共卫生信息联盟、国家医学科学院、医院协会等组织合作支持卫生系统以解决免疫接种的不信任问题,同时对于政府的行为提出建议,及时监测疫苗质量。[34]
我国现行作用于公众、行业协会等非政府行为者的政策较少,可以进一步加强引导,广泛调动社会公众的参与积极性,鼓励公众参与到疫苗管理评价、监督与反馈的进程,充分发挥公众的监督评价作用,借鉴日本、美国等国的疫苗协会建设经验,完善行业协会的自我监管机制[35],引导疫苗企业依法开展生产经营活动。同时,可以完善公益诉讼机制,现行的《行政诉讼法》只允许人民检察院以政府在药品监管中的不当行为或不作为为由提起公益诉讼,可以探索给予非政府组织提起公益诉讼的能力,以便更有效地利用非政府行为者来确保疫苗安全。[18]
4.4 政策落点的匀实性不强,应做好紧密衔接目前,各政策落点已建立了较为稳定的连接,但较集中于使用、流通、生产等前端及终端环节,对于后端的监测与追溯仍待深化。一方面,国家药品监督管理总局自2019年以来累计印发与疫苗追溯相关的5项标准[36],但疫苗全过程的信息化整合难度较大,推进速度较慢,所以应凝聚工作共识,加大各地区对标转化、数据集建设等工作力度,鼓励有条件、有能力的地区试点先行,探索大数据、人工智能、物联网等新技术在疫苗追溯这一场景中的应用潜力。另一方面,我国预防接种监测系统存在报告不足及报告偏见的问题,需要借鉴国际上主动监测与持续监测结合的模式[37],进一步革新监测数据挖掘方法,将疫苗接种数据与临床数据链接,以实现更强的因果关系评估。
致谢
本研究为比尔和梅琳达·盖茨基金会(INV-034554)支持的“疫苗与免疫服务提供创新实验室”项目产出。盖茨基金会未参与研究设计、数据分析、数据解释、文章写作或提交等。本文内容完全由作者负责,不代表资助者的任何观点。
作者声明本文无实际或潜在的利益冲突。
| [1] |
叶家楷, 曹雷, 余文周, 等. 中国2016-2019年适龄儿童国家免疫规划疫苗常规免疫接种率监测[J]. 中国疫苗和免疫, 2022, 28(1): 94-100. DOI:10.19914/j.CJVI.2022019 |
| [2] |
袁平, 金雅玲, 郑景山, 等. 2014年中国第二类疫苗接种监测数据分析[J]. 中国疫苗和免疫, 2016, 22(2): 143-148, 158. |
| [3] |
中国食品药品检定研究院. 中检院生物制品批签发信息公示表[EB/OL]. (2021-01-01)[2022-08-11]. https://www.nifdc.org.cn/nifdc/xxgk/ggtzh/jwgk/shwzhppfgg/index.html
|
| [4] |
任弢, 黄萃, 苏竣. 公共政策文本研究的路径与发展趋势[J]. 中国行政管理, 2017(5): 96-101. |
| [5] |
吴林海, 陈宇环, 陈秀娟. 中国食品安全风险治理政策工具的演化轨迹与内在逻辑[J]. 公共治理研究, 2022, 34(3): 32-45. |
| [6] |
袁野, 杨清清, 邓维斌, 等. 基于政策工具的我国生物医药产业政策文本分析[J]. 中国卫生经济, 2022, 41(3): 81-86. |
| [7] |
宋佳, 范成鑫, 王婉晨, 等. 利益相关者视角下我国药品集中带量采购政策研究——基于政策工具的文本分析[J]. 中国卫生政策研究, 2022, 15(2): 11-17. |
| [8] |
谭清立, 梁诗渝. 基于政策工具的短缺药供应保障机制的推进与优化研究[J]. 中国卫生政策研究, 2021, 14(12): 26-33. |
| [9] |
刘曦, 邓蒙, 刘伟, 等. 2009-2020年国家基本药物制度政策文本研究[J]. 中国卫生政策研究, 2021, 14(5): 35-41. |
| [10] |
王瑞丽, 朱嘉亮, 黄志禄. 基于NVIVO 12.0及政策文本的国家药品抽检发展历程分析[J]. 中国药业, 2021, 30(3): 6-10. |
| [11] |
黄红华. 政策工具理论的兴起及其在中国的发展[J]. 社会科学, 2010(4): 13-19, 187. |
| [12] |
孙志建. 政府治理的工具基础: 西方政策工具理论的知识学诠释[J]. 公共行政评论, 2011, 4(3): 67-103, 180-181. |
| [13] |
Mc Donnell L M, Elmore R F. Getting the Job Done: Alternative Policy Instruments[J]. Educational Evaluation and Policy Analysis, 1987, 9(2): 133-152. |
| [14] |
Howlett M, Ramesh M. Studying Public Policy: Policy Cycles and Policy Subsystems[M]. London: Oxford University Press, 1995.
|
| [15] |
Rothwell R, Zegveld W. Reindusdalization and Technology[M]. London: Logman Group Limited, 1985.
|
| [16] |
国务院办公厅. 关于建立职业化专业化药品检查员队伍的意见[EB/OL]. (2019-07-09)[2022-08-11]. https://www.nmpa.gov.cn/xxgk/fgwj/qita/20190718080001391.html
|
| [17] |
Rutschman A. The Vaccine Race in the 21st Century[J]. Political Science, 2019, 61: 730-770. |
| [18] |
Feng J, Li Q. How to ensure vaccine safety: An evaluation of China's vaccine regulation system[J]. Vaccine, 2021, 39(37): 5285-5294. |
| [19] |
张敬雅. 突发公共卫生事件应急处置流程研究[D]. 长春: 东北师范大学, 2021.
|
| [20] |
姚立辉, 张秋. 疫苗安全突发事件对应急管理的启示[J]. 中国药师, 2020, 23(8): 1608-1611. |
| [21] |
韩敏. 我国疫苗责任强制保险发展研究[D]. 石家庄: 河北经贸大学, 2020.
|
| [22] |
叶泽明. 疫苗问题的思考: 内地与香港应急管理体系比较研究及启示[J]. 现代商贸工业, 2019, 40(7): 137-139. |
| [23] |
董铎. 我国疫苗不良事件监测体系研究[D]. 沈阳: 沈阳药科大学, 2007.
|
| [24] |
丁丽莹. 论我国疫苗安全监管制度的完善[D]. 大连: 辽宁师范大学, 2020.
|
| [25] |
唐裕佳. 我国免疫规划存在的问题及其对策研究[D]. 重庆: 中共重庆市委党校, 2022.
|
| [26] |
任龙军. 疫苗行政监管法律制度研究[D]. 哈尔滨: 黑龙江大学, 2022.
|
| [27] |
胡颖廉. 协同应对未知: 国家疫苗产能储备制度构建探析[J]. 中国行政管理, 2020(5): 26-31. |
| [28] |
宋劲松, 刘杰. 我国大规模传染病应急产品产能储备研究[J]. 南京社会科学, 2020(3): 28-36, 47. |
| [29] |
马永闯. 我国一类疫苗接种服务现状研究[D]. 苏州: 苏州大学, 2020.
|
| [30] |
邢立镛, 林秀旎, 周慧贤, 等. 构建满足WHO全球基准评估工具(GBT)的药品监管部门疫苗监管质量管理体系研究[J]. 中国药事, 2022, 36(4): 391-398. |
| [31] |
宋华琳. 疫苗管理的体系建构与法律制度创新—《中华人民共和国疫苗管理法》立法解读[J]. 中国食品药品监管, 2019(7): 4-12. |
| [32] |
PeterGrabosky. Using Non-Governmental Resources to Foster Regulatory Compliance[J]. Governance, 1995, 8(4): 527-550. |
| [33] |
Government of Canada. Canada Vaccine industry Committee, Building on the Legacy of Vaccines in Canada: Value, Opportunities, and Challenges Series[EB/OL]. (2020-03-11)[2022-08-11]. https://www.canada.ca/en/health-canada/services/health-care-system/reports-publications.html.
|
| [34] |
Shashank S, Venkatesh M P. Vaccine Regulation, Licensing and Approval in USA[J]. Journal of Pharmaceutical Research International, 2021, 33(60): 664-673. |
| [35] |
张彤彤. 《疫苗管理法》出台背景下疫苗生产监管的实施困境与应对策略研究[D]. 兰州: 西北民族大学, 2020.
|
| [36] |
中华人民共和国商务部. 国家疫苗追溯标准规范包含哪些?[EB/OL]. (2020-03-11) [2022-08-11]. https://zycpzs.mofcom.gov.cn/html/zhishiwenda/2020/3/1583906339496.html
|
| [37] |
Liu D, Wu W, Li K, et al. Surveillance of adverse events following immunization in China: Past, present, and future[J]. Vaccine, 2015, 33(32): 4041-4046. |
(编辑 薛云)





