2. 清华大学医院管理研究院 广东深圳 518055
2. Institute for Hospital Management of Tsinghua University, Shenzhen Guangdong 518055, China
基因治疗药物(Gene therapy drug)是一种新型生物医药产品,通过修复、抑制或引入基因来治疗特定遗传缺陷。[1]与传统治疗相比更为精准、个性化,有望减少副作用和提高治疗效果[2-3],还能为癌症等疾病提供新的治疗路径[4-5],有望延长患者生存期,提高生活质量[6-7]。
1993年以来,我国出台多项政策推动基因治疗研究与转化应用,《基因工程安全管理办法》和《人的体细胞治疗及基因治疗临床研究质控要点》等,为基因疗法提供了质量控制指导方针。2023年出台的《药审中心加快创新药上市许可申请审评工作规范(试行)》进一步明确了创新药上市审批流程,促进了基因治疗药物的市场准入和应用。经过40余年的政策演进,我国已形成了多元化监管模式,这不仅为基因治疗药物的研发和市场化提供了稳定支持,也为实现生物医药行业的高质量发展奠定了基础。
虽然现有研究已经关注到基因治疗药物领域,特别是在孤儿药和特定治疗产品的分析上,但对基因治疗药物政策文本的系统研究仍显不足,通常仅局限于研发或上市的单一阶段展开探讨。[8]因此,本文通过构建涵盖政策工具—互动主体—政策环节的三维分析框架,结合统计学方法,对基因治疗药物政策进行系统研究[9],以期厘清当前基因治疗药物政策现状,为优化基因治疗药物政策提出建议。
1 资料与方法 1.1 资料来源以“基因药”“基因治疗”“基因修饰细胞治疗”等为关键词,通过访问国务院、国家卫生健康委员会、国家发展和改革委员会、国家药品监督管理局、国家药品监督管理局药品审评中心等相关部委和下属机构的官方网站,补充检索北大法宝数据库,纳入由国务院部委及直属机构发布的,与基因治疗药物紧密相关的法规条例、政策条文、指导意见、通知、产业结构目录、创新规划等政策文件。纳入与排除标准如下:(1)纳入标准:发文单位为国家级层面;政策文件与基因治疗药物的研发、生产、临床应用等环节紧密相关。(2)排除标准:政策文件内容不涉及基因治疗实质性内容的文件;解读、新闻报道或答疑解惑类的非政策性文件;与已纳入文件内容重复或高度相似的文件。由于2009年前相关政策文件数量较少(仅有1993年发布了2份政策文件),因此将2009年颁布《医疗技术临床应用管理办法》作为基因治疗政策研究的起始时间节点,经2名评价员分别人工筛选后讨论,最终选取2009年3月—2024年3月国家层面发布的37份相关政策文件(表 1)。
| 表 1 2009年以来国家层面的基因治疗药物政策文本示例 |
本文运用内容分析法与词频分析法。首先,基于政策工具视角,使用NVivo20软件量化分析纳入的政策文件,编码方式为“政策序号-章号-条目号/段落号-内容”。其中,政策类条文条目较为清晰,故以条目为单位进行编码;指导类文件以段落为单位进行编码(将主题接近的段落归为一段)。若同一条政策条目涉及多个政策工具或互动主体,该条目可被多次统计,文本编码示例如表 1所示。其次,本文将基因治疗药物政策文件按照不同环节分为研发、生产和使用3类,使用3D文字云3.1.6版本软件对每个环节文件中的高频词汇进行分析统计。
| 表 2 部分基因治疗药物政策文件内容编码情况 |
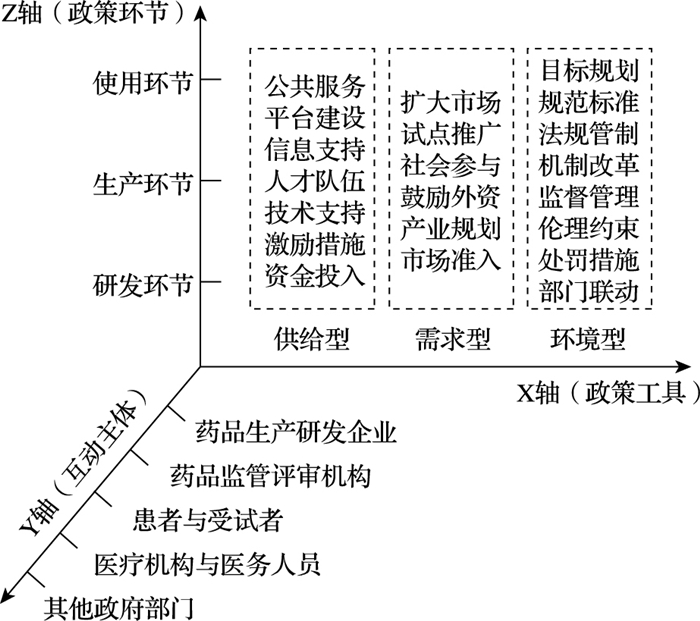
基于政策工具理论,结合我国基因治疗药物政策的实际情况,构建针对我国基因治疗药物相关政策的“政策工具—互动主体—政策环节”三维分析框架(图 1)。
|
图 1 基因治疗政策三维分析框架 |
政策工具分类法被广泛运用于医疗卫生政策的量化研究中[10],本研究沿用Rothwell和Zegvelad提出的基本政策工具分类法[11],将政策工具分为供给型、需求型和环境型三大类[12],侧重于比较不同类型的政策工具在政策制定与施行过程中的作用,体现政策的推力、拉力与影响力之间的互动关系[13]。
本研究根据政策具体内容,将供给型、需求型和环境型政策工具的定义进行优化:供给型政策工具主要包括政府在资金和技术方面对基因治疗药物研发、生产和临床应用的扶持措施,旨在增强产业的研发能力和生产效率,从而提高基因治疗药物的供给水平;需求型政策工具侧重通过激励措施和引导策略,促进公众、医疗机构和医药企业对基因治疗药物的需求,旨在有效地扩大市场,推动基因治疗药物的广泛应用;环境型政策工具则主要包括政府对基因治疗药物产业发展提供的政策环境和制度支持,旨在构建稳定、可预测的产业发展环境,为长远发展提供坚实基础(表 3)。
| 表 3 各维度具体涵义及关键词 |
| 表 4 基本政策工具分布 |
在基因治疗药物的研发、生产、推广和使用过程中,涉及到政府机构、医疗机构、患者及相关制药企业等多个利益相关者的利益均衡和协调。因此,必须全面考虑各方因素,制定统一的标准和规范[14],以确保基因治疗药物的安全性和有效性。
本研究将参与者分为五大主体:药品研发生产企业、药品监管评审机构、患者与受试者、医疗机构与医务人员、其他政府部门,以期更加清晰地识别各方的需求和责任,进而制定出更加协同有效的政策和措施。
2.3 Z维度:政策环节维度政策环节存在连贯性,在基因治疗药物方面体现在从实验室到市场的场景是连续的,同时从研发到临床应用的整个流程也是连续的。每个环节都需要特定的政策支持和规范,明确每个环节的政策重点有助于理解整个流程的监管逻辑和实施效果。
本研究依据研发、生产和使用三个主要环节将基因治疗药物的政策文件进行划分,研发阶段的政策重点在于鼓励创新和保护知识产权,以促进基础研究和早期药物发现;生产阶段政策应关注生产过程的安全性、质量控制和供应链管理;使用阶段的重点是确保药物的可及性和可负担性。通过梳理各阶段的政策重点,本研究旨在揭示政策如何影响基因治疗药物的全生命周期发展,从而为政策制定者提供决策支持。
3 结果 3.1 基本情况研究纳入的37份政策文件均为国家级文件。从发文数量来看,基因治疗药物的政策数量与日俱增,体现了我国对于这一领域的高度重视。从文件类别来看,指导原则在纳入的政策中占比较高(75.68%),包含22例临床研究技术指导原则和6例非临床研究技术指导原则,其存在和数量分布揭示了政府在药物研发过程中对于不同阶段的关注点和规范要求。从政策目标来看,我国基因治疗药物政策围绕多元目标综合施策。可将政策目标归纳整理为:(1)鼓励和支持基因治疗药物的研发和创新;(2)提升基因治疗药物的生产能力和供应链管理水平;(3)保障基因治疗药物的安全性与有效性;(4)促进加强基础研究与临床应用的结合;(5)提高基因治疗药物的普及率和可及性。
3.2 政策工具维度如表 3所示,政策工具共筛选出246个文本条目,综合运用了多种政策工具,但三类政策工具之间的使用比例存在明显差异。其中,供给型政策工具的使用频率最高,文本条目数量为113(45.9%),其次使用较多的是环境型政策工具,数量为102(41.5%),而需求型政策工具占比明显偏少,数量为31(12.6%)。
具体而言,不同政策工具内部各个维度之间也存在较大的差异。在供给型政策工具中,技术支持占70.8%,而其他各个维度的占比则相对较少。需求型政策工具占比整体偏少,其中扩大市场与产业规划的政策条目略多,其余维度较为均衡。环境型政策工具中,关于监督管理、规范标准与机制改革的政策条目较多,分别占25.5%、22.5%和20.6%,而关于机制创新和处罚措施的政策条目较少。
3.3 互动主体维度分析互动主体维度共筛选出195个文本条目,各互动主体维度的占比较为均衡。其中,以药品生产研发企业为主体的文本条目数量最多,为72条,占36.9%;其次为药品监管评审机构,数量为43条,占22.1%;患者与受试者、医疗机构与医务人员分别占19.0%与11.8%;占比最少的是其他政府部门,数量为20条,占10.2%(表 5)。
| 表 5 互动主体各维度分布 |
我国的基因治疗药物政策全面覆盖了药物研发、生产和使用的各个关键阶段,部分政策涉及多个相关环节。本文对37份政策进行整体分析,其中,20份政策仅涉及一个环节,17份涉及两个及以上环节,4份涉及三个环节。其中,涉及基因治疗药物研发环节的政策文件最多,共计32份,占86.5%;16份政策文件涉及生产环节,主要关注基因治疗药物的生产管理、质量控制、风险防控等方面;涉及基因药物使用环节的政策文件相对较少,共10份,对于药物的临床应用、市场推广、患者管理等方面进行具体规范。
按照基因治疗药物政策文件的不同环节分别进行词频分析发现,在研发环节,高频词主要聚集于研究与开发的具体过程;在生产环节,高频词汇如“生产”“产品”等词体现出对生产的具体流程与产出结果的关注;而在使用环节,“科技”“伦理”“审查”等高频词汇反映出政策在药物的使用过程中需要综合考虑伦理规范。同时,“主管部门”“医疗机构”等词在其他两环节较少提及,为使用环节特有,直观表现出在药物使用环节需要多机构协同配合(表 6)。
| 表 6 基因治疗药物政策不同环节词频分析侧重点比较 |
将政策工具(X维度)和互动主体(Y维度)叠加,可了解不同互动主体对各类政策工具的关注重点。从而分析各主体在不同政策工具中的参与程度和侧重领域。政策工具在各互动主体中的应用主要体现在供给维度和环境维度。药品生产研发企业的政策工具响应总频次最高,其次为其他政府部门,而针对患者与受试者的政策工具出现频次最低。对政策子工具分析发现,针对药品生产研发企业的技术指导子工具响应频数最高,且远高于其他维度;环境维度的细分领域对于各个互动主体的应用范围最为广泛,其中的规范标准子工具涉及了所有互动主体(表 7)。
| 表 7 政策工具—互动主体交叉维度分布 |
如图所示,针对不同政策环节三个维度政策工具的使用较为广泛。从数量上看,供给型和环境型政策工具使用较多,需求型政策工具在各环节中使用均较少。其中频次最高的是研发环节的技术指导子工具,其次是生产环节的技术指导子工具、研发环节的规范标准和监督管理子工具。在基因药的各个环节,均运用到技术指导、扩大市场、产业规划、市场准入、规范标准、法规管制、监督管理、伦理约束这8类政策子工具,一定程度上兼顾了研发环节、生产环节和使用环节的全流程,而公共服务、激励措施、试点推广和体制建设4类政策子工具则应用较少(表 8)。
| 表 8 政策工具—政策环节交叉维度分布 |
如表 9所示,研发环节药品生产研发企业出现频次最多,其次是药品监管评审机构;生产环节中,药品生产研发企业出现频次占绝大多数,其余各主体出现频次均较少;使用环节除患者与受试出现频次较少之外,其余各主体分布较为均衡。
| 表 9 互动主体—政策环节交叉维度分布 |
在综合分析我国基因治疗药物政策时,发现政策工具在研发、生产和使用环节分布不均。需求型政策工具尤其不足,政策拉动效应有限;供给型政策工具虽占主导,但主要集中在技术支持上,大部分为对基因治疗领域的基础研究和关键核心技术进行原则指导;而环境型政策工具虽分布均衡,但加强技术指导、伦理审查和人类遗传资源审批等关键领域的规范和完善不足。
因此,在新政策的制定过程中应当进一步平衡各类政策工具的选取,提高政策之间的互补性。一是强化需求型政策工具,应将需求型工具与其他政策工具结合,加大对基因治疗药物研发与推广的扶持力度。通过产业规划、税收优惠和市场准入支持等措施,推广行之有效的试点经验,拓展基因治疗药物市场的发展空间。同时,倡导社会参与,加强公众对基因治疗药物的认知,提高政策的透明性和合理性。[15-16]二是优化供给型政策工具,供给类政策应从单一的技术指导转向促进公共服务和基础设施建设,形成基因资源在安全监管下共享共用的新格局。加强公共服务支持,推动第三方专业服务平台与孵化器的建设,利用现代技术提高药物研发效率和公共服务能力。建设科技创新基地和专业孵化器,建立符合国际标准的生产流程和质量管理体系,提升基因治疗领域的创新策源能力和成果转化应用水平。三是细化环境型政策工具,明确政策落点,加强技术指导、伦理审查和人类遗传资源审批等关键领域的规范和完善。坚守生物安全底线,考虑地区伦理和文化差异,确保基因治疗技术的接受度和应用方式。[17-18]
4.2 互动主体交叉,合作促进共赢我国基因治疗药物各互动主体在政策中的占比频次相对均衡,药品生产研发企业在研发与生产环节的政策关注度最高,这反映了其在基因治疗药物产业链中的核心地位。药品监管评审机构的占比紧随其后,显示了政策对于规范和监管的重视。患者与受试者的关注体现了政策对临床获益和安全性的考量,而医疗机构与医务人员的占比则反映了基因药物使用场景的重要性。其他政府部门的占比最少,这可能表明政策在促进跨部门协调和合作方面还有提升空间。
建议针对药品生产研发企业,应提供优化研发与生产环节的政策支持,给予更多税收优惠、资金支持等激励措施,以鼓励其加大研发投入,推动技术创新和产品迭代。[19]鼓励国内企业参与国际合作,引进国外先进技术和管理经验,提升我国基因治疗药物的国际竞争力。针对监管评审机构,政策应进一步完善注册审批流程,防止不合格药品流入市场。引导其加强专业能力建设,要求其充分验证基因治疗药物的疗效,证明其相对于传统治疗方法所增加的额外成本合理且有效。[20]针对患者和临床试验受试者,政策应加强对其权益的保护,同时提高他们对基因治疗药物的认知和接受度。鼓励对其开展长期跟踪研究,验证基因治疗药物的长期疗效和安全性,仔细评估治疗对患者、家庭和社会的益处和负担。[21]针对医疗机构与医务人员,政策应鼓励其在基因治疗药物的使用和推广中发挥更大作用,促进在提供培训、优化治疗方案等方面的参与。最后,针对其他政府部门,政策应进一步明确其职责和协作机制,确保政策在研发、生产、使用等各环节的连贯性和有效性,强化跨部门协调机制。
4.3 环节联动增效,构建全链条生态我国基因治疗药物政策已经初具各环节全面的政策覆盖,体现了对基因治疗药物全生命周期的细致管理和指导。政策中,大部分文件涉及多个环节,少数文件覆盖三个环节。政策文件主要集中在研发环节,覆盖率远高于非临床和使用环节,这种差异可能源于临床研究直接关联到人体试验,其安全性和有效性评估对于药物能否进入市场至关重要。此外,临床阶段的研究往往更接近产品商业化。相比之下,使用环节的政策文件较少,缺乏在消费端的经济性分析,这可能与需求型政策工具的不足有关。此外,词频分析中并未出现药物可及性、成本效益分析、医保覆盖等内容,但现实中基因药物的高成本仍是挑战,说明对基因治疗药物的经济性和费效比尚缺乏政策考量。
在研发环节,政策应补充非临床阶段技术指导原则。在非临床研究阶段提供更多的指导和支持,顺应我国人口老龄化趋势,引导年龄相关退行性疾病与慢性疾病的基础机制[22],以确保基因治疗药物的科学性和有效性,从而为临床研究打下坚实的基础。在生产环节,政策应明确涉及研发支持、生产监管、市场准入、医保报销等具体领域,设定清晰的实施时间表和阶段性目标,促进产业链协同发展,促进上下游紧密结合。[23]在使用环节,政策在保障药物的可及性和可负担性方面相对薄弱,需从着重监管逐步转向加强需求引导并重。应加强经济评价,确保成本效益和药物的可及性与合理定价,确保药品质量和供应的稳定性,扩大患者的可及性和可选方案[24],从长远和可持续的角度出发,平衡创新激励和公共利益。综上,政策应更加均衡地覆盖研发、生产和使用环节,满足市场需求和患者利益。
作者声明本文无实际或潜在的利益冲突。
| [1] |
Kesharwani R K, Misra K. Biotechnology in the Modern Medicinal System: Advances in Gene Therapy, Immunotherapy, and Targeted Drug Delivery[M]. CRC Press, 2021.
|
| [2] |
Rakesh K S. Therapeutic Approaches for the Management of Autoimmune Disorders via Gene Therapy: Prospects, Challenges and Opportunities[J]. Current gene therapy, 2022, 22(3): 245-261. DOI:10.2174/1566523221666210916113609 |
| [3] |
Dunbar C E, High K A, Joung J K, et al. Gene therapy comes of age[J]. Science, 2018, 359(6372): 1-11. |
| [4] |
High K A. Turning genes into medicines: what have we learned from gene therapy drug development in the past decade?[J]. Nature Communications, 2020, 11(1): 1-4. DOI:10.1038/s41467-019-13993-7 |
| [5] |
Belete T M. The current status of gene therapy for the treatment of cancer[J]. Biologics: Targets and Therapy, 2021, 15: 67-77. DOI:10.2147/BTT.S302095 |
| [6] |
Hashem H G. Ocular Gene Therapy: A Literature Review with Special Focus on Immune and Inflammatory Responses[J]. Clinical ophthalmology (Auckland, NZ), 2022, 16: 1753-1771. DOI:10.2147/OPTH.S364200 |
| [7] |
Ling P. Huntington's Disease: New Frontiers in Therapeutics[J]. Current Neurology and Neuroscience Reports, 2021, 21(3): 1-9. |
| [8] |
史海涛, 谢正福, 何本霞, 等. 细胞和基因治疗产品现状与我国监管政策研究[J]. 中国食品药品监管, 2024(6): 46-55. |
| [9] |
中华医学会眼科学分会眼底病学组, 中国医师协会眼科医师分会眼底病专业委员会. 中国遗传性视网膜疾病基因治疗手术安全性管理和视功能评价指标设定专家共识[J]. 中华眼底病杂志, 2022, 38(8): 636-642. DOI:10.3760/cma.j.cn511434-20220808-00442 |
| [10] |
李玥茗, 卓丽军, 朱静佳, 等. 基于政策工具的我国中医药科技创新政策文本分析[J]. 中国卫生政策研究, 2024, 17(1): 36-42. |
| [11] |
Rothwell R, Zegveld W. An assessment of government innovation policies[J]. Review of Policy Research, 1984, 3(3-4): 436-444. DOI:10.1111/j.1541-1338.1984.tb00138.x |
| [12] |
李浩, 戴遥, 陶红兵. 我国DRG政策的文本量化分析: 基于政策目标、政策工具和政策力度的三维框架[J]. 中国卫生政策研究, 2021, 14(12): 16-25. |
| [13] |
赵筱媛, 苏竣. 基于政策工具的公共科技政策分析框架研究[J]. 科学学研究, 2007(1): 52-56. DOI:10.3969/j.issn.1003-2053.2007.01.011 |
| [14] |
常浩然, 杨锦茹, 胡善菊, 等. 基于三维分析框架的我国药品集中带量采购政策量化分析[J]. 中国卫生事业管理, 2023, 40(2): 122-127. |
| [15] |
张军, 李笑蕾, 任跃明. 中国与欧盟、美国基因治疗产品安全性监管研究[J]. 中国药事, 2021, 35(4): 368-379. |
| [16] |
Takamura K, Tachibana K, Kusakabe T, et al. New Japanese regulatory frameworks for post-marketing management of pharmaceutical products[J]. Pharmaceutical Research, 2020, 37: 1-5. DOI:10.1007/s11095-019-2719-z |
| [17] |
高建超, 韦薇, 张旻, 等. 细胞和基因治疗产品监管科学研究进展和展望[J]. 中国新药杂志, 2022, 31(2): 105-108. |
| [18] |
Kozan D W, Farber S A. Is It Ever Wise to Edit Wild-Type Alleles? Engineered CRISPR Alleles Versus Millions of Years of Human Evolution[J]. Arteriosclerosis, Thrombosis, and Vascular Biology, 2024, 44(2): 328-333. |
| [19] |
Moumné L, Marie A-C, Crouvezier N. Oligonucleotide therapeutics: from discovery and development to patentability[J]. Pharmaceutics, 2022, 14(2): 1-24. |
| [20] |
Kerpel-fronius S, Baroutsou V, Becker S, et al. Development and use of gene therapy orphan drugs: ethical needs for a broader cooperation between the pharmaceutical industry and society[J]. Frontiers in Medicine, 2020, 7: 1-9. |
| [21] |
Ryan M M. Gene therapy for neuromuscular disorders: prospects and ethics[J]. Archives of Disease in Childhood, 2022, 107(5): 421-426. |
| [22] |
冯雪娇, 衡超, 于新语, 等. 基因治疗行业市场分析及展望[J]. 中国生物工程杂志, 2023, 43(6): 102-112. |
| [23] |
Nishida Y, Kodama K, Sengoku S. The gap between development and manufacturing in gene therapy: Strategic options for overcoming traps[J]. Drug Discovery Today, 2023, 28(2): 103429. |
| [24] |
Rogers S L, Keeling N J, Giri J, et al. PARC report: a health-systems focus on reimbursement and patient access to pharmacogenomics testing[J]. Pharmacogenomics, 2020, 21(11): 785-796. |
(编辑 赵晓娟)





