2. 复旦大学全球健康研究所 上海 200032
2. Global Health Institute, Fudan University, Shanghai 200032, China
医药产品(Health Products)的全球采购是促进全球健康至关重要的环节。全球采购能够在全球范围内有效匹配需求与供给,实现资源的合理再分配。[1]通过全球采购,各国和各多边组织能够从来自不同国家或地区的供应商处获得产品、服务或原料,以满足其所在国家、地区或组织援助地区的需求。
《“十四五”生物经济发展规划》指出,我国要“积极参与全球生物安全治理,推动生命科学、生物技术双边和多边国际合作,促进创新要素合理流动,实现生物经济效益互利共赢”。[2]参与医药产品的全球采购是中国医药产业更大范围、更宽领域和更深层次的融入世界卫生经济的重要途径。然而,我国目前在多边组织全球采购中的参与度却仍然不高。抗击艾滋病、结核病和疟疾全球基金(The Global Fund to Fight AIDS,Tuberculosis and Malaria,以下简称“全球基金”)采购的价格和质量报告数据库(Price & Quality Reporting System)数据显示,我国在2022年全球基金全球采购的份额中仅占11.96%。[3]
全球基金是全球最重要的卫生援助筹资机构之一,其迄今为止已筹集并分配超过537亿美元支持全球范围内的卫生援助项目。[4]为了确保大量援助资金的高效利用,全球基金形成了其独特、复杂的采购和监管模式,也深刻影响着医药产品的全球采购链。
因此,本研究以全球基金为例,采用定性和定量研究方法,分析全球基金开展医药产品采购的具体机制、制度标准、采购现况以及中国对全球基金采购的供应现状。以期为促进中国企业和产品未来进一步融入全球医药产品采购链提供建议与参考。
1 资料与方法本研究采用文献分析法,以“Procurement”“Health products”“Prequalification”为关键词,在全球基金以及其他相关组织机构的官网检索政策文件,包括《全球基金医药产品采购和供应管理政策指南》《全球基金质量控制政策》《全球基金运营政策手册》等。从全球基金开展采购的方式、采购产品的质量要求和相应认证流程等方面,分析总结全球基金开展全球采购的特点。
采用二手数据定量描述,分析全球基金采购产品的主要供应商、供应国及其随时间变化的趋势,以及中国在全球基金采购中的参与情况。定量数据来源于全球基金采购的价格与质量报告数据库中订单采购日期(Purchase Order Date)在2013年1月1日至2022年12月31日的数据。
本研究采用专家咨询法,针对全球基金采购特点、医药产品质量认证流程和认证标准、中国参与全球采购的挑战等问题开展专家咨询,旨在对本研究定性与定量分析结果进行补充和验证。专家选择标准为:(1)在医药产品采购领域或国际质量标准认证领域有5年及以上工作经验;(2)在知情同意的前提下自愿参与研究并能积极配合。研究最终向8名专家开展咨询。
2 全球基金开展全球采购的方式全球基金及其赠款受援方开展全球采购的具体方式可以分为三类:自行采购、通过第三方组织的采购和集中采购。
2.1 自行采购自行采购是指受援方使用全球基金“年度资助计划”的资金自主完成的采购。受援方可以基于自身现有的采购和供应管理系统、规则、程序进行采购。
但开展自行采购的受援方仍需遵循全球基金制定的流程和标准,遴选供应商和产品,并接受全球基金对采购的审查和监督。首先,受援方对供应商的选择必须基于全球基金规定的职权范围,且只有在获得全球基金的批准后,才能与供应商签订采购合同。其次,受援方自行采购的产品以及产品的生产场所需要符合全球基金的相关要求[5],且产品的采购价格不得超过全球基金规定的“通过集中采购实现的最高价格”。第三,开展自行采购的受援方需向全球基金的审查小组提交采购清单、供应链管理安排方案以及产品样本等材料,接受全球基金对采购程序和产品质量的检查。最后,采购流程正式开始后,受援方需建立采购长期监管机制并定期向全球基金汇报采购进展。
2.2 通过第三方组织的采购当受援方采购能力和供应链管理能力不足时,可选择通过第三方组织的采购或集中采购。通过第三方组织的采购指的是受援方选择符合全球基金要求的第三方组织机构,使用“年度资助计划”资金完成的采购。
符合全球基金要求的第三方组织包括:(1)与遏制结核病伙伴关系组织(The Stop TB Partnership)下设全球抗结核药品管理中心(The Global Drug Facility)以及全球基金官方合作的采购服务代理商;(2)联合国部门或专门机构;(3)IDA基金(The International Dispensary Association Foundation)、供应链管理伙伴关系组织(The Partnership for Supply Chain Management);(4)疟疾预防联盟(The Alliance for Malaria Prevention);(5)其他符合全球基金规定的组织。[6]
除已列出的组织之外,受援方如果希望通过其他第三方组织进行采购,则必须向全球基金提供必要理由说明,并根据全球基金要求提供审核文件。所有开展采购的第三方组织还需要在全球基金的赠款实体数据库(Grant Entity Data)中完成注册。[7]
2.3 集中采购集中采购指的是受援方向全球基金提出采购需求,由全球基金采购管理部门及其合作采购服务代理商完成的采购。用于集中采购的资金独立于“年度资助计划”。受援方的“年度资助计划”资金和用于集中采购的资金总额不得超过受援方所获全球基金赠款的总额度。
在集中采购中,受援方首先需要在全球基金当前的赠款周期内注册成为集中采购的接受方,然后在全球基金在线采购平台——万博(Wambo)平台上提出集中采购申请。全球基金采购交易管理小组负责审查集中采购申请。集中采购申请获批后,全球基金将估算申请所包含的费用,并将估算报价单同时提交给全球基金内部审查机构和采购申请方进行审核与确认。报价单获批后,全球基金会在万博平台上发布集中采购信息,鼓励供应商投标并开展自由竞标。全球基金的采购服务代理商负责同产品供应商和物流供应商进行信息沟通、对采购过程进行监督、确保产品质量符合全球基金的要求。
采购中标后,全球基金将从受援方的可用赠款资金中锁定用于此次采购的资金直至采购完成,以确保相应赠款仅用于当前采购。申请采购的受援方验收产品后,由全球基金支付集中采购的货款并向申请采购的受援方发送赠款资金对账单。对账单经受援方确认无异议后,集中采购流程全部完成。
3 全球基金全球采购的产品质量标准全球基金将其采购的各类医药产品分为“药物”“体外诊断用品、个人防护装备和医疗器械”以及“病媒控制产品”三个类别,分别制定质量控制政策(表 1)。[8-10]在同类型产品的质量控制政策中,针对不同用途或性质的产品质量标准并不完全相同。例如,“抗逆转录病毒药物、抗疟疾药物和抗结核病药物(以下简称“三抗药物”)”的产品质量标准为:产品通过世界卫生组织(World Health Organization, WHO)资格预审;或产品被严格监管机构(Stringent Regulatory Authority)批准使用;或产品被WHO列名机构(WHO-Listed Authority,WLA)批准使用;或产品被专家评审小组推荐使用。对非三抗药物的其他药物产品的质量标准为:产品必须满足药物使用国家的监管机构制定的相关质量标准。
| 表 1 全球基金采购产品相关质量标准 |
虽然针对不同产品的具体标准各异,但综合来看,下述5项标准几乎同全球基金采购的所有产品相关:(1)产品通过WHO资格预审;(2)产品通过WLA认证;(3)产品通过严格监管机构认证;(4)产品被专家评审小组推荐使用;(5)产品通过全球协调工作组(The Global Harmonization Task Force)创始成员国之一的监管机构认证。本节将针对上述质量标准,逐条简述其所适用范畴、评估开展和认证的具体流程。
3.1 WHO资格预审除了“避孕套”以及“非三抗药物的其他药物产品”,其他产品的质量标准中均涉及“产品通过WHO资格预审”。WHO针对不同产品建立预审小组,制定评判标准,并组织开展产品资格预审。各类产品资格预审小组的具体人员组成各不相同,但当前小组成员的国籍组成均以美国、欧洲国家、非洲国家为主。[11]
以WHO药物资格预审为例。资格预审的流程包括四个阶段:确定药物参审资质和提交预审资料、产品档案初筛、产品质量与生产场所的评估以及资格预审最终判定。[12]
生产商参与WHO资格预审的“第一道门槛”是其生产的原料药或制剂需要在《WHO资格预审评估邀请清单》中。该清单以WHO基本药物目录和WHO治疗指南为基础制定,并纳入WHO专家评审委员会申请加入清单的制剂和原料药。截至目前,这一清单已经涵盖了用于治疗艾滋病、结核病、疟疾、被忽视的热带病、腹泻、流感、新型冠状病毒感染和用于生殖健康的制剂,以及用于生产上述制剂的原料药。[13]
确定制剂或者原料药在清单中后,药物生产商应根据预审方式向WHO提交相应的资料。预审方式包括全面评审和简化评审。全面评审主要针对以往未经WHO或严格监管机构评估的制剂和原料药。接受全面评审的药物生产商需要提交的材料包括:预审意向书、产品档案、产品样品、产品生产场所相关文件、产品档案中临床研究机构出具的相关文件等。简化评审针对已经通过严格监管机构评估的制剂和原料药,以及在制剂的全面评审过程中原料药主文件已经通过WHO审查的原料药。简化评审要求药物生产商提交下述材料:严格监管机构出具的产品质量评估报告、生产场所检查报告和符合WHO标准的产品证书原件或副本等。[14]
收到药物生产商提交的文件后,WHO首先会针对产品档案的完整性开展筛选,并告知申请人初筛结果。针对通过筛选的产品档案,WHO将根据相应规范指定专家或者评估员进行评估,且优先选择药物生产国家的国家药品监管机构成员开展评估。最后,WHO将安排检查小组对药物生产场所进行实地检查,以检验药物生产场所是否满足WHO制定的“良好生产规范”要求。[15]顺利通过上述审查后,在该生产场所生产的产品将通过资格预审。
“病媒控制产品”与“药物”的资格预审的流程相似。但WHO未针对病媒控制产品设立《WHO资格预审评估邀请清单》,即任何用于病媒控制的产品都能参加WHO的资格预审。[16]“病媒控制产品”的资格预审方式分为“资格预审途径”和“新干预途径+资格预审途径”。其中“资格预审途径”适用于现有WHO政策建议支持的产品,“新干预途径+资格预审途径”适用于不被现有WHO政策建议支持的产品。产品能否得到现有WHO政策建议的支持则由WHO下设提交前协调委员会(Pre-submission Coordination Committee)进行判断。当产品被判定适用“新干预途径+资格预审途径”,那么产品除需要通过“资格预审途径”外,还需要被确定具有公共卫生价值,才能最终通过资格预审。
“体外诊断用品、个人防护装备和医疗器械”的资格预审流程也大致相同。主要区别在于对于多数该类产品,WHO要求产品的生产场所需满足相应的国际标准化组织标准(即ISO标准),而非良好生产规范。
WHO资格预审名单数据显示,截至2024年9月30日,中国通过WHO资格预审的原料药、制剂、体外诊断用品和病媒控制产品的品种数分别为59种、52种、13种和7种,分别占通过WHO资格预审的对应产品品种数的32.96%、7.83%、11.50%和7.69%。
3.2 严格监管机构和WLA认证“药物被严格监管机构批准使用”是全球基金采购“三抗药物”的质量要求之一。“严格监管机构”的概念最初由WHO和全球基金共同提出。严格监管机构包括:(1) 人用药品技术要求国际协调理事会(International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use, ICH)成员;(2) ICH观察员,包括以瑞士药监局为代表的欧洲自由贸易联盟、加拿大卫生部等;(3) ICH互认协议机构,包括澳大利亚、挪威、冰岛和列支敦士登的国家监管机构。2017年,中国国家药品监督管理局加入ICH。但自2015年10月23日至今,全球基金和WHO仍未对“严格监管机构”的名单进行官方发布更新。目前,在严格监管机构名单中,除日本厚生劳动省以外,其余均为欧美国家的监管机构。中国国家药品监督管理局目前仍未被认可属严格监管机构之列。
随着WHO对医药产品质量监管的参与度增加,“严格监管机构”概念逐步被“WLA”所取代。WLA指的是符合WHO规定的所有相关指标和要求的监管机构或区域监管系统。“被WLA批准使用”是全球基金采购的“三抗药物”和“体外诊断用品、个人防护装备和医疗器械”的质量标准之一。在2024年5月公示的最新WLA名单中包括来自韩国、新加坡、美国和31个欧洲国家的相关监管机构。[17]
目前,中国国家药品监督管理局属于“过渡性WLA”中的“疫苗生产国的国家监管机构”。[18]“过渡性WLA”中的监管机构可以通过向WHO提出申请意向、提交自我评估报告、接受并通过WHO所组织的一系列绩效评估流程后,正式成为WLA。WHO的WLA绩效评估流程主要由其召集的WLA技术咨询小组以及WHO主管“获取药品和卫生产品”事务的助理总干事开展评估和商定。现有WLA技术咨询小组由来自WHO的6个区域的14名专家组成,其中包括一位中国专家。[19]
3.3 专家评审小组推荐使用“产品被专家评审小组推荐使用”是全球基金采购的“三抗药物”和“体外诊断用品、个人防护装备和医疗器械”中的“体外诊断用品”“医疗器械”以及“避孕套”的质量标准之一。专家评审小组是一个由WHO设立、外部技术专家组成的独立技术机构。现有专家评审小组包括药物专家评审小组和体外诊断用品专家评审小组。不同于WHO资格预审,专家评审小组主要服务于采购部门或资助机构。采购方在开展采购的过程中可要求专家评审小组对其采购的产品进行风险等级评估,从而为采购决策提供参考。专家评审小组不会直接与其评估产品的生产商联系,而是由产品采购方负责转接。[20]
相较于其他质量标准,“专家评审小组推荐使用”的效力有限。具体而言,当存在两种或者两种以上的产品符合除“专家评审小组推荐使用”以外的其他质量标准之一时,采购方不能选择仅满足“专家评审小组推荐使用”的产品。换言之,只有在采购方确定只有一种或没有产品符合其他质量标准,但仍希望继续采购同类产品时,才可以采购仅满足“专家评审小组推荐使用”的产品。
从审核认证流程来看,产品和产品生产商需要满足一定的条件才能参加专家评审小组的审核。“药物”参与专家评审小组审核的条件为:药物生产场所必须经由WHO、严格监管机构、WLA或国际药品检查合作计划成员等组织机构检查,并被认为符合对应药物的良好生产规范。药物生产商已向WHO提交产品资格预审申请,并已接受WHO审查;或者已向严格监管机构或WLA提交了销售许可申请,且严格监管机构或WLA已接受申请并进行审查。[10]“体外诊断用品”参与专家评审小组审核的条件为:产品正在接受,或生产商承诺参与WHO资格预审或全球协调工作组创始成员国之一的监管机构的审查。此外,产品生产场所需要符合ISO 13485(2016)或ISO 9000系列或其他同等质量体系等标准。[21]满足条件的产品生产商可将产品档案随审核意向书一同提交给产品采购方,由采购方提交至专家评审小组。专家评审小组将依据评估程序,对产品注册信息、产品生产场所质量控制信息、产品标签信息、产品稳定性测试数据等进行审查,并公示评审结果。[22-23]
3.4 全球协调工作组创始成员国的监管机构认证全球协调工作组是设立在英国的非官方性组织,最早由来自美国、欧盟、日本、加拿大和澳大利亚的监管机构和行业协会发起成立。通过全球协调工作组创始成员国的监管机构认证,是全球基金采购中“体外诊断用品、个人防护装备和医疗器械”的质量标准之一。例如,针对医疗器械和体外诊断用品生产企业,质量要求包括产品生产企业需符合全球协调工作组创始成员国的监管机构认同的质量管理体系。针对基于全球协调工作组分类规则[24]进行分类的C类和D类医疗器械(不包括体外诊断用品),质量标准包括产品被全球协调工作组创始成员国的监管机构批准使用。
4 全球基金采购概况2013—2022年,全球基金及其受援方共采购6类产品,采购总额为130.31亿美元。采购额前三的产品为“抗逆转录和抗新冠病毒药物”“病媒控制产品”“体外诊断用品、个人防护装备和医疗器械”。这3类产品各年度采购额总和占各年度全球基金采购总额的80%以上(图 1)。其中,采购总额最高的是“抗逆转录和抗新冠病毒药物”,其历年采购总额达到58.02亿美元,且该类别产品各年度采购额占同年度全球基金采购总额的比例均在40%以上(2020和2022年除外)。

|
注:在全球基金采购价格与质量报告数据库中,“避孕套”独立于“体外诊断用品、个人防护装备和医疗器械”进行统计。 图 1 全球基金各年度采购总额及各类别产品采购额 |
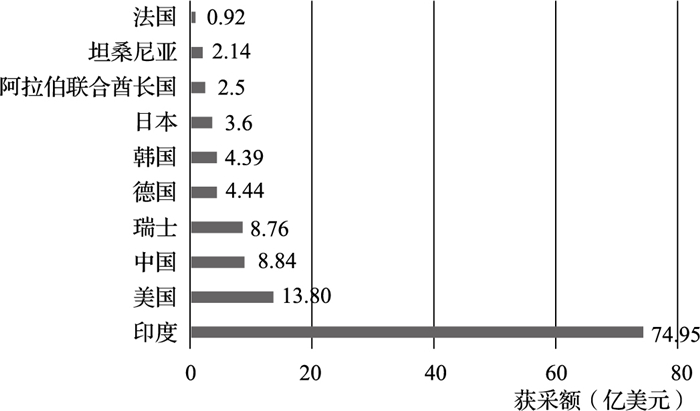
2013—2022年,共有54个国家和地区的384家产品供应商参与全球基金及其受援方的采购。印度是全球基金采购最主要的供应国家。2013—2022年间,全球基金及其受援方共向印度供应商采购总额达到74.95亿美元的产品,占全球基金及其受援方采购总额的57.52%(图 2)。
|
图 2 2013—2022年全球基金获采额前10的国家 |
在全球基金及其受援方采购的6类产品中,印度都是获采额前3的供应国之一。尤其是“抗逆转录和抗新冠病毒药物”类别,印度供应商获采总额约为55.1亿美元,占该类产品总采购额的94.97%。目前,中国在“抗疟疾药物”“避孕套”以及“病媒控制产品”3类产品的获采额占比中位列前3(表 2)。
| 表 2 2013—2022年全球基金采购各类型产品主要供应国家 |
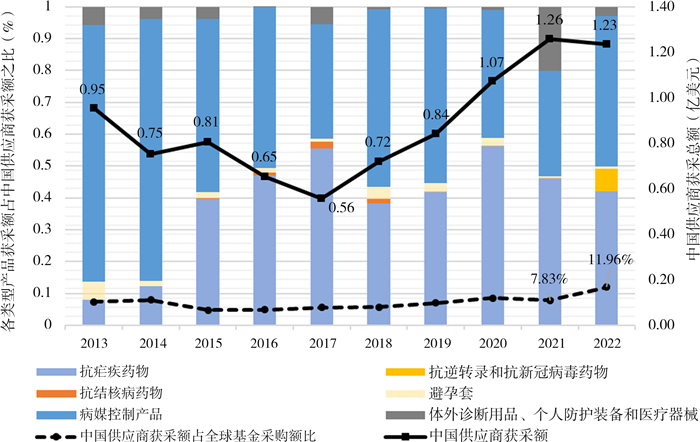
中国供应商的获采总额占全球基金及其受援方采购总额的比例总体呈现增长趋势。中国供应商的获采总额自2013年的0.95亿美元增长至2022年的1.23亿美元。尤其自2017年起,中国供应商获采总额保持每年0.12亿美元到0.23亿美元的增长,在2021年达到1.26亿美元(图 3)。
|
图 3 全球基金采购中国供应商各年度获采额及各类型产品获采额及其占比 |
“病媒控制产品”和“抗疟疾药物”一直是中国供应商主要获采产品,其历年获采总额占中国获采总额之比达到52.48%和38.77%。此外,“病媒控制产品”获采额占比呈下降趋势,“抗疟疾药物”则呈现增长趋势。
2013—2022年,共有60家中国企业向全球基金及其受援方供应产品。其中有30家供应“体外诊断用品、个人防护装备和医疗器械”,18家供应“避孕套”,供应“抗疟疾药物”和“抗逆转录和抗新冠病毒药物”的均只有1家。
在全球基金采购中,获采额最多的中国供应商是供应“长效杀虫蚊帐”的天津永阔科技集团有限公司和主要供应抗疟疾药物“青蒿琥酯”的桂林南药股份有限公司。2013—2022年期间,两者的获采总额分别达到4.14亿美元以及3.43亿美元,占中国供应商获采总额的46.83%和38.77%(表 3)。
| 表 3 2013—2022年全球基金采购主要中国供应商及其获采额 |
总体上看,中国对全球基金全球采购的参与度有所升高。但相比于印度,中国企业的获采额较低、优势产品类型较少。本文通过对全球基金采购方式及其采购产品的质量要求分析,认为主要原因有二:一是中国企业对医药产品的国际质量标准的认证参与有限;二是中国在现有医药产品国际质量标准体系的制定机制中参与有限。
6.1 中国企业优劣势产品类别及获采额的变化趋势分析在获采额及其占比方面,自2017年以来,中国企业的获采额占全球基金采购额比呈现逐年增长趋势。这与近年来中国政府越发重视参与全球卫生治理有关。例如,中国国家药品监督管理局在2017年正式加入ICH,在2021年正式启动“国际药品检查合作计划预加入申请计划”。这些举措均有助于提升中国医药产品的国际知名度和竞争力,树立国际品牌形象。
在获采的产品类别方面,与疟疾有关的“抗疟疾药物”和“病媒控制产品”是中国企业主要的获采产品。一方面是因为2010—2020年,是中国抗击疟疾的最终阶段——“消除疟疾”阶段。在该阶段,中国国内的疟疾患者极少,国内抗疟疾产品的供应远大于需求,产品的主要销售途径是国际市场;另一方面则是因为我国拥有80%以上的青蒿素资源,国内企业生产的抗疟疾药物在成本方面具有一定的优势,具有很强的国际竞争力。[25]“抗逆转录和抗新冠病毒药物”是中国主要的“劣势产品”。这可能是因为目前中国企业生产的抗逆转录病毒药物以仿制药为主,缺少新类型的抗逆转录病毒治疗药物单剂及固定复方制剂。[26]此外,多数中国企业因该类产品未通过国际标准认证,也无法参与全球采购。[27]
6.2 中国企业对医药产品的国际质量标准的认证参与有限通过WHO资格预审、WLA认证或严格监管机构认证等国际公认的医药产品质量认证是产品获得全球基金采购的前提。除了全球基金,这些国际质量标准也是诸多国际组织开展采购的主要依据。[28]
但目前,通过国际标准认证的中国企业产品数量仍然很少。以WHO资格预审为例,其原因可能是鲜少有企业了解WHO资格预审的规则和流程;企业申请WHO资格预审还面临着较高的前期费用,且产品通过WHO资格预审后的收益无法得到保障。[29]此外,参与国际多边组织全球采购以及WHO资格预审的中国专家数量也一直较少。这也可能导致中国医药企业在参与国际多边组织全球采购和参与WHO资格预审时缺乏引导和可咨询的对象。
6.3 中国在现有医药产品国际质量标准体系的制定机制中参与有限在全球基金的采购中,严格监管机构、全球协调工作组创始成员国的监管机构以及WLA的产品认证实际上等同于WHO的资格预审。但目前中国尚无监管机构属于以上三类监管机构。综合以上机构的成员组成数据,上述认证机构从建立之初至今都以欧美国家的机构为主导。这一情况可能使得中国医药企业在寻求产品质量认证时,相比别国企业会面临更多阻碍。
另一方面,目前应用较广泛的国际标准过去一直以欧美国家的质量标准为参考制定,这些标准同对应的中国产品标准存在差别,也会导致中国医药产品更不易通过国际标准的认证。例如,目前WHO药物资格预审参考的基本文件是《国际药典》。《国际药典》由WHO的药物制剂规格专家委员会编撰和修订,其修订的主要依据就是美国及部分欧洲国家的药典。[30]
6.4 关于中国进一步融入全球采购市场的政策建议本研究建议中国医药企业和相关政府部门继续共同发力促进中国未来进一步融入全球医药产品采购市场。
中国的医药企业应当关注、重视并积极参与全球采购,把握国家发展和改革委员会、国家药品监督管理局等部门发布的《“十四五”医药工业发展规划》和《“十四五”国家药品安全及促进高质量发展规划》等政策带来的机遇,进一步加入全球医药产品市场。企业还应严抓产品质量,早日同国际质量标准“接轨”,积极促进产品通过国际公认的产品质量标准认证。通过上述国际标准认证,也能使中国企业及其产品获得更多参与双边和多边全球贸易的机会。
针对中国有关政府部门,一方面可以增强对采购专业官员的培养,增强采购专员对相关企业的指导和联系,搭建企业同更多有需求的国际组织间的对话平台等举措,为促进医药企业进一步加入全球采购建立支持性环境,并提升国内医药企业对国际多边组织全球采购的关注度。另一方面,还应当继续增强国内药品监督管理机构专业能力,早日推进医药产品的中国标准到国际标准的转化并参与到国际标准的制定中。
作者贡献:胡孝龙负责定量与定性资料收集与分析以及论文撰写;方晢伊负责论文设计、资料收集、论文审稿与修改;黄葭燕负责理论指导、论文设计、论文审稿与修改。
作者声明本文无实际或潜在的利益冲突。
| [1] |
Analyzing the sourcing literature: Over two decades of research[J]. Journal of Purchasing and Supply Management, 2019, 25(5): 100521.
|
| [2] |
发展改革委. 关于印发《"十四五"生物经济发展规划》的通知(发改高技〔2021〕1850号)[EB/OL]. (2021-12-20)[2024-07-31]. https://www.gov.cn/zhengce/zhengceku/2022-05/10/content_5689556.htm
|
| [3] |
The Global Fund. Price & Quality Reporting Price Reference Report[EB/OL]. [2024-07-31]. https://insights.theglobalfund.org/t/Public/views/PriceQualityReportingPriceReferenceReport/Countries?iframeSizedToWindow=true&%3Aembed=y&%3AshowAppBanner=false&%3Adisplay_count=no&%3AshowVizHome=no
|
| [4] |
冯浩然, 梁笛, 黄葭燕. 抗艾滋病、结核病和疟疾全球基金与主要捐赠国的合作及其对中国的启示[J]. 中国卫生政策研究, 2022, 15(9): 73-80. DOI:10.3969/j.issn.1674-2982.2022.09.011 |
| [5] |
The Global Fund. Guide to Global Fund Policies on Procurement and Supply Management of Health Products[EB/OL]. [2024-06-20]. https://www.theglobalfund.org/media/5873/psm_procurementsupplymanagement_guidelines_en.pdf
|
| [6] |
The Global Fund. Guidelines for Grant Budgeting[EB/OL]. [2024-06-23]. https://www.theglobalfund.org/media/3261/core_budgetinginglobalfundgrants_guideline_en.pdf
|
| [7] |
The Global Fund. Operational Policy Manual[EB/OL]. [2024-06-09]. https://www.theglobalfund.org/media/3266/core_operationalpolicy_manual_en.pdf
|
| [8] |
The Global Fund. Quality Assurance Policy for Vector Control Products and Related Equipment[EB/OL]. [2024-08-04]. https://www.theglobalfund.org/media/13767/psm_qa-vector-control-products-equipment_policy_en.pdf
|
| [9] |
The Global Fund. Quality Assurance Policy for Medical Devices (including InVitro Diagnostics) and Core Personal Protective Equipment[EB/OL]. [2024-08-24]. https://www.theglobalfund.org/media/13577/psm_qa-medical-devices_policy_en.pdf
|
| [10] |
The Global Fund. Quality Assurance Policy for Pharmaceutical Products[EB/OL]. [2024-08-04]. https://www.theglobalfund.org/media/5894/psm_qapharm_policy_en.pdf
|
| [11] |
World Health Organization. Department of Regulation and Prequalification 2023 annual report[EB/OL]. [2024-08-03]. https://www.who.int/publications/m/item/department-of-regulation-and-prequalification-2023-annual-report
|
| [12] |
World Health Organization. WHO Expert Committee on Specifications for Pharmaceutical Preparations[EB/OL]. [2024-08-23]. https://iris.who.int/bitstream/handle/10665/340323/9789240020900-eng.pdf?sequence=1
|
| [13] |
World Health Organization. 34th Invitation to manufacturers of Active Pharmaceutical Ingredients (API) to submit an Expression of Interest (EOI) for API evaluation to the WHO Prequalification Unit (PQT)[EB/OL]. [2024-08-24]. https://extranet.who.int/prequal/sites/default/files/document_files/34rd-invitation-for-api-eoi-v1.0.pdf
|
| [14] |
World Health Organization. Guidelines on submission of documentation for prequalification of finished pharmaceutical products approved by stringent regulatory authorities[EB/OL]. [2024-09-05]. https://gxp-academy.org/upload/iblock/4d6/4d60594fd319202b4d3e2ab825702c72.pdf
|
| [15] |
World Health Organization. WHO good manufacturing practices for pharmaceutical products: main principles[EB/OL]. [2024-08-24]. https://www.who.int/publications/m/item/trs986-annex2
|
| [16] |
World Health Organization. Overview of the WHO Prequalification Assessment of Vector Control Products[EB/OL]. [2024-08-24]. https://extranet.who.int/prequal/sites/default/files/document_files/WHO_PQT_VectorControlProducts_June2021.pdf
|
| [17] |
World Health Organization. List of WHO Listed Authorities WLAs[EB/OL]. [2024-08-03]. https://www.who.int/publications/m/item/list-of-who-listed-authorities-wlas
|
| [18] |
World Health Organization. List of transitional WLAs[EB/OL]. [2024-08-17]. https://www.who.int/publications/m/item/list-of-transitional-wlas
|
| [19] |
World Health Organization. Technical Advisory Group on WHO Listed Authorities (TAG-WLA)[EB/OL]. [2024-08-04]. https://www.who.int/groups/technical-advisory-group-on-who-listed-authorities-(tag-wla)
|
| [20] |
World Health Organization. The Expert Review Panel (ERP)[EB/OL]. [2024-08-25]. https://extranet.who.int/prequal/sites/default/files/document_files/73_ERP_Feb2019_new%20templ.pdf
|
| [21] |
The Global Fund. Expert Review Panel for Diagnostics Terms of Reference[EB/OL]. [2024-08-25]. https://www.theglobalfund.org/media/5844/psm_erpd_tor_en.pdf
|
| [22] |
The Global Fund. Timeline of the Expert Review Panel Process for Diagnostic Products (ERPD)[EB/OL]. [2024-08-24]. https://www.theglobalfund.org/media/8997/psm_2017-03-erpprocessfordiagnostics_timeline_en.pdf
|
| [23] |
The Global Fund. Timeline of the Expert Review Panel Process for Pharmaceutical Products[EB/OL]. [2024-08-24]. https://www.theglobalfund.org/media/5587/psm_2017-02-selectedmedicinesmanufacturersexpressionofinterest_timeline_en.pdf
|
| [24] |
The Global Harmonization Task Force. Principles of Medical Devices Classification[EB/OL]. [2024-08-01]. https://www.imdrf.org/sites/default/files/docs/ghtf/final/sg1/technical-docs/ghtf-sg1-n77-2012-principles-medical-devices-classification-121102.pdf
|
| [25] |
黄旸木, 许铭. 中国抗疟产品的可持续发展路径[J]. 中国血吸虫病防治杂志, 2022, 34(2): 120-121, 140. |
| [26] |
马春涛, 霍秀敏, 王强. 我国艾滋病抗病毒治疗药品注册情况分析[J]. 中国艾滋病性病, 2020, 26(9): 941-944, 953. |
| [27] |
马奇三, 王正平, 李金亮, 等. 抗艾滋病药物的现状与挑战[J]. 聊城大学学报(自然科学版), 2020, 33(1): 70-78. |
| [28] |
LEOW A, HU J, HIRD T. An overview of WHO Prequali-fication[EB/OL]. [2024-08-04]. https://rethinkpriorities.org/wp-content/uploads/2023/07/WHO-PQ.pdf
|
| [29] |
HUANG Y, PAN K, PENG D, et al. A qualitative assessment of the challenges of WHO prequalification for anti-malarial drugs in China[J]. Malaria Journal, 2018, 17(1): 149. DOI:10.1186/s12936-018-2303-8 |
| [30] |
World Health Organization. The Eleventh Edition of The International Pharmacopoeia[EB/OL]. [2024-08-03]. https://digicollections.net/phint/2022/index.html#p/home
|
(编辑 薛云)





