卫生技术评估(Health Technology Assessment, HTA)最早诞生于20世纪70年代的美国,是卫生政策和卫生管理决策系统的重要辅助工具和方法。[1]根据世界卫生组织[2]在2015年发布的关于全球处于不同地区、不同经济发展水平国家(有125个成员国参加)的HTA现状的全面评估报告,超过半数的国家已将HTA及其结果引入到对卫生技术的准入、管理、监测等一系列决策过程中。HTA通过决策转化应用于卫生政策制定,已经在优化全球卫生配置上发挥了巨大的作用。[3-5]
而在我国,HTA领域发展相对滞后,尤其是在进一步利用HTA结果以实现更好的决策转化方面。面对当前我国卫生体系医疗费用的不合理快速增长以及有限医疗资源分配、利用不合理的问题,国家对循证决策提出了更高的要求,未来在医疗技术准入、医保报销、药品定价等诸多方面,HTA结果将越来越多的作为决策依据完成其决策转化,从而辅助循证决策。同是社会医疗保险为主的国家, 德国在HTA应用和决策转化方面保持持续创新地探索,尤其在实现HTA服务于决策转化过程中,德国有效地发挥了政府层面宏观监督指导和社会层面的具体细则实施的作用,通过利用HTA这一科学决策工具选择高效的、必要的、富有成本收益的医疗服务进入社会医疗保险报销系统,在有力控制了医疗费用增长的同时为患者提供了更加优质的健康服务。
1 德国HTA情况概述 1.1 德国HTA组织机构的发展及特点 1.1.1 HTA的发展20世纪90年代以来,伴随着循证医学运动(Evidence-based Medicine Movement)在德国的发起,HTA和卫生经济学等也引起了广泛的讨论。同时,受驱于紧张的卫生医疗费用预算,外加联邦卫生部对将HTA运用于医保报销决策的浓厚兴趣,越来越来多的利益相关者达成广泛共识,即通过对现有卫生技术进行评估后进行准入决策以控制费用增长,并同时确保提供更加质优高效服务。随后,来自疾病基金协会、医师协会、医学科研高校、学术研究组织等的学术工作小组作为中坚力量,开始致力于开展各种HTA项目研究,或是为各协会的相关疾病报销、内部决策等提供决策支持,或是从科研学术的角度致力于HTA方法、应用、培训等方面的研究和工作。1997—2002年,成立于汉诺威医学院(Hannover Medical School)下的卫生保健技术评估科学工作组,在联邦政府的资助下进行了一系列多达50项的HTA项目,为德国HTA数据库的建立以及HTA相关方法的后续改进奠定了良好的基础。[6]
在2000年德国卫生体系改革浪潮的推进下,德国卫生技术评估局(DAHTA, 隶属于德国医学文献与情报学会, DIMDI)正式成立,被要求对联邦资助的HTA项目进行系统管理,并通过组建一个信息化数据库囊括相关HTA项目成果用于支持国家卫生决策。2004年,伴随着法定医疗保险现代化法(the Statutory Health Insurance Modernization Act)出台,由众多利益相关方组成的卫生自我管理体系中的最高决策机构——联邦联合委员会(G-BA)正式诞生;该委员会由德国自我管理卫生系统中的四大主导组织构成:联邦医保基金协会(GKV-Spitzenverband)、德国医院联盟(DKG)、国家法定健康保险医师协会(KBV)和国家法定健康保险牙医协会(KZBV)。[7]G-BA被赋予组织或委托开展HTA项目的职责:在联邦卫生部的监督下G-BA可通过基于HTA的循证决策过程发布具有法律约束力的标准、指令等,对药品、诊断、治疗过程、医疗器械和非医学治疗的提供和报销做出相关规定。随后,G-BA依据一项新法案(GKV)建立了一个独立的HTA机构——卫生保健质量与疗效研究院(IQWiG)。而IQWiG的主要职责就是进行HTA评估为G-BA决策提供参考,开展的HTA评估包括药品的收益和成本效益评估、非药品医疗技术的干预项目评估(比如医疗设备、诊断治疗方法、疾病预防筛查等)。至此,德国基于三大HTA组织机构的国家层面HTA决策转化体系正式组成。
1.1.2 HTA组织机构的特点德国卫生体系强调各方自我管理,在政府对相关的机构职能、财政预算等宏观层面的体系框架进行规划设计后,具体运行方案由医疗服务体系中的各方代表谈判确定,主要依靠行业力量进行自我管理以及服务购买者、使用者之间的制约。[8]审视德国HTA以及HTA决策转化机制的成长发展过程,政府支持和监督、从法律层面确保HTA决策转化成果落实到位以及基于国家层面HTA机构的各行业协会、相关院所、组织、患者群体等利益相关方都可参与决策的严谨决策转化流程缺一不可。从最开始的循证医学运动统一认识,到之后的各种背景下的学术科研工作小组不断探索HTA方法、管理流程和决策转化机制,再到最后形成以德国自我管理体系中的最高决策机构为中心的三大HTA管理机构,并通过立法确定其基于HTA的决策转化成果的严格落实;形成了能适用于不同层级、不同组织,并针对各种不同技术类型的HTA评估方法及决策转化机制。
1.2 德国HTA决策转化管理流程 1.2.1 HTA决策转化管理相关法规指令德国在立法以及国家政策高度上确定了HTA决策转化的顺畅运行。首先G-BA由2004年法定医疗保险现代化法出台成立,其基于HTA进行循证决策的权力由德国社会法第五册(SGB Ⅴ)赋予(联邦卫生部负责监督)。[9]而主要实施HTA评估的机构IQWiG同样是由G-BA在2004年依据新法案(GKV)建立,并且其开展HTA评估辅助G-BA决策的职责在SGB Ⅴ中进行了明文规定。在建立国家层面的HTA机构之上,德国持续探索完善HTA决策转化机制,2010年11月11日,德国议会通过了市场对医药产品的改革法案(AMNOG),这项法案新赋予了G-BA和IQWiG一项重要的职责:对新获批准上市的药品进行额外效益评估,以辅助社会医疗保险机构对新药的定价和报销方面的政策制定。DAHTA也是德国医改的产物,虽然在实际决策制定中的直接作用弱于其他两大机构,但其建立的HTA数据库对决策转化证据支持也起到了积极作用。
1.2.2 HTA决策转化的相关方目前,在德国的HTA管理体系中,主要形成了G-BA、IQWiG、DIMDI这三个国家层面的HTA组织机构,分别实现决策转化整体性管理、评估科学化管理以及HTA的信息平台化管理等;各机构各有功能定位,又通过信息共享来共同实现全国HTA的完善系统管理。G-BA是德国HTA决策转化体系中的主导管理者,负责基于包括HTA评估结果等证据做出卫生决策。最终决策转化的HTA项目可在G-BA内部开展,大部分委托IQWiG、高等院校研究机构等独立第三方评估机构进行,同时也参考DIMDI的HTA信息库信息。
德国参与HTA决策转化管理的相关方除了组成G-BA四大支柱组织:联邦医保基金协会、德国医院联盟、国家法定健康保险医师协会和国家法定健康保险牙医协会之外,根据社会法和患者参与法案(the Patient Involvement Act)的相关规定,特殊的患者代表或是维护患者权益的组织代表也有权参与G-BA决策流程(但无表决权)。其他利益相关方,如患者家属、医药企业、医药企业协会等也有途径参与决策过程。还有具体决策的关键方:德国卫生体系最终决策主体是G-BA决策委员会(Plenum)以及其下的九个子委员会(subcommittees)。
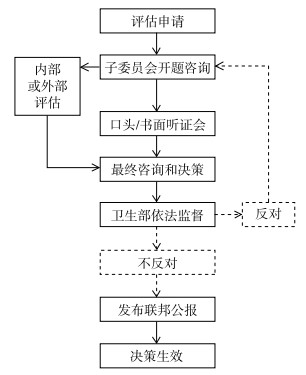
1.2.3 HTA决策转化具体管理流程在进行具体的HTA决策转化管理时,主要包括五个阶段:评估申请——开题咨询——外部科学评估——听证会——决议及指令发布(图 1)。首先,由G-BA决策委员会内部成员,或患者代表、社会医疗保险医疗服务提供者和基金资助者,以及一些特殊医药技术供应商等都可以提出HTA评估申请。之后,G-BA从提交的申请中选定正式开展评估的项目,并进一步确定具体评估问题,然后根据受众的不同、判定标准的差异,任命子委员会负责相关证据收集以及管理独立的HTA评估工作。然后,根据具体评估需求,决策委员会一般委托IQWiG等HTA评估机构进行外部评估。之后由G-BA根据HTA初步结果确定是否需要举行听证会,尤其是涉及到第三方利益时,一般书面和口头两种方式的听证会都要举行。最后,根据HTA评估结果以及听证会结果,由子委员会汇总所有商议结果并做出初步决策意见呈交决策委员会,决策委员会再据此做出最终决策并撰写详细国家指令上交给卫生部并公布在G-BA官网供公众审阅。最终,如果卫生部在两个月内没有提出异议,该指令将被发布到联邦公报上,并且一般在发布后第二天,相应指令规定即在全国生效实施。
|
图 1 G-BA主导的HTA决策转化过程 |
德国从法律层面确保HTA决策转化,最新关于药品准入的法规是2010年11月德国议会通过的市场对医药产品的改革法案(AMNOG),G-BA和IQWiG开始致力于对新药的额外效益评估(以下简称AMNOG评估),即对新获批准上市的药品进行额外效益评估,用于新药定价和医保报销等方面的药品医保准入政策制定。
2.1.2 药品准入HTA决策转化具体过程2010年之后,G-BA和IQWiG开展的AMNOG评估就已经成为医保对具有新的活性成分体系药品的医保内定价参考基础。AMNOG评估将新药的额外效益结果划分为六类:重大(持续重大的改善,如可治愈,存活时间大量延长,长时间免于严重的病症,严重副作用影响极大减缓)、可观(有显著的改善,如明显病情减缓,存活时间适当延长,严重病症的缓解,严重副作用影响减缓或其他副作用明显减缓)、少量(适当的高于边际收益的改善,如严重病症的减缓,副作用减少)、边际(无额外效益)和低于已准入参照药品。
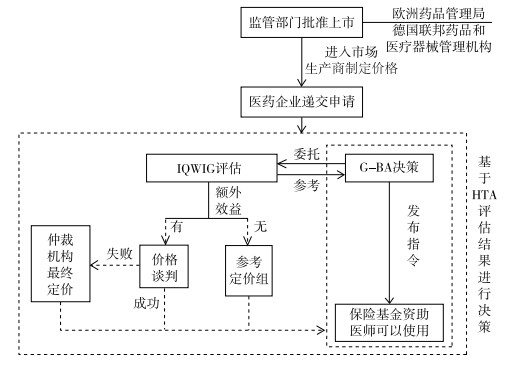
具体决策流程及HTA在相应环节的作用如图 2。在新药获批上市三个月内,医药公司上交医保准入申请和药品相关信息,G-BA委托IQWiG等第三方HTA机构完成AMNOG评估。评估初步结果将在网上公示,医药公司、协会和专家等利益相关方都可据此提交书面或口头意见。接下来的三个月内,G-BA将基于HTA评估结果、各利益相关方意见以及其他证据做出该药品医保准入的最终决策。决策详细内容包括额外效益的程度、适宜接受新药治疗的患者群、质量保证的行政要求以及治疗成本说明等,如果新药品具有额外效益,这些都将作为新药医保定价谈判的基础证据。接下来医药公司与联邦医保支付基金协会将据此谈判确定新药报销支付价格的协商以及零售折扣价格。在这个谈判阶段G-BA提供平台并且管理全过程,双方将按照G-BA安排好的议程进行谈判,如果在特定时间段内谈判没有达成共识,定价最终决策权将被转交给仲裁委员会。仲裁委员会将依据欧洲价格水平确定最终价格,或者,由于定价进行到这一步与新药的成本效益性关系极大,仲裁委员会可以继续要求HTA机构开展更深入的经济学评价,并且基于进一步的HTA结果来确定新药适宜的价格。然而,如果G-BA评估认为新药相比于参照药品并不具备额外效益,新药将需在上市六个月内被纳入到已有参考定价系统中,意味着该新药的年治疗成本不得高于参照药品所在参考定价药品组已设的基准线。
|
图 2 德国新药医保准入方面HTA决策转化过程 |
总之,受市场改革作用影响,在新药上市后的快速定价报销决策中,HTA被作为一种科学有效地方法嵌入到了决策过程,HTA决策转化也从原有医保准入决策扩展到药品定价谈判与决策中。
2.2 药品准入HTA决策转化成果根据实地调研所得材料,截至2015年8月10日,IQWiG已经审核进行了114份AMNOG评估(表 1),高效应对了欧洲新药上市后医保准入决策速度较慢的问题,并且保证了决策的科学性。表 1展示了2011年以来在德国许可上市的新药对比已有药品没有额外效益的占比为56%,意味着在AMNOG评估机制下一半以上的新上市药品失去了以前实际存在的不合理优势(即在相比已有药品没有额外效益的情况下还具有定相对较高价格的可能性),从而在很大程度上控制了新药价格上涨。从这个例子可见,德国在HTA决策转化上的持续探索不仅快速响应了卫生体系决策、管理需求,还为德国卫生医保系统的持久健康运营奠定了科学合理的决策基石。
| 表 1 基于AMNOG的药物评估情况汇总表 |
审视德国的HTA发展进程,德国HTA发展起步于一些研究机构、学术团体等自下而上的探索;多方利益相关者也慢慢对HTA的应用优势有了认知;在卫生医疗费用不断增长压力下,国家层面如联邦卫生部与多方利益相关者达成通过基于HTA的循证决策控制费用增长并同时确保提供质优高效服务的广泛共识;最终发展出写入社会法案的国家层面的G-BA、IQWiG以及DIMDI三大HTA组织机构。并且,根据改革发展需求,德国也在国家层面快速回应并积极出台相应法案来进一步促进HTA在更广范围的决策转化。此外,为维持这些HTA组织机构的良性发展,联邦政府提供了较为稳定的资金支持,并且培养了多学科背景的专业人才,以切实做到采用科学的评估方法以产出较高质量的HTA报告。
我国HTA决策转化的现实发展滞后,相关研究者、决策者、执行者等甚至未完全形成HTA决策转化意义的认知,部分决策者仍采用经验主义决策的做法来进行相关决策;而现有的研究者也专注于特定领域的评估活动而且学术成果无法形成有效的决策影响。德国与我国都是以社会医疗保险为主的国家,德国顺畅的HTA决策转化机制已经为其医保、卫生体系健康发展起到了关键作用。医改已经进入到深水区的我国也应认清HTA决策发展需求,加强HTA决策转化的意义认知,在持续发展现有HTA研究之上,尝试借助国家层面的政策、法定约束力量研究构建促进HTA决策转化的相关制度机制、方法路径等,真正实现HTA的循证决策价值。尤其是在卫生法的修订出台呼声渐涨的背景下,尝试将HTA这种科学的决策方法或机制纳入相关法律,并明确相关组织机构权责,尽早探索建立起我国的HTA决策转化相关制度机制有着很大的意义和必要性。此外,要真正实现我国HTA的决策转化的最大化效用,必须要保证产出的HTA具有较高的质量、较强的时效、较好的操作性等,而这些都是基于完备的HTA组织机构能力建设基础之上的,同时完备的人才梯队建设、稳健的评估研究经费支援等也很重要。
3.2 探索建立透明、多方参与的HTA决策转化方式,促进循证决策德国HTA决策转化过程中,一方面,联邦卫生部会及时根据G-BA关于HTA的最新方法、研究前沿等成果向联邦议院和联邦参议院提出相关的立法倡议;而另一方面,G-BA也会基于自身和IQWiG、DIMDI的评估报告来向医疗服务提供者、社会医疗保险基金以及患者发布相关报销指令等。这两种面向不同的决策需求而实施的分层式决策转化模式,使HTA应用决策的形式更加具有针对性和科学性,分别灵活地实现了决策制定的过程导向和效果导向。并且不论是在评估过程中还是在具体的决策转化中都有各利益相关方的广泛参与,这种广泛参与的形式也促进了有效地决策转化。此外,在这个过程中,HTA组织机构之间的互助也有利于促进决策参考报告的产出,进而加快了决策过程。尤其是G-BA和IQWiG之间,G-BA的很多决策都基于IQWiG提供的评估结果;虽然,基于法案IQWiG由G-BA建立,但是近些年来IQWiG不断发展,形成了科学的自我评估方法体系以及较为透明的评估流程等,已成长为与全球HTA金标准的英国NICE接近的独立专业机构。
我国决策转化机制并未有效建立,目前所开展的评估活动更多地停留在学术阶段,缺乏向决策转化的实现方法和路径的宣传、培训以及激励;此外,国内现有的HTA机构呈现零散分布,相互之间联系甚微,无法形成评估合力来实现有效决策辅助。参考借鉴德国的经验,在大环境中,借助政府力量,切实建立起透明的、多方参与的、具有决策影响力的HTA决策转化路径,并保证完善相关的宣传和激励等保障机制配套建设,通过完善路径引导、鼓励和促进政府真正进行循证决策。
3.3 建立国家层面的独立HTA机构并构建我国HTA决策成果共享网络平台,推进我国HTA决策转化体系建设德国基于国家层面三大HTA机构的各自HTA决策转化运行顺畅,并且HTA机构之间也形成了有效的共享机制:HTA方法指南以及HTA报告成果等不仅在G-BA、IQWiG等的官方网站中被及时公示以供各方参考学习,而且在应用早期就形成了国家层面的HTA信息库;此外,联邦公报也公布相关成果以便进行更广范围的成果传播。信息共享和广泛的成果传播不仅有利于决策转化过程,更有利于决策转化后的政策落地。
在我国,尚没有形成有影响的HTA成果共享,导致很多相类似的评估在低水平的重复进行,很大程度上浪费了研究资源,也无助于我国HTA的整体质量提升和HTA有效决策转化。查看我国目前已有的HTA组织机构官方网站信息,发现仅有国家卫计委内部评估机构网站等提供了项目介绍以及决策转化成果传播信息。国际经验证明实现HTA的整体式发展、高质量建设,不同评估机构间的成果共享网络平台建设非常必要。[10]建议首先建立国家层面的独立HTA机构,发展成熟后可尝试在省市级支援组建HTA机构,根据各地实际差异致力于地方决策转化实施,基于现实需求,进行及时、独立、客观地循证决策活动,更好地满足多元化的决策需要。同时将各HTA机构纳入同一网络实现资源共享和决策转化成果传播,积极稳妥推进我国HTA决策转化体系建设。
| [1] | Drummond M F, Schwartz J S, Jönsson B, et al. Key principles for the improved conduct of health technology assessments for resource allocation decisions[J]. International journal of technology assessment in health care, 2008, 24(3): 244–258. DOI:10.1017/S0266462308080343 |
| [2] | World Health Organization. 2015 Global Survey on Health Technology Assessment by National Authorities[R]. Geneva:WHO Document Production Services, 2015. |
| [3] | 陈英耀, 刘文彬, 耿劲松, 等. 发展我国卫生技术评估的政策建议[J]. 中国卫生质量管理, 2015, 22(1): 61–64. |
| [4] | 王海银, 何达, 王贤吉, 等. 国内外卫生技术评估应用进展及建议[J]. 中国卫生政策研究, 2014, 7(8): 19–23. |
| [5] | 陈洁, 于德志, 耿庆山. 卫生技术评估[M]. 1版. 北京: 人民卫生出版社, 2013. |
| [6] | FrickeF U, DaubenH P, 宗欣, 等. 卫生技术评估:德国视角[J]. 中国药物经济学, 2010(1): 12. |
| [7] | 李珍, 赵青. 德国社会医疗保险治理体制机制的经验与启示[J]. 德国研究, 2015(2): 9. |
| [8] | 张倩, 陈英耀, 应晓华. 法国、德国、荷兰卫生技术评估发展历程及思考[J]. 中国卫生质量管理, 2011, 18(1): 4–7. |
| [9] | Perleth M, Gibis B, Gohlen B. A short history of health technology assessment in Germany[J]. Int J Technol Assess Health Care, 2009, 25(Suppl 1): 112–119. |
| [10] | 吕兰婷, 王虎峰. 我国药品支付价格形成及谈判定价中引入卫生技术评估的路径探讨[J]. 中国药房, 2015, 26(15): 2020–2023. DOI:10.6039/j.issn.1001-0408.2015.15.02 |
(编辑 薛 云)




