随着人口老龄化加剧、心脑血管疾病及恶性肿瘤等重大疾病发病率的增加,纳入医保报销目录的新技术将越来越多。在全球卫生改革的背景下,研究证据为世界各国缓解医药费用的过快增长和科学化决策提供了更多、更有效的信息。[1, 2]循证医保决策基于最佳研究证据,结合决策情景和医疗实践现状进行决策,是将风险最小化和成本效果最大化的决策过程。[3]医保决策者需要同时考虑多种类型的研究证据,对新技术的多维度属性进行权衡。近年来,学者提出了将多准则决策分析(multi criteria decision analysis,MCDA)方法用于开展循证决策研究。证据与价值对决策的影响(Evidence and Value: Impact on Decision Making,EVIDEM)框架整合了证据和价值观,运用规范化的通用准则(核心模型)和情景化准则(情景化工具)增强决策者和研究者的交流与合作,通过科学透明的决策支持工具对MCDA进行了拓展和应用。[4-6]本研究基于EVIDEM构建新技术①的医保报销循证决策框架,为医保的循证、透明、科学决策提供方法学借鉴。
① 文中提及的“新技术”指2010年及以后通过市场准入,已上市但暂未纳入基本医疗保险报销目录的医学技术。
1 资料与方法课题组由EVIDEM协作网(EVIDEM Collaboration)授权,负责翻译EVIDEM的循证决策支持工具和方法学指南。在2015年5月10—14日赴日本参加第13届国际卫生技术评估年会期间,应邀参加了EVIDEM协作网的内部会议,咨询了协作网主席,获得了EVIDEM协作网的专家咨询问卷供参考。之后,通过Skype和E-mail进一步对研究框架进行分析和讨论,探讨将EVIDEM用于新技术医保报销循证决策的可行性。
课题组采用文献分析、专题小组讨论和定性访谈的方法在EVIDEM的基础上结合医保报销初步构建决策框架。设计医保报销决策的专家咨询问卷,通过专家咨询确定各项准则的必要性和权重,权重选用Likert 5级评分法(1分表示“完全不同意”,5分“表示完全同意”)。咨询的专家是医保报销的决策者或参与医保决策的研究者。共有14位专家同意进行咨询,包括国家的医保管理人员,参与基本药物目录制定、循证医学、卫生技术评估和卫生经济学领域的高级职称专家以及3家三级医院医保部门的负责人。专家来源地区涵盖北京、上海、四川、广东、浙江、安徽和江苏。在专家咨询过程中,如果遇到课题组难以回答的关于决策准则的概念性问题,则通过咨询EVIDEM协作网得以解答。在分析专家咨询结果时,对于部分专家提出需要进一步探讨的决策框架和决策准则,以电话询问的方式联系专家进一步了解其对准则修订的建议并选取专家一致认可的准则和子准则。
2 结果 2.1 通用准则的构建与解析在通用准则中,EVIDEM框架主要考虑五个维度的准则,即技术的需要(疾病的严重程度、影响的人群范围、未满足的要求)、技术的比较结果(相对有效性、相对安全性/耐受性、患者感知/报告的结果)、技术的益处类型(治疗学益处类型、预防的益处类型)、技术的经济性(技术成本、其它医疗成本、非医疗成本)、关于技术的知识(证据的质量、专家共识/临床指南)。[7]
结合医保决策实践,将“未满足的要求”调整为“已报销技术未满足的要求”,体现了已纳入医保的医疗技术在治愈或改善目标症状的不足之处,例如有效性、安全性、患者报道的临床结局和便捷性等方面的不足。“预防的益处类型”是从公共卫生角度,新技术在人群水平降低的疾病风险类型(例如预防、减少疾病传播和控制危险因素),然而此类新技术较少为医保决策者所考虑。将“治疗学益处类型”调整为“技术的益处类型”,归入“技术的需要”维度,从患者水平分析技术的治疗/诊断益处类型(例如缓解症状、延长生命、治愈、确诊)。关于“技术的经济性”维度,非医疗成本(例如失能成本、生产力丧失、照顾者时间)并非医保报销决策的主要影响因素。此外,将“其它医疗成本”调整为“经济性评价”(例如成本最小化分析、成本效果分析、成本效益分析、成本效用分析),因为新技术的经济学评价能够客观地体现其经济性。“关于技术的知识”维度中提及的证据质量及临床指南/专家共识,在实践应用时需要融入其它维度的准则进行分析。例如在评估新技术的相对有效性时,分析证据质量以及探讨临床有效性是否得到临床指南或专家共识的认可。研究建立的通用准则及其权重见表 1。
| 表 1 医保报销决策的通用准则 |
决策者结合技术评估报告对各项准则进行分析后,可以采用线性加权的原理为目标技术赋值(见公式1),确定新技术的医保报销优先级。
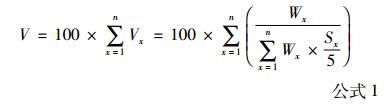
|
上式中,V代表目标技术的价值(可能的取值范围为:0~100),Wx是每个评价准则的权重,Sx是每个评价准则的评分,∑Wn是权重的加权。
2.2 情景化准则的构建与解析基于通用准则形成的量化分值可以明示决策者各维度的循证决策依据,同时确立了新技术的优先次序。情景化准则辅助将循证决策框架因地制宜地用于不同的决策情境,情境因素对医保报销决策会产生质的影响即对新技术的肯定、中立和否定。在情景化准则中,EVIDEM框架主要考虑了卫生系统的使命和任务、优先重点人群和可及性、共同的目标和特定的利益、对环境产生影响、系统的能力和对技术的合理使用、政策背景、机会成本和可负担性。
我国医保政策的主要宗旨是优先满足群众的基本医疗卫生需求,决策者需要关注新技术的纳入是否与医保的基本保障原则相符,是否会造成基金欺诈。结合医保决策,将“卫生系统的使命和任务”调整为“医保的使命和任务”。医保关注“优先重点人群和可及性”,优先重点要随着经济发展和居民健康状况的改善与时俱进。“共同的目标和特定的利益”可以成为医保决策的准则,因为意识到决策者面临的压力和利益冲突以及此类因素如何影响决策有助于确保决策的公正性。
在医保决策时,除非是放射性技术,决策者通常不会考虑技术“对环境的影响”。“系统的能力和对技术的合理使用”更多情况下是医疗机构考虑的层面,可以通过限定部分医疗机构的技术开展来实现。政策背景会影响新技术的价值判断,例如应世界卫生组织“2030年消除丙型肝炎”的愿景制定相应的丙肝药品报销政策。关于“机会成本和可负担性”,核心准则已经考虑了技术的经济性,故将该准则调整为“医保基金的可承受性”。据此,新技术医保报销决策的情景化准则见表 2。
| 表 2 医保报销决策的情景化准则 |
在我国医药卫生制度改革进一步深化的背景下,医疗保险制度作为新一轮医改的重要环节受到社会各方的普遍关注。不同医保模式的国家为循证决策提供制度保障,让决策者基于研究证据结合医疗卫生服务现状做出最佳决策。[8]全民健康覆盖需要研究证据的支持,呼吁开展循证决策。[9]医保循证决策是一个复杂的过程,决策者需要科学的决策方法支撑,才能对研究证据和价值观进行有效地整合与分析,充分利用现存的信息在不同的目标技术间进行科学、合理的分析与取舍。[10]
EVIDEM框架为系统化和一致性的循证决策提供了方法学工具。目前,一些国家和地区尝试将EVIDEM框架应用于医疗卫生决策。例如哥伦比亚在EVIDEM框架的基础上提出资源配置的决策准则[6]、加泰罗尼亚学者将其用于评估罕见病治疗药品[11]、加拿大药品咨询委员会从公共支付的角度评估用于慢性非癌性疼痛的药品曲马多[12]、南非从私人健康保险的角度提出是否报销用于宫颈癌筛查的液基细胞学涂片技术[13]。以上几项研究采用了专家咨询或利益相关方调研,结合决策情境对EVIDEM框架进行调适并确定准则的权重。修订后的EVIDEM框架多保留以下准则:技术的需要、技术的比较结果(相对有效性、相对安全性/耐受性)、技术的成本、技术的益处类型和关于技术的知识。然而,已发表的研究限于对EVIDEM框架的各准则进行取舍,并未基于新技术纳入医保报销的实践对其进行重新界定。
研究的创新性体现在基于EVIDEM,从决策者和研究者的角度初步构建了新技术医保报销循证决策框架,为将有效且具有成本效果的新技术纳入医保报销目录,以及循证制定的医保报销政策提供决策支持。多准则的新技术价值评估是一种综合性分析方法,源自为群众提供安全、有效、方便、价廉的医疗卫生服务目标,此观念贯穿于框架的各项决策准则。通用准则的赋值过程体现了决策团体基于研究证据的反思和讨论,权重确定过程则反映决策者的价值取向。
本项研究在医保循证决策支持方法尚未成熟的背景下,初步提出的循证决策框架还有待于进一步接受检验和进行调整。框架中确定的各项准则(例如技术的需要、技术的比较结果、技术的经济性)满足MCDA对准则提出的完整性、非冗余性和互相独立性要求。本文运用5分线性加权法获取权重,此方法简单、直观,能够体现研究对象的观点,在MCDA的权重确定过程中得到了应用。[12, 13]但是该方法在准则较多的情况下其区分度降低,在后续的验证性研究中需要运用其它类型的权重引导技术和不同的评分量表进一步分析。此外,有学者建议运用更多的类别例如7、9、10分量表获取权重。研究者还可以运用其它方法例如层次分析法、最好—最差评分、100分赋分法确定权重。[14]本文提出的医保循证决策框架为之后开展的研究提供理论基础。
决策者可以根据待评价的技术并结合决策情境修订研究制定的框架,以体现规范化和可行性。例如对于存在伦理学争议或是产生社会影响的新技术,还需要考虑其伦理性或社会影响。在借鉴循证决策框架进行新技术的医保报销决策时,研究者运用卫生技术评估的方法获取、评价、整合并报告各维度证据,决策者衡量新技术的核心价值并根据情景化工具进行定性分析,结合分析结果对新技术进行权衡和取舍。为了保障决策的科学性和无偏倚,遴选待评估的新技术、制订证据获取方案、评价证据的质量、整合证据的主要结果并提出推荐意见等环节应遵循公开(过程公开、结果公开)、透明(评估报告和推荐意见的产生)和中立(避免利益冲突尤其是经济利益)的原则。[15, 16]
4 小结新技术的医保决策与公众利益息息相关,基于EVIDEM的医保循证决策框架整合了证据与价值观,提供了可借鉴的决策准则。该框架适用于评估新技术和确定纳入医保报销范围的优选重点技术,将有助于提升决策的科学性和透明度。
作者声明本文无实际或潜在的利益冲突。
| [1] |
Clement F M, Harris A, Li J J, et al. Using effectiveness and cost-effectiveness to make drug coverage decisions:a comparison of Britain, Australia, and Canada[J]. JAMA, 2009, 302(13): 1437-1443. DOI:10.1001/jama.2009.1409 |
| [2] |
Majdzadeh R, Yazdizadeh B, Nedjat S, et al. 加强循证决策:不改善卫生系统管理, 可能吗?[J]. 中国卫生政策研究, 2012, 5(5): 3-8. |
| [3] |
Dionne F, Mitton C, Dempster B. Developing a multi-criteria approach for drug reimbursement decision making:an initial step forward[J]. J Popul Ther Clin Pharmacol, 2015, 22(1): e68-77. |
| [4] |
Goetghebeur M M, Wagner M, Khoury H, et al. Bridging health technology assessment (HTA) and efficient health care decision making with multicriteria decision analysis (MCDA):applying the EVIDEM framework to medicines appraisal[J]. Med Decis Making, 2012, 32(2): 376-388. DOI:10.1177/0272989X11416870 |
| [5] |
Wagner M, Khoury H, Willet J, et al. Can the EVIDEM framework tackle issues raised by evaluating treatments for rare diseases:analysis of issues and policies, and context-specific adaptation[J]. Pharmacoeconomics, 2016, 34(3): 285-301. DOI:10.1007/s40273-015-0340-5 |
| [6] |
Jaramillo HE, Goetghebeur M, Moreno-Mattar O. Testing multi-criteria decision analysis for more transparent resource-allocation decision making in Colombia[J]. Int J Technol Assess Health Care, 2016, 32(4): 307-314. DOI:10.1017/S0266462316000350 |
| [7] |
Goetghebeur MM, Wagner M, Khoury H, et al. Evidence and value:impact on decision making-the EVIDEM framework and potential applications[J]. BMC Health ServRes, 2008, 8(1): 270. |
| [8] |
Bae EY, Hong JM, Kwon HY, et al. Eight-year experience of using HTA in drug reimbursement:South Korea[J]. Health Policy, 2016, 120(6): 612-620. DOI:10.1016/j.healthpol.2016.03.013 |
| [9] |
袁蓓蓓. 全民健康覆盖:需要研究证据支持的全球运动[J]. 中国卫生政策研究, 2014, 7(2): 5-10. |
| [10] |
Kwon S H, Park S K, Byun J H, et al. Eliciting societal preferences of reimbursement decision criteria for anti cancer drugs in South Korea[J]. Expert Rev Pharmacoecon Outcomes Res, 2017, 17(4): 411-419. DOI:10.1080/14737167.2017.1277144 |
| [11] |
Gilabert-Perramon A, Torrent-Farnell J, Catalan A, et al. Drug evaluation and decision making in Catalonia:development and validation of a methodological framework based on multi-criteria decision analysis (MCDA) for orphan drugs[J]. Int J Technol Assess Health Care, 2017, 33(1): 111-120. DOI:10.1017/S0266462317000149 |
| [12] |
Tony M, Wagner M, Khoury H, et al. Bridging health technology assessment (HTA) with multicriteria decision analyses (MCDA):field testing of the EVIDEM framework for coverage decisions by a public payer in Canada[J]. BMC Health Serv Res, 2011, 11: 329. DOI:10.1186/1472-6963-11-329 |
| [13] |
Miot J, Wagner M, Khoury H, et al. Field testing of a multicriteria decision analysis (MCDA) framework for coverage of a screening test for cervical cancer in South Africa[J]. Cost Eff Resour Alloc, 2012, 10(2): 1-12. |
| [14] |
Preston CC, Colman AM. Optimal number of response categories in rating scales:reliability, validity, discriminating power, and respondent preferences[J]. Acta Psychol, 2000, 104: 1-15. DOI:10.1016/S0001-6918(99)00050-5 |
| [15] |
Marsh K, Caro JJ, Hamed A, et al. Amplifying Each Patient's Voice:A Systematic Review of Multi-criteria Decision Analyses Involving Patients[J]. Appl Health Econ Health Policy, 2017, 15(2): 155-162. DOI:10.1007/s40258-016-0299-1 |
| [16] |
Richardson HS. Intelligence and transparency in health technology assessment[J]. Int J Technol Assess Health Care, 2016, 32(1-2): 1-7. DOI:10.1017/S0266462316000143 |
(编辑 刘 博)





